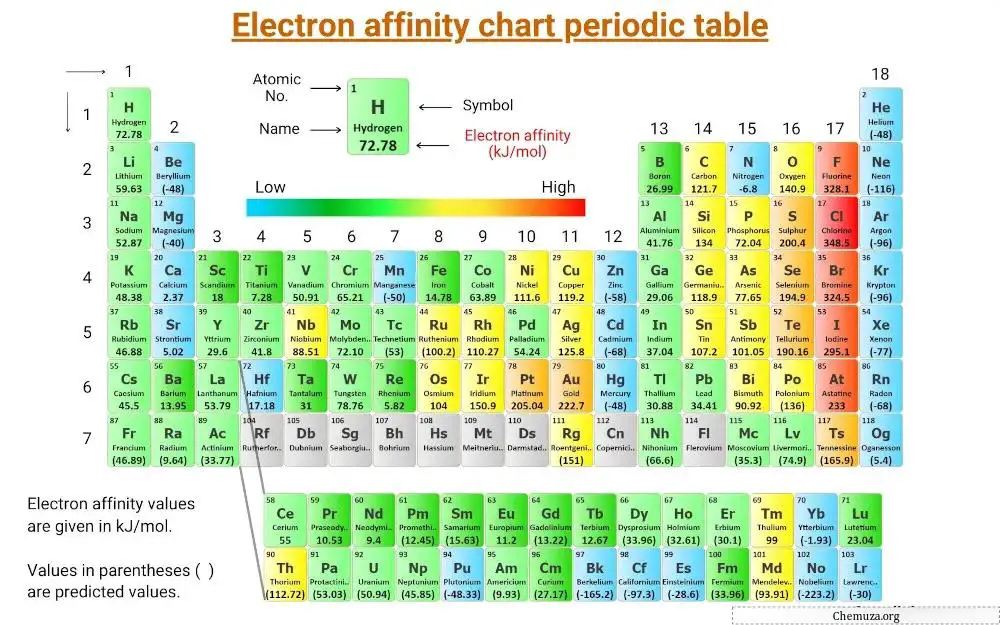
これは、元素の電子親和力を示す周期表です。
[注:電子親和力の値は kJ/mol で示されます。 ( )内の値は予測値です。
電子親和力が何なのかわからない場合は、ここで簡単に説明します。
電子親和力とは何ですか?
電子親和力は、孤立したガス原子の最外殻に電子が追加されたときに発生するエネルギー変化の尺度です。
エネルギー変化量 (ΔE とも呼ばれます) は、正、負、またはゼロのいずれかになります。
ΔE の正の値はプロセス中にエネルギーが吸収されることを示し、ΔE の負の値はエネルギーが放出されることを示します。
電子親和力 (E EA ) の符号はエネルギー変化 (ΔE) の符号と反対であり、正の E EA値は負の ΔE 値に対応し、その逆も同様です。
E EAの正の値が大きいほど、電子が中性原子に追加されるときに放出されるエネルギーが多くなります。
例:ハロゲンは高い正のEEA値を持ち、電子が最外殻に追加されると多くのエネルギーを放出することを示します。
周期表のすべての元素の電子親和力
| 要素 | 電子親和力 (kJ/mol) |
| 1 |水素(H) | 72.78 |
| 2 |ヘリウム(He) | (-48) |
| 3 |リチウム(Li) | 59.63 |
| 4 |ベリリウム(Be) | (-48) |
| 5 |ホウ素(B) | 26.99 |
| 6 |カーボン(C) | 121.77 |
| 7 |窒素(N) | -6.8 |
| 8 |酸素(O) | 140.98 |
| 9 |フローライト(F) | 328.16 |
| 10 |ネオン(Ne) | (-116) |
| 11 |ナトリウム(Na) | 52.87 |
| 12 |マグネシウム(Mg) | (-40) |
| 13 |アルミニウム(Al) | 41.76 |
| 14 |シリコン(Si) | 134.06 |
| 15 |リン(P) | 72.04 |
| 16 |硫黄(S) | 200.4 |
| 17 |塩素(Cl) | 348.57 |
| 18 |アルゴン (Ar) | (-96) |
| 19 |カリウム(K) | 48.38 |
| 20 |カルシウム(Ca) | 2.37 |
| 21 |スカンジウム (Sc) | 18 |
| 22 |チタン(Ti) | 7.28 |
| 23 |バナジウム(V) | 50.91 |
| 24 |クロム(Cr) | 65.21 |
| 25 |マンガン(Mn) | (-50) |
| 26 |鉄(Fe) | 14.78 |
| 27 |コバルト(Co) | 63.89 |
| 28 |ニッケル(Ni) | 111.65 |
| 29 |銅(Cu) | 119.23 |
| 30 |亜鉛(Zn) | (-58) |
| 31 |ガリウム(Ga) | 6月29日 |
| 32 |ゲルマニウム (Ge) | 118.93 |
| 33 |ヒ素 (As) | 77.65 |
| 34 |セレン(Se) | 194.95 |
| 35 |臭素(Br) | 324.53 |
| 36 |クリプトン (Kr) | (-96) |
| 37 |ルビジウム (Rb) | 46.88 |
| 38 |ストロンチウム(Sr) | 5.02 |
| 39 |イットリウム(Y) | 29.6 |
| 40 |ジルコニウム(Zr) | 41.8 |
| 41 |ニオブ(Nb) | 88.51 |
| 42 |モリブデン(Mo) | 72.10 |
| 43 |テクネチウム (Tc) | (53) |
| 44 |ルテニウム(Ru) | (100.27) |
| 45 |ロジウム(Rh) | 110.27 |
| 46 |パラジウム(Pd) | 54.24 |
| 47 |銀(Ag) | 125.86 |
| 48 |カドミウム(Cd) | (-68) |
| 49 |インジウム (インチ) | 37.04 |
| 50 |錫(Sn) | 107.29 |
| 51 |アンチモン(Sb) | 101.05 |
| 52 |テルル(Te) | 190.16 |
| 53 |ヨウ素(I) | 295.15 |
| 54 |キセノン(Xe) | (-77) |
| 55 |セシウム (Cs) | 45.5 |
| 56 |バリウム(Ba) | 13.95 |
| 57 |ランタン | 53.79 |
| 58 |セリウム(Ce) | 55 |
| 59 |プラセオジム (Pr) | 10.53 |
| 60 |ネオジム(Nd) | 9.4 |
| 61 |プロメチウム (Pm) | (午後12時45分) |
| 62 |サマリウム(Sm) | (15.63) |
| 63 |ユウロピウム (EU) | 11.2 |
| 64 |ガドリニウム(Gd) | (13.22) |
| 65 |テルビウム (Tb) | 12.67 |
| 66 |ジスプロシウム (Dy) | (33.96) |
| 67 |ホルミウム (Ho) | (32.61) |
| 68 |エルビウム (Er) | (30.1) |
| 69 |ツリウム (Tm) | 99 |
| 70 |イッテルビウム (Yb) | (-1.93) |
| 71 |ルテニウム(Lu) | 4月23日 |
| 72 |ハフニウム(Hf) | 午後5時18分 |
| 73 |タンタル(Ta) | 31 |
| 74 |タングステン(W) | 78.76 |
| 75 |レニウム(Re) | 5.82 |
| 76 |オスミウム(骨) | 104 |
| 77 |イリジウム(Ir) | 150.94 |
| 78 |プラチナ(Pt) | 205.04 |
| 79 |金(Au) | 222.75 |
| 80 |水銀 (Hg) | (-48) |
| 81 |タリウム(Tl) | 30.88 |
| 82 |鉛(Pb) | 34.41 |
| 83 |ビスマス(Bi) | 90.92 |
| 84 |ポロニウム (Po) | (136) |
| 85 |アスタチン (At) | 233 |
| 86 |ラドン (Rn) | (-68) |
| 87 |フランシウム (Fr) | (46.89) |
| 88 |ラジウム (Ra) | (9.64) |
| 89 |アクチニウム(Ac) | (33.77) |
| 90 |トリウム(Th) | (112.72) |
| 91 |プロタクチニウム (Pa) | (53.03) |
| 92 |ウラン(U) | (50.94) |
| 93 |ネプツニウム (Np) | (45.85) |
| 94 |プルトニウム(Pu) | (-48.33) |
| 95 |アメリシウム (Am) | (9.93) |
| 96 |キュリウム (Cm) | (27.17) |
| 97 |バーケリウム(Bk) | (-165.24) |
| 98 |カリフォルニア (参照) | (-97.31) |
| 99 |アインスタイニウム (Es) | (-28.6) |
| 100 |フェルミウム (Fm) | (33.96) |
| 101 |メンデレビウム (MD) | (93.91) |
| 102 |ノーベリウム (いいえ) | (-223.22) |
| 103 |ローレンセシウム(左) | (-30.04) |
| 104 |ラザフォージウム (Rf) | 未知 |
| 105 |ドブニウム (Db) | 未知 |
| 106 |シーボーギウム (Sg) | 未知 |
| 107 |ボーリウム (Bh) | 未知 |
| 108 |ハシウム (Hs) | 未知 |
| 109 |マイトネリウム (マウント) | 未知 |
| 110 |ダルムシュタディウム (Ds) | 未知 |
| 111 |レントゲニウム(Rg) | (151) |
| 112 |コペルニシウム (Cn) | 未知 |
| 113 |ニホニウム(Nh) | (66.6) |
| 114 |フレロビウム (フロリダ) | 未知 |
| 115 |モスコビウム (Mc) | (35.3) |
| 116 |リバモリウム(Lv) | (74.9) |
| 117 |テネシー州 (TS) | (165.9) |
| 118 |オガネソン (Og) | (5.403) |
