酢酸ニッケルは、式 Ni(CH3COO)2 で表される化合物です。ニッケルと酢酸塩成分を含むため、電気メッキや触媒合成などのさまざまな産業で使用されています。
| IUPAC名 | 酢酸ニッケル |
| 分子式 | Ni(CH3COO)2 |
| CAS番号 | 373-02-4 |
| 同義語 | 酢酸ニッケル塩、二酢酸ニッケル、酢酸ニッケル |
| インチチ | InChI=1S/2C2H4O2.Ni/c2 1-2(3)4;/h2 1H3,(H,3,4);/q;;+2/p-2 |
酢酸ニッケルの性質
酢酸ニッケルの配合
二酢酸ニッケルの化学式は、Ni(CH3COO)2 です。これは、各二酢酸ニッケル分子には 2 つの CH3COO イオンに結合した 1 つの Ni 原子が含まれていることを意味します。
酢酸ニッケルのモル質量
二酢酸ニッケルのモル質量は約 176.7 g/mol です。この値は、酢酸イオンのニッケル原子 1 個と酸素原子 4 個の原子量を加算して計算されます。
酢酸ニッケルの沸点
二酢酸ニッケルの沸点は約 140°C (284°F) です。この温度では、化合物は液体状態から気体状態に変化します。
酢酸ニッケルの融点
二酢酸ニッケルの融点は約 140°C (284°F) です。これは、固体化合物が液体に変わる温度です。
酢酸ニッケルの密度 g/mL
二酢酸ニッケルの密度は約 1.744 g/mL です。この密度値は単位体積あたりの化合物の質量を表し、液体の特性を評価するために一般的に使用されます。
酢酸ニッケルの分子量
二酢酸ニッケルの分子量は分子量とも呼ばれ、176.7 g/mol です。この値は、化合物内のすべての原子の原子量を加算することによって計算されます。
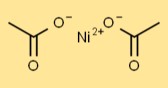
酢酸ニッケルの構造
二酢酸ニッケルの構造には、2 つの CH3COO イオンに結合した中心の Ni 原子が含まれます。酢酸イオンはニッケル原子の周囲の配位に寄与し、ニッケル原子に特定の幾何学形状を与えます。
酢酸ニッケルの溶解度
二酢酸ニッケルは水に中程度の溶解度を持っています。水に溶解して溶液を形成することができます。溶解度は、温度や溶液中の他の物質の存在によって異なります。
| 外観 | 緑色の結晶性粉末 |
| 比重 | ~1,744g/mL |
| 色 | 緑 |
| 匂い | 無臭 |
| モル質量 | ~176.7 g/モル |
| 密度 | ~1,744 g/mL |
| 融合点 | ~140°C (284°F) |
| 沸点 | ~140°C (284°F) |
| フラッシュドット | 適用できない |
| 水への溶解度 | 適度 |
| 溶解性 | 各種溶剤に可溶 |
| 蒸気圧 | 十分に文書化されていない |
| 蒸気密度 | 十分に文書化されていない |
| pKa | 十分に文書化されていない |
| pH | 十分に文書化されていない |
酢酸ニッケルの安全性と危険性
二酢酸ニッケルは潜在的な安全上のリスクをもたらします。接触または吸入すると、皮膚、目、気道を刺激する可能性があります。有害な影響を引き起こす可能性があるため、摂取を避けてください。その煙の吸入を避けるために、適切な換気が必要です。取り扱う際は手袋やゴーグルなどの適切な保護具を着用してください。適切に処分し、環境への放出を避けてください。暴露した場合は医師の診察を受けてください。二酢酸ニッケルを使用する場合は、取り扱い、保管、廃棄に伴うリスクを最小限に抑えるために、安全データシートと指示に従ってください。
| ハザードシンボル | 健康被害 |
| セキュリティの説明 | 皮膚や目の炎症を引き起こします。飲み込んだり吸入すると有害です。環境への放出を避けてください。保護具を着用してください。暴露された場合は医師の診察を受けてください。 |
| 国連識別番号 | UN3077 (クラス9) |
| HSコード | 2915.12.00 |
| 危険等級 | 9(その他の危険物) |
| 梱包グループ | Ⅲ |
| 毒性 | 中程度の毒性。飲み込んだり、吸入したり、皮膚や目に接触すると、炎症や損傷を引き起こす可能性があります。 |
酢酸ニッケルの合成方法
二酢酸ニッケルはさまざまな方法で合成できます。一般的なアプローチは、酸化ニッケル (NiO)または炭酸ニッケル (NiCO3)を酢酸 (CH3COOH)またはその誘導体と反応させることです。この反応は制御された条件下で起こり、副生成物として二酢酸ニッケルと水が生成します。別の方法では、金属ニッケルまたは水酸化ニッケル (Ni(OH)2) を酢酸またはその塩で処理し、二酢酸ニッケルの生成を促進します。
さらに、塩化ニッケル (NiCl2) などの可溶性ニッケル塩を可溶性酢酸塩と混合することにより、沈殿プロセスを使用することもできます。この混合物により二酢酸ニッケルが溶液から沈殿し、分離して収集できます。このプロセス中に慎重に pH を調整すると、最適な結果が得られます。
これらの合成方法は、化学反応における触媒や前駆体としての使用を含む、さまざまな用途の二酢酸ニッケルの製造に不可欠です。方法の選択は、必要な純度、効率、生産規模などの要因によって異なります。
酢酸ニッケルの用途
二酢酸ニッケルは、その独特の特性と化学組成により、いくつかの産業で多用途に応用されています。重要な用途には次のようなものがあります。
- 電気めっき: 二酢酸ニッケルは、電気めっきプロセスにおいてニッケル イオン源として機能します。さまざまな基材上へのニッケルの薄層の堆積を容易にし、耐食性を向上させ、装飾的な仕上げを提供します。
- 触媒合成: 化学者は、複数の化学反応の触媒を作成するための前駆体としてそれを使用します。石油化学や製薬などの産業は、ニッケル含有触媒に大きく依存しています。
- 繊維産業: 繊維の染色プロセスにおいて、染料を生地の繊維に固定し、染料の付着性と色堅牢度を向上させるのに役立ちます。
- 実験用試薬: 科学者は、特定の化合物を検出および同定するための試薬として二酢酸ニッケルを使用し、特定の官能基をテストできるようにします。
- 表面処理: メーカーは、プリント基板の製造などの表面処理用途にこれを適用します。銅表面に保護層を形成するのに役立ちます。
- 有機合成: さまざまな有機合成反応において、二酢酸ニッケルは炭素-炭素結合および炭素-ヘテロ原子結合の形成において重要な役割を果たします。
- ガス精製: ガス精製プロセス、特に工業用ガスから硫化水素などの不純物を除去する際に重要な役割を果たします。
- 分析化学: 二酢酸ニッケルは分析化学の標準試薬であり、校正と品質管理の目的で使用されます。
全体として、二酢酸ニッケルの多様な用途は、製品の美観の向上から重要な化学変換やプロセスの支援に至るまで、業界全体でのその重要性を浮き彫りにしています。
質問:
Q: アセタールとニッケルを 1 つのループで混合できますか?
A: アセタールとニッケルをバックルに混合することは、一般的に推奨されません。アセタールは特定の金属と反応し、バックルのコンポーネントに腐食や損傷を引き起こす可能性があるためです。
Q: イオン性化合物酢酸ニッケルの正しい式は何ですか?
A: イオン性化合物である二酢酸ニッケルの正しい式は、Ni(CH3COO)2 です。
Q: 酢酸ニッケル(ii) + 臭化鉄(ii) には実験式がありますか?
A: 二酢酸ニッケル(II)と臭化鉄(II)は直接化合物を形成しないため、実験式は適用できません。
Q: アセタールニッケルウォーターブロックとは何ですか?
A: アセタール ニッケル ウォーター ブロックとは、PC 液冷システムで使用される冷却コンポーネントを指し、通常はアセタール プラスチックで作られ、表面がニッケルメッキされています。
Q: ニッケルと銅と酢酸の反応速度はどのくらいですか?
A: ニッケルと銅は酢酸とゆっくりと反応し、水素ガスを放出してそれぞれの二酢酸塩を形成します。
Q: 酢酸ニッケルはどのようにして作られるのですか?
A: 二酢酸ニッケルは、酸化ニッケルまたは炭酸ニッケルを酢酸と反応させ、結晶化および精製することによって製造できます。
Q: 酢酸ニッケルを除去するにはどうすればよいですか?
A: 二酢酸ニッケルは、地域の規制に従って有害廃棄物として処分してください。適切な廃棄方法については、廃棄物管理当局に相談することが重要です。
Q: 酢酸ニッケル(ii)の式は何ですか?
A: 二酢酸ニッケル(II)の化学式は Ni(CH3COO)2 です。
Q: 酢酸ニッケルは溶けますか?
A: はい、二酢酸ニッケルは水に適度に溶け、さまざまな用途に使用できる溶液を形成します。
