酢酸カリウム (C2H3KO2) は、カリウム、炭素、水素、酸素で構成される化合物です。食品業界では防腐剤として、また空港の滑走路の凍結防止剤として一般的に使用されています。
| IUPACの名称 | 酢酸カリウム |
| 分子式 | C2H3KO2 |
| CAS番号 | 127-08-2 |
| 同義語 | KAc、エタン酸カリウム |
| インチチ | InChI=1S/C2H4O2.K/c1-2(3)4;/h1H3,(H,3,4);/q;+1/p-1 |
酢酸カリウムの性質
酢酸カリウムの配合
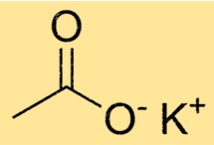
酢酸カリウムの化学式はC2H3KO2です。 K+ イオンと CH3COO- イオンから構成されます。酢酸イオンは多原子であり、複数の原子が結合して構成されています。酢酸塩の場合、それは 2 つの炭素原子、3 つの水素原子、2 つの酸素原子で構成されています。
酢酸カリウムのモル質量
C2H3KO2 のモル質量は 98.14 g/mol です。モル質量は物質 1 モルの質量であり、分子内のすべての原子の原子質量を加算することによって計算されます。 C2H3KO2 の場合、カリウム、炭素、水素、酸素の原子量が追加されてモル質量に達します。
酢酸カリウムの沸点
C2H3KO2 の沸点は 881°C (1618°F) です。沸点とは、物質が液体から気体に変化する温度です。 C2H3KO2 は他の化合物に比べて沸点が比較的高く、これはそのイオン性と、正に帯電したカリウムイオンと負に帯電した酢酸イオン間の強い引力に起因すると考えられます。
酢酸カリウム 融点
C2H3KO2 の融点は 292°C (558°F) です。融点とは、固体が液体に変わる温度です。 C2H3KO2 は比較的高い融点を持っていますが、これはそのイオン性と、正に帯電したカリウム イオンと負に帯電した酢酸イオン間の強い引力に起因すると考えられます。
酢酸カリウムの密度 g/mL
C2H3KO2 の密度は 1.57 g/mL です。密度は物質の単位体積あたりの質量です。 C2H3KO2 の比較的高い密度は、そのイオン性と結晶格子内のイオンのコンパクトな配置に起因すると考えられます。
酢酸カリウムの分子量
C2H3KO2 の分子量は 98.14 g/mol です。分子量は、分子内のすべての原子の原子量の合計です。 C2H3KO2 の場合、カリウム、炭素、水素、酸素の原子量の合計です。
酢酸カリウムの構造
C2H3KO2 はイオン性の結晶構造を持っています。正に帯電した K+ イオンと負に帯電した CH3COO- イオンから構成されます。酢酸イオンは、各炭素原子が酸素原子と水素原子に結合して平面状に配置されています。カリウムイオンは酢酸イオンの面の間に位置し、三次元の結晶格子を形成します。
| 外観 | 白色の結晶性粉末 |
| 比重 | 1.57g/cm3 |
| 色 | 無色 |
| 匂い | 無臭 |
| モル質量 | 98.14g/モル |
| 密度 | 1.57g/ml |
| 融合点 | 292°C (558°F) |
| 沸点 | 881°C (1618°F) |
| フラッシュドット | 適用できない |
| 水への溶解度 | 水に非常に溶けやすい |
| 溶解性 | エタノール、メタノールに可溶 |
| 蒸気圧 | 適用できない |
| 蒸気密度 | 適用できない |
| pKa | 4.76 |
| pH | 7(10%水溶液) |
酢酸カリウムの安全性と危険性
C2H3KO2 は一般に、毒性が低く、発がん性や変異原性の影響は知られていないため、人体での使用には安全であると考えられています。ただし、皮膚や目に刺激を与える可能性があり、長期間または繰り返し暴露すると皮膚炎を引き起こす可能性があります。また、気道に対して軽度の刺激性があり、大量に吸入すると咳や息切れを引き起こす可能性があります。摂取すると、胃腸の炎症、吐き気、嘔吐を引き起こす可能性があります。さらに、C2H3KO2 は特定の化学物質と反応して、酢酸や水酸化カリウムなどの危険な副産物を生成する可能性があります。したがって、不適合物質との接触を避けるために、慎重に取り扱い、適切に保管する必要があります。
| ハザードシンボル | なし |
| セキュリティの説明 | 熱、火花、炎から遠ざけてください。摂取、吸入、皮膚や目との接触を避けてください。手袋と保護メガネを着用してください。 |
| ID | UN2923 |
| HSコード | 2915.29.10 |
| 危険等級 | 8 |
| 梱包グループ | Ⅲ |
| 毒性 | 毒性が低い。皮膚、目、気道を刺激する可能性があります。経口摂取すると、胃腸の炎症、吐き気、嘔吐を引き起こす可能性があります。 |
酢酸カリウムの合成法
C2H3KO2 を合成するには、水酸化カリウムを酢酸で中和するか、炭酸カリウムと酢酸を反応させるか、金属カリウムと酢酸を反応させる必要があります。
中和法では、pHが中性レベルに達するまで水酸化カリウム溶液に酢酸をゆっくりと加えます。このプロセスにより、C2H3KO2 と水が生成されます。次に、実験者は得られた溶液を蒸発させ、C2H3KO2 の白色結晶固体を取得します。
この方法では、酢酸と炭酸カリウムの混合物を完全に加熱する必要があります。その後、混合物をろ過して残りの固体を除去し、蒸発させて結晶化させて C2H3KO2 を取得します。
カリウム金属と酢酸の反応は、C2H3KO2 を合成する別の方法です。このプロセスでは、金属カリウムを酢酸溶液に添加し、C2H3KO2 と水素ガスを生成します。次に、溶液を蒸発させて C2H3KO2 を結晶化させると、抽出が可能になります。
酢酸カリウムの用途
C2H3KO2 は、次のようなさまざまな業界で幅広く使用されています。
除氷剤: 従来の塩ベースの除氷剤が環境に悪影響を与える可能性がある空港の滑走路、橋、その他の表面で除氷剤として一般的に使用されます。
食品保存料: 特定の食品の腐敗を防ぎ、保存期間を延ばすための食品保存料として使用されます。
緩衝剤:医薬品、繊維、化粧品など様々な業界で緩衝剤として使用されています。
触媒: 無水酢酸などの特定の化学物質の製造における触媒として使用されます。
実験用試薬: さまざまな分析および研究目的に使用される一般的な実験用試薬。
動物用飼料添加物: 成長と全体的な健康を改善するために、家畜、特に家禽や豚の飼料の飼料添加物として使用されます。
難燃剤: 火災の危険を軽減するために、一部のプラスチックや繊維に難燃剤として使用されます。
医療用途: 低カリウム血症 (カリウムレベルの低下) の治療や一部の透析液の成分など、一部の医療用途でも使用されます。
質問:
Q: 酢酸カリウムは溶けますか?
A: はい、C2H3KO2 は水に溶けます。
Q: 酢酸カリウムの式は何ですか?
A: 酢酸カリウムの式は CH3CO2K です。
Q: 酢酸カリウムは何に使われますか?
A: C2H3KO2 は、除氷剤、食品保存料、緩衝剤、触媒、実験用試薬、動物飼料添加物、難燃剤、および一部の医療用途など、さまざまな目的に使用されています。
Q: 酢酸カリウムは水に溶けますか?
A: はい、C2H3KO2 は水に溶けます。
Q: 酢酸カリウムは酸ですか、それとも塩基ですか?
A: C2H3KO2 は酸でも塩基でもありませんが、溶液中で安定した pH を維持するのに役立つ緩衝剤として機能します。
