過塩素酸ナトリウムは、式 NaClO4 の化合物です。これは白色の結晶性固体であり、水への溶解度が高く、さまざまな工業プロセスで酸化剤として一般的に使用されます。
| IUPAC名 | 過塩素酸ナトリウム |
| 分子式 | NaClO4 |
| CAS番号 | 7601-89-0 |
| 同義語 | 過塩素酸、ナトリウム塩;過塩素酸ナトリウム (フランス);過塩素酸ナトリウム (ドイツ語); Perclorato di sodio (イタリア語);ペルクロラート・ソディコ (スペイン語);国連 1502 |
| インチチ | InChI=1S/ClHO4.Na/c2-1(3,4)5;/h(H,2,3,4,5);/q;+1/p-1 |
過塩素酸ナトリウムの性質
過塩素酸ナトリウムの配合
過塩素酸ナトリウムの化学式は NaClO4 です。これは、化合物が 1 つのナトリウム原子、1 つの塩素原子、および 4 つの酸素原子で構成されていることを意味します。過塩素酸ナトリウムは、さまざまな工業プロセスで一般的に使用される強力な酸化剤です。
過塩素酸ナトリウムのモル質量
NaClO4 のモル質量は 122.44 g/mol です。これは、1 モルの NaClO4 に 122.44 グラムの化合物が含まれていることを意味します。化合物のモル質量は、化学反応に必要な物質の量を決定する際に重要です。
過塩素酸ナトリウムの沸点
NaClO4 の沸点は 545°C (1013 hPa) です。これは、化合物が液体から気体に変化する温度です。 NaClO4 は、ナトリウムと過塩素酸イオン間の強い静電力により沸点が高くなります。
過塩素酸ナトリウム 融点
NaClO4 の融点は 482°C です。これは、化合物が固体状態から液体状態に変化する温度です。 NaClO4 は、ナトリウムと過塩素酸イオン間の強い静電力により融点が高くなります。
過塩素酸ナトリウムの密度 g/mL
NaClO4 の密度は 2.52 g/mL です。これは、1 ミリリットルの NaClO4 の重さが 2.52 グラムであることを意味します。物質の密度は、浮力や粘度などの物理的特性を決定する際に重要です。
過塩素酸ナトリウムの分子量
NaClO4 の分子量は 122.44 g/mol です。これは、化合物内のナトリウム、塩素、酸素原子の原子量の合計です。化合物の分子量は、その物理的および化学的特性を決定する際に重要です。
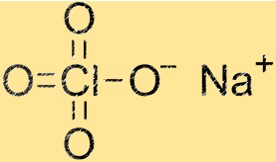
過塩素酸ナトリウムの構造
NaClO4 の構造は、Na+ カチオンと ClO4- アニオンから構成される結晶格子です。ナトリウム陽イオンは 4 つの酸素原子に囲まれていますが、ClO4- 陰イオンは 1 つの塩素原子と 4 つの酸素原子で構成されています。結晶格子構造は、NaClO4 にその特徴的な物理的および化学的特性を与えます。
過塩素酸ナトリウムの溶解度
NaClO4 は水への溶解度が高く、20℃での溶解度は 209 g/100 mL です。これは、大量の NaClO4 が少量の水に溶解できることを意味します。 NaClO4 は溶解度が高いため、ロケット燃料用の過塩素酸アンモニウムの製造など、さまざまな工業プロセスで役立ちます。
| 外観 | 白色の結晶固体 |
| 比重 | 2.52g/ml |
| 色 | 白 |
| 匂い | 無臭 |
| モル質量 | 122.44 g/モル |
| 密度 | 2.52g/ml |
| 融合点 | 482℃ |
| 沸点 | 545℃(1013hPa) |
| フラッシュドット | 適用できない |
| 水への溶解度 | 209 g/100 mL(20℃) |
| 溶解性 | 水とエタノールに溶ける |
| 蒸気圧 | 利用不可 |
| 蒸気密度 | 利用不可 |
| pKa | 利用不可 |
| pH | 利用不可 |
過塩素酸ナトリウムの安全性と危険性
NaClO4 は危険な化合物であり、注意して取り扱う必要があります。これは強力な酸化剤であり、有機物質、還元剤、その他の化学物質と激しく反応する可能性があります。 NaClO4 の粉塵や蒸気にさらされると、目、皮膚、呼吸器系に炎症を引き起こす可能性があります。 NaClO4 を摂取すると、胃腸の炎症、吐き気、嘔吐を引き起こす可能性があります。 NaClO4 は水生生物にも有害なので、適切に処分する必要があります。 NaClO4 を取り扱うときは、暴露を避けるために手袋、ゴーグル、呼吸用保護具などの個人用保護具を着用する必要があります。事故のリスクを最小限に抑えるためには、適切な換気と保管も重要です。
| ハザードシンボル | ああ、Xn |
| セキュリティの説明 | 粉塵、煙霧、ガス、ミスト、蒸気、スプレーを吸入しないでください。保護手袋/保護服/保護眼鏡/保護面を着用してください。吸入した場合: 傷病者を新鮮な空気の場所に移し、呼吸しやすい姿勢で休ませてください。飲み込んだ場合: 口をすすぐ。嘔吐を誘発しないでください。気分が悪くなった場合は、中毒センターまたは医師に連絡してください。 |
| 国連識別番号 | UN1502 |
| HSコード | 2829.90.90 |
| 危険等級 | 5.1 |
| 梱包グループ | Ⅱ |
| 毒性 | 飲み込むと有毒、吸入したり皮膚に接触すると有害です。刺激や腐食を引き起こす可能性があります。 |
過塩素酸ナトリウムの合成方法
NaClO4 はさまざまな方法で合成できます。
一般的な方法では、塩素酸ナトリウムと塩酸を反応させ、NaClO4 と塩化ナトリウムを生成します。
別の方法には、過塩素酸塩の存在下での塩化ナトリウム溶液の電気分解が含まれます。塩化ナトリウムから塩素酸ナトリウムへの変換が起こり、続いて塩酸を添加すると NaClO4 に変換されます。
別のアプローチは、硫酸の存在下で塩素酸ナトリウムと塩化ナトリウムを反応させることである。この方法では、NaClO4 と硫酸ナトリウムの混合物が生成され、分別結晶化によって分離できます。
別の方法では、塩素酸ナトリウムと過塩素酸アンモニウムを反応させ、NaClO4 と塩化アンモニウムを生成します。固体ロケット推進剤の酸化剤として一般的に使用される NaClO4 の製造には、この方法が使用されます。
塩酸の存在下で次亜塩素酸ナトリウムと塩素酸ナトリウムを反応させると、NaClO4 も合成されます。この方法では、主生成物として NaClO4 と塩化ナトリウムが生成されます。
過塩素酸ナトリウムの用途
NaClO4 は、さまざまな業界でさまざまな用途に使用されます。 NaClO4 の一般的な用途をいくつか示します。
- ロケット推進剤: 酸素含有量が高く安定性が高いため、固体ロケット推進剤の酸化剤として一般的に使用されます。
- 火工品: フレア、花火、照明弾などの火工品組成物の酸化剤として使用されます。
- 分析化学: 分析化学において、さまざまなサンプル中のイオンを測定するための過塩素酸イオン源として使用されます。
- 電気めっき: めっき浴の導電性と安定性を向上させるために、電気めっき溶液の成分として使用されます。
- 電池: 溶解度が高く、電池の電気化学的特性を改善する能力があるため、リチウムイオン電池の電解質として使用されます。
- 医療用途: ヨウ素輸送の競合阻害剤として甲状腺疾患の治療に使用されます。医療画像用の造影剤の製造にも使用されます。
- 水処理: 消毒剤として水処理で使用され、水から特定の汚染物質を除去します。
質問:
Q: 過塩素酸ナトリウムの式は何ですか?
A: NaClO4。
Q: 過塩素酸ナトリウムは水に溶けますか?
A: はい、NaClO4 は水によく溶けます。
Q: 過塩素酸ナトリウムは酸ですか、それとも塩基ですか?
A: NaClO4 は酸でも塩基でもありません。それは塩です。
Q: 過塩素酸アンモニウムと臭化ナトリウムの反応は何ですか?
A: 反応は NH4ClO4 + NaBr → NaClO4 + NH4Br です。
Q: 過塩素酸ナトリウムにはナトリウムイオンが何個含まれていますか?
A: NaClO4 にはナトリウムイオンが存在します。
Q: NaClO4 は酸ですか、それとも塩基ですか?
A: NaClO4 は酸でも塩基でもありません。それは塩です。
Q: NaClO4 溶液にはどのような溶解種が存在しますか?
A: NaClO4 溶液では、溶解種は Na+ イオンと ClO4- イオンです。
Q: 3.30 モルの NaClO4 には何モルの酸素が含まれますか?
A: 3.30 モルの NaClO4 には 13.2 モルの酸素が含まれています。
Q: NaClO4 は水に溶けますか?
A: はい、NaClO4 は水によく溶けます。
Q: 1.10 モルの NaClO4 には何モルの酸素が含まれますか?
A: 1.10 モルの NaClO4 には 4.4 モルの酸素が含まれています。
