硝酸鉄IIIは化合物です。鉄イオンと硝酸イオンが結合して生成されます。産業用途や実験室用試薬として一般的に使用されています。
| IUPAC名 | 硝酸鉄(III) |
| 分子式 | Fe(NO3)3 |
| CAS番号 | 10421-48-4 |
| 同義語 | 硝酸第二鉄、三硝酸鉄、硝酸鉄(III)塩 |
| インチチ | InChI=1S/Fe.3NO3/c;3 2-1(3)4/q+3;3 -1 |
硝酸鉄(III)の性質
硝酸鉄(III)の式
硝酸鉄IIIの化学式はFe(NO3)3です。 1 つの鉄イオン (Fe) と 3 つの硝酸イオン (NO3) で構成されています。この式は、鉄カチオンと硝酸アニオンの組み合わせを表します。
硝酸鉄(III) モル質量
硝酸鉄のモル質量は、その構成元素の原子質量を加算することで計算できます。鉄 (Fe) のモル質量は 55.845 g/mol ですが、各硝酸イオン (NO3) のモル質量は 62.0049 g/mol です。これらの値を加算すると、硝酸鉄のモル質量は約 241.86 g/mol となります。
硝酸鉄(III)の沸点
硝酸鉄には特定の沸点がありません。加熱するとさまざまな窒素酸化物に分解され、最終的には酸化鉄が形成されます。分解温度は、濃度や他の物質の存在などの要因によって異なります。
硝酸鉄(III)の融点
硝酸鉄の融点は約 47°C (117°F) です。この温度では、固体化合物は液体状態に変わります。融点は、不純物や化合物の正確な組成などの要因によってわずかに異なる可能性があることに注意することが重要です。
硝酸鉄(III)の密度 g/mL
Fe(NO3)3 の密度は約 1.68 g/mL です。密度は物質の単位体積あたりの質量を表します。この場合、化合物 1 ミリリットルあたりの Fe(NO3)3 の質量を示します。
硝酸鉄(III)の分子量
硝酸鉄の分子量は約 241.86 g/mol です。分子量とは、分子内のすべての原子の原子量の合計を指します。
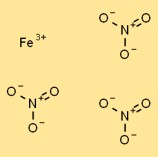
硝酸鉄(III)の構造
硝酸鉄は固体の状態では結晶構造を持っています。これは、配位した硝酸アニオン (NO3-) に囲まれた Fe3+ カチオンで構成されています。鉄カチオンはイオン結合によって結合されていますが、硝酸アニオンは静電気力によってカチオンに引き寄せられます。
硝酸鉄(III)の溶解度
硝酸鉄は水に非常に溶けます。水に容易に溶解し、透明な淡黄色の溶液を形成します。他の溶媒または物質における硝酸鉄の溶解度は異なる場合があります。
| 外観 | 淡黄色の結晶 |
| 比重 | 1.68 |
| 色 | 淡い黄色 |
| 匂い | 無臭 |
| モル質量 | 241.86 g/モル |
| 密度 | 1.68g/ml |
| 融合点 | 47°C (117°F) |
| 沸点 | 分解された |
| フラッシュドット | 適用できない |
| 水への溶解度 | 非常に溶けやすい |
| 溶解性 | 水および極性溶媒に可溶 |
| 蒸気圧 | 利用不可 |
| 蒸気密度 | 利用不可 |
| pKa | 利用不可 |
| pH | 酸 |
硝酸鉄(III)の安全性と危険性
硝酸鉄には安全上のリスクがいくつかあるため、取り扱いには注意が必要です。皮膚、目、呼吸器系を刺激すると考えられています。化合物との直接接触は避け、手袋やゴーグルなどの保護具を着用する必要があります。硝酸鉄を摂取または吸入すると有害な影響が生じる可能性があるため、摂取または吸入しないでください。吸入のリスクを最小限に抑えるために、この化合物を換気の良い場所で作業することが重要です。誤って暴露または摂取した場合は、直ちに医師の診察を受ける必要があります。安全を確保するために、適切な保管および取り扱い方法に従う必要があります。
| ハザードシンボル | シー・オー |
| セキュリティの説明 | 皮膚や目の炎症を引き起こします。呼吸器への刺激を引き起こす可能性があります。飲み込むと有害。 |
| 国連識別番号 | UN 1466 (無水) |
| HSコード | 28342990 |
| 危険等級 | 5.1 (酸化剤) |
| 梱包グループ | Ⅱ |
| 毒性 | 中程度の毒性 |
硝酸鉄(III)の合成方法
硝酸鉄はさまざまな方法で合成できますが、一般的な方法は酸化鉄(III) (Fe2O3) を濃硝酸 (HNO3) に溶解することです。この反応により、次の方程式で表される硝酸鉄が生成されます。
濃硝酸は酸化鉄(III)を溶解し、Fe(NO3)3と水を生成します。
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O。
別の方法では、金属鉄を硝酸と過酸化水素の混合物と組み合わせ、鉄を酸化して硝酸鉄を形成します。この有名な反応は「王水」法と呼ぶにふさわしいものです。
硝酸と過酸化水素の混合物に金属鉄を加えると、硝酸鉄と水が生成されます。
2Fe + 8HNO3 + 6H2O2 → 2Fe(NO3)3 + 6H2O。
含まれる化学物質には腐食性と酸化性があるため、これらの反応を実行する場合は注意することが重要です。保護具を着用し、換気の良い場所で作業するなど、適切な安全対策を講じる必要があります。
評判の良い化学物質供給業者は市販の硝酸鉄を提供しており、産業や研究室でのさまざまな用途に一貫した信頼性の高い化合物の供給源を確保しています。
硝酸鉄(III)の用途
硝酸鉄は、さまざまな産業や研究室でいくつかの実用的な用途があります。硝酸鉄の主な用途をいくつか紹介します。
- 工業用触媒: ナイロンやその他のポリマーの製造を含むいくつかの工業プロセスでは、硝酸鉄が触媒として使用されます。
- 染色および顔料: 染色および顔料業界では、染料を布地に固定し、色の堅牢性を向上させる媒染剤として硝酸鉄を使用しています。
- エッチング剤: 金属加工およびエレクトロニクス産業では、金属表面に複雑なパターンやデザインを作成するために硝酸鉄をエッチング剤として使用します。
- 実験用試薬: 硝酸鉄は、さまざまな化学反応や実験、特に他の化合物の合成のための一般的な実験用試薬として機能します。
- 酸化剤: 硝酸鉄は、その強力な酸化特性により、有機合成を含む化学反応において酸化剤として機能します。
- 水処理: 硝酸鉄は、水処理プロセスで産業廃水からリン酸塩や硫化物などの不純物を除去するのに役立ちます。
- 写真: 一部の写真プロセス、特に鉄ベースの写真乳剤の調製では、硝酸鉄が使用されます。
- 分析化学: 硝酸鉄は、特定の物質を検出および定量するための比色分析などの分析化学技術に応用されています。
- 木材の保存: 木材の保存処理は有効成分として硝酸鉄を使用し、木材を菌類の腐敗や昆虫の侵入から保護します。
- 医薬品への応用: 特定の医薬品や医薬品の製剤には硝酸鉄が使用されます。
硝酸鉄は腐食性と酸化性があるため、硝酸鉄を扱う場合は適切な取り扱いと安全上の注意事項に従う必要があることに注意することが重要です。
質問:
Q: 硝酸鉄(III)は可燃性ですか?
A: いいえ、硝酸鉄は可燃性ではありません。
Q: 硝酸鉄(III)の安全性と取り扱い上の懸念は何ですか?
A: 安全性に関する懸念には、皮膚、目、気道への刺激が含まれます。したがって、適切な保護具と予防措置を講じて取り扱う必要があります。
Q: 硝酸鉄(III)を表す式は何ですか?
A: 硝酸鉄の化学式は Fe(NO3)3 です。
Q: 硝酸鉄(III)の式は何ですか?
A: 硝酸鉄(III) の化学式は Fe(NO3)3 です。
Q: 硝酸鉄(III)のモル質量は何ですか?
A: Fe(NO3)3 のモル質量は約 241.86 g/mol です。
Q: 水酸化鉄は水に溶けますか?
A: 水酸化鉄は水に溶けにくいです。
Q: 硝酸鉄(III)と反応しますか?
A: いいえ、カルシウム (Ca) は通常、Fe(NO3)3 と反応しません。
Q: 硝酸鉄(III) はアスピリンのどの部分と反応しますか?
A: 硝酸鉄(III) は、アスピリン分子に存在するカルボン酸基 (-COO-) と反応します。
Q: 硝酸鉄(III)の分子量はどれくらいですか?
A: Fe(NO3)3 の分子量は約 241.86 g/mol です。
Q: Al は硝酸鉄(III) と反応しますか?
A: はい、アルミニウム (Al) は Fe(NO3)3 と反応して硝酸アルミニウムと金属鉄を形成します。
Q: 3.80 M 硝酸鉄(III) 溶液では、50.0 g の水に何モルの硝酸塩が溶解しますか?
A: 硝酸塩のモルを決定するには、水のモル濃度と質量のみが提供されるため、溶液の体積が必要です。
