炭酸ニッケル (NiCO3) は、ニッケルイオンと炭酸イオンから生成されます。これは、その独特の特性によりセラミックや触媒に使用される緑色の固体です。
| IUPAC名 | 炭酸ニッケル(II) |
| 分子式 | NiCO3 |
| CAS番号 | 3333-67-3 |
| 同義語 | 炭酸ニッケル;炭酸、ニッケル塩、一炭酸ニッケル |
| インチチ | InChI=1S/CH2O3.Ni/c2-1(3)4;/h(H2,2,3,4);/q;+2 |
炭酸ニッケルの性質
炭酸ニッケル配合
一炭酸ニッケルの化学式は NiCO3 です。 1 つのニッケル (Ni) 原子、1 つの炭素 (C) 原子、3 つの酸素 (O) 原子で構成されています。
炭酸ニッケルのモル質量
一炭酸ニッケル (NiCO3) のモル質量は、1 モルあたり約 118.7 グラムです。この値は、構成元素の原子量を合計することによって得られます。
炭酸ニッケルの沸点
一炭酸ニッケルは沸点に達する前に分解する傾向があるため、明確な沸点がありません。加熱すると酸化ニッケル、二酸化炭素、酸素に分解します。
炭酸ニッケルの融点
一炭酸ニッケルの融点は約 200°C (392°F) です。この温度では固体から液体に変化します。
炭酸ニッケルの密度 g/mL
一炭酸ニッケルの密度は、1 立方センチメートルあたり約 3.6 グラム (g/cm3) です。この密度値は、単位体積あたりの化合物の質量を示します。
炭酸ニッケルの分子量
一炭酸ニッケル (NiCO3) の分子量は 1 モルあたり約 118.7 グラムです。構成原子の原子量を加算することで計算されます。
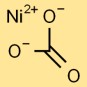
炭酸ニッケルの構造
一炭酸ニッケルは、中心のニッケル原子と 3 つの酸素原子が三角形の配置で結合した基本構造を持っています。これが炭酸イオンの核を形成します。この構造はイオン結合と共有結合によって結合されています。
炭酸ニッケルの溶解度
一炭酸ニッケルは水に溶けにくいです。溶液の pH が低下すると、その溶解度は増加します。塩酸などの物質を含む酸性溶液にも溶解します。
一炭酸ニッケルの特性により、さまざまな用途に役立ちます。水に溶けないため、セラミックや顔料の用途に適しています。高温での分解は、触媒プロセスでの使用に貢献します。
| 外観 | 緑色に点灯 |
| 比重 | 3.6g/cm3 |
| 色 | 緑 |
| 匂い | 無臭 |
| モル質量 | 118.7g/モル |
| 密度 | 3.6g/cm3 |
| 融合点 | 200°C (392°F) |
| 沸点 | 沸騰する前に分解してしまう |
| フラッシュドット | 適用できない |
| 水への溶解度 | 難溶性 |
| 溶解性 | 塩酸などの酸に溶ける |
| 蒸気圧 | 利用不可 |
| 蒸気密度 | 利用不可 |
| pKa | 適用できない |
| pH | 適用できない |
炭酸ニッケルの安全性と危険性
一炭酸ニッケルは潜在的な安全上のリスクをもたらします。接触すると皮膚や目を刺激し、発赤や不快感を引き起こす可能性があります。その粉塵や蒸気を吸入すると、気道の炎症や咳を引き起こす可能性があります。手袋やメガネなどの適切な保護具を着用し、慎重に取り扱うことをお勧めします。化合物を摂取または吸入しないでください。暴露した場合は、患部を洗い、症状が続く場合は医師の診察を受けてください。リスクを最小限に抑えるには、適切な換気と封じ込め対策が不可欠です。一炭酸ニッケルを扱う場合は、安全プロトコルに従うことが、潜在的な健康上の問題を防ぎ、安全な環境を確保するために非常に重要です。
| ハザードシンボル | 刺激物、健康被害 |
| セキュリティの説明 | 刺激性;接触や吸入を避けてください。取り扱い注意 |
| 国連識別番号 | 帰属されていない |
| HSコード | 2836.40.00 |
| 危険等級 | 未分類 |
| 梱包グループ | 未分類 |
| 毒性 | 皮膚や目に炎症を引き起こす可能性があります。吸入すると呼吸器刺激 |
炭酸ニッケルの合成法
一炭酸ニッケルはさまざまな方法で合成できます。一般的なアプローチには、水中での可溶性ニッケル塩 (塩化ニッケルや硫酸ニッケルなど) と可溶性炭酸塩 (炭酸ナトリウムなど) の反応が含まれます。 2 つの溶液を混合すると、緑色の沈殿物の形で不溶性の一炭酸ニッケルが形成されます。次いで、この沈殿物を濾過し、洗浄し、乾燥させて、最終生成物を得る。
別の方法では、水分の存在下で酸化ニッケルまたは水酸化ニッケルと二酸化炭素ガスとを反応させる。これにより、水と一炭酸ニッケルが形成されます。このプロセスは、一炭酸ニッケルを製造するために工業的によく使用されます。
さらに、可溶性ニッケル塩の溶液を可溶性炭酸塩の溶液と混合することにより、沈殿プロセスを使用することができる。得られた混合物を撹拌し、生成した一炭酸ニッケルの沈殿物を集めて処理する。
これらの合成方法により、セラミック、触媒、顔料などのさまざまな用途に使用される一炭酸ニッケルが生成されます。高品質の一炭酸ニッケル製品を得るには、反応条件と精製ステップを注意深く制御することが重要です。
炭酸ニッケルの用途
一炭酸ニッケルは、そのユニークな特性によりさまざまな用途に使用されます。重要な用途には次のようなものがあります。
- セラミックとガラスの製造: 一炭酸ニッケルは、芸術的表現や産業用途向けにセラミックやガラスを鮮やかな色で強化します。
- 触媒: さまざまな化学プロセスにおいて触媒または触媒前駆体として機能し、高温での分解中に酸素を放出して酸化反応を促進します。
- 電気めっき: 前駆体として一炭酸ニッケルを使用すると、さまざまな表面にニッケルを電気めっきできるため、表面の外観と耐食性が向上します。
- 電池産業: 電池技術、特にニッケルベースの電池技術では、ニッケルは正極材料に貢献し、電池システムの進歩を支えています。
- 顔料とインク: 一炭酸ニッケルは、顔料、インク、塗料の緑色のスペクトルを生成するのに不可欠です。
- 農業: 肥料中の栄養ニッケル源としての応用は植物の成長に利益をもたらし、農業でも使用されます。
- 医学: まれではありますが、研究者は、特定のニッケル化合物、特に一炭酸ニッケルが抗菌特性を示しているため、潜在的な医療応用を模索しています。
- 写真: 歴史的には、白黒写真のトナーとして役割を果たし、色合いやコントラストを豊かにしてきました。
- 繊維: 繊維業界では、染料の吸収を改善し、生地に色を注入するために一炭酸ニッケルを使用しています。
- 研究と教育: 一炭酸ニッケルの化学的特性により、化学実験室における教育用のデモンストレーション、実験、研究における重要性が確立されています。
これらの多用途用途は、セラミックスの美観の向上から電池や触媒などの先端技術での役割に至るまで、さまざまな産業における一炭酸ニッケルの重要性を示しています。
質問:
Q: 最も反応性の高い元素はどれですか?
答え: ナトリウムです。
Q: 鉄とクロム、炭素、ニッケルを混ぜて作られる有用な材料は何ですか?
答え: ステンレス製です。
Q: 炭酸ニッケルは水に溶けますか?
答え: あまり溶けません。
Q: ニッケルテトラカルボニルには炭素が何モル含まれていますか?
A: ほくろは 4 つです。
Q: 炭素鋼からニッケルメッキを除去するにはどうすればよいですか?
A: 適切な化学剥離剤または電気化学的方法を使用します。
Q: 硝酸ニッケル(II)と炭酸ナトリウムの正味のイオン反応式は?
A: Ni²⁺ + CO₃²⁻ → NiCO₃(s)。
Q: ニッケル抽出における一酸化炭素の役割は何ですか?
A: 鉱石からニッケルを抽出するための還元剤として機能します。
Q: 一炭酸ニッケルの溶解性は?
A:水への溶解度が低い。
Q: 炭素、ナトリウム、ニッケルの原子番号は?
A:炭素:6、ナトリウム:11、ニッケル:28。
Q: 炭酸アンモニウム、塩化ニッケル、水を混合するとどうなりますか?
A: 一炭酸ニッケルの沈殿が形成され、塩化アンモニウムガスが発生します。
