次亜塩素酸マグネシウム (Mg(ClO)2) は、マグネシウム、酸素、塩素から構成される化合物です。消毒剤、漂白剤、水処理薬品として使用されます。
| IUPACの名称 | 次亜塩素酸マグネシウム |
| 分子式 | Mg(ClO)2 |
| CAS番号 | 10233-03-1 |
| 同義語 | 塩素酸マグネシウム、次亜塩素酸マグネシウム塩、オキシ塩化マグネシウム、MagOCl |
| インチチ | InChI=1S/Cl2O2・Mg/c1-3-2;/q-1;+2 |
次亜塩素酸マグネシウムの性質
次亜塩素酸マグネシウム配合
次亜塩素酸マグネシウムの化学式は Mg(ClO)2 です。これは、分子ごとに 1 つのマグネシウム原子、2 つの塩素原子、2 つの酸素原子が含まれていることを意味します。わずかに塩素臭のある白色の固体で、消毒剤や水処理薬品として広く使用されています。
次亜塩素酸マグネシウムのモル質量
Mg(ClO)2 のモル質量は 127.21 g/mol です。この値は、化学式内の各元素、すなわちマグネシウム (24.31 g/mol)、塩素 (35.45 g/mol)、酸素 (15.99 g/mol) の原子量を加算することによって計算されます。 mol) にそれぞれの指数を掛けます。
次亜塩素酸マグネシウムの沸点
Mg(ClO)2 は沸点に達する前に分解するため、定義された沸点がありません。加熱すると、Mg(ClO)2 は酸素ガスを放出し、塩化マグネシウムが固体残留物として残ります。
次亜塩素酸マグネシウム 融点
Mg(ClO)2の融点は100℃です。この温度では、固体の Mg(ClO)2 結晶が液体に変わります。ただし、高温では不安定になるため、取り扱いには注意することをお勧めします。
次亜塩素酸マグネシウムの密度 g/mL
Mg(ClO)2 の密度は室温で 2.08 g/mL です。これは、1 ミリリットルの Mg(ClO)2 の質量が 2.08 グラムであることを意味します。
次亜塩素酸マグネシウムの分子量
Mg(ClO)2 の分子量は 127.21 g/mol です。これは、化合物内のすべての元素、つまりマグネシウム、塩素、酸素の原子量の合計です。
次亜塩素酸マグネシウムの構造
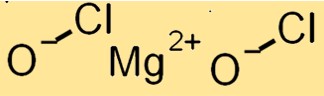
Mg(ClO)2 は単斜晶系の結晶構造を持っています。これは、イオン結合によって結合された Mg+2 カチオンと ClO-アニオンで構成されています。 ClO アニオンは、Mg+2 カチオンの周りに歪んだ四面体配置になっています。
次亜塩素酸マグネシウムの溶解度
Mg(ClO)2 は水にわずかに溶け、20℃での溶解度は 14.6 g/100 mL です。次亜塩素酸イオンの加水分解により、水中でわずかに塩基性の溶液を形成します。ただし、Mg(ClO)2 を水に溶解することはお勧めできません。有毒な塩素ガスが発生する可能性があり、人間の健康に害を及ぼす可能性があります。
| 外観 | 白色固体 |
| 比重 | 2.08 g/mL(20℃) |
| 色 | 白 |
| 匂い | 軽度塩素化 |
| モル質量 | 127.21 g/モル |
| 密度 | 2.08 g/mL(20℃) |
| 融合点 | 100℃ |
| 沸点 | 沸点に達する前に分解する |
| フラッシュドット | 適用できない |
| 水への溶解度 | わずかに溶ける(20℃で14.6 g/100 mL) |
| 溶解性 | 水にわずかに溶ける、酸に溶ける |
| 蒸気圧 | 適用できない |
| 蒸気密度 | 適用できない |
| pKa | 適用できない |
| pH | やや基本的な解決策 |
次亜塩素酸マグネシウムの安全性と危険性
Mg(ClO)2 は、正しく取り扱わないと危険です。これは、特定の化学物質と激しく反応する可能性のある強力な酸化剤です。皮膚、目、粘膜に接触すると炎症や火傷を引き起こす可能性があります。粉塵やミストを吸入すると、呼吸器疾患を引き起こす可能性があります。また、有毒な塩素ガスが発生する可能性があるため、Mg(ClO)2 を酸や他の塩素含有化合物と混合しないようにすることも重要です。 Mg(ClO)2 を取り扱うときは、手袋やゴーグルなどの保護具を着用し、混触しない化学物質から離れた涼しく乾燥した場所に保管することをお勧めします。
| ハザードシンボル | 酸化剤、有害 |
| セキュリティの説明 | 熱、火花、裸火から遠ざけてください。粉塵や霧を吸い込まないでください。手袋と保護メガネを着用してください。 |
| 国連識別番号 | 1748年 |
| HSコード | 2828.10.10 |
| 危険等級 | 5.1 (酸化剤)、6.1 (有毒) |
| 梱包グループ | Ⅱ |
| 毒性 | LD50 (経口、ラット) – 290 mg/kg; LC50 (吸入、ラット) – 2.07 mg/L/4 時間。皮膚刺激 – 軽度。目の炎症 – 重度 |
次亜塩素酸マグネシウムの合成法
Mg(ClO)2を合成するために最も一般的に使用される方法は、酸化マグネシウムと塩素ガスを反応させることです。
ある方法では、Mg(ClO)2 を生成するには、水の存在下で酸化マグネシウムを塩素ガスと混合する必要があります。発熱反応中は、望ましくない副生成物の形成を避けるために慎重に制御する必要があります。
別の方法には、水酸化マグネシウムと次亜塩素酸の反応が含まれます。 pHを維持するために、反応は通常、水酸化ナトリウム溶液中で行われます。得られたMg(ClO)2溶液は濾過により分離し、反応後に乾燥させることができる。
3 番目の方法には、炭酸マグネシウムと次亜塩素酸の反応が含まれます。この反応により、Mg(ClO)2 と二酸化炭素が生成されます。望ましくない副生成物の形成を避けるために、反応を注意深く監視する必要があります。
使用する合成方法に関係なく、Mg(ClO)2 は酸化特性と潜在的な危険性があるため、慎重に取り扱うことが重要です。
次亜塩素酸マグネシウムの用途
Mg(ClO)2 は、その酸化特性と塩素ガスを放出する能力により、いくつかの実用的な用途があります。 Mg(ClO)2 の一般的な用途をいくつか示します。
- 水処理: 有害な細菌やウイルスを殺すため、水処理工場で消毒剤として一般的に使用されます。
- 漂白剤: 繊維、紙、その他の素材の漂白剤として使用されます。
- スイミングプール: 良好な水の化学的性質を維持するために、スイミングプールの消毒剤として使用されます。
- 臭気制御: 廃棄物処理場や下水道システムの不快な臭気を制御するために使用されます。
- 酸化剤: エポキシドやケトンなどのさまざまな化学物質の製造において酸化剤として使用されます。
- 農業: 真菌性疾患や細菌性疾患と戦うための消毒剤および殺虫剤として農業で使用されます。
- 衛生: 病院、食品加工工場、その他の施設の表面や設備の消毒剤としても使用されます。
質問:
Q: 次亜塩素酸マグネシウムの式は何ですか?
A: 次亜塩素酸マグネシウムの化学式は Mg(ClO)2 です。
Q: 次亜塩素酸マグネシウムの pH レベルはどれくらいですか?
A: Mg(ClO)2 の pH レベルはその濃度に依存し、変化する可能性があります。ただし、Mg(ClO)2 溶液の pH は一般に 8 ~ 10 です。
Q: 次亜塩素酸マグネシウムの分子式は何ですか?
A: 次亜塩素酸マグネシウムの分子式は Mg(ClO)2 です。
Q: Mg(ClO)2 の名前は何ですか?
A: Mg(ClO)2 の名前は次亜塩素酸マグネシウムです。
Q: Mg(ClO)2 は酸ですか、それとも塩基ですか?
A: Mg(ClO)2 は塩基性塩であり、水溶液中では弱塩基として作用します。
Q: Mg(ClO)2 は塩ですか?
A: はい、Mg(ClO)2 は塩です。水によく溶ける白色の結晶性化合物で、金属(マグネシウム)と非金属(塩素)の両方を含んでいます。
