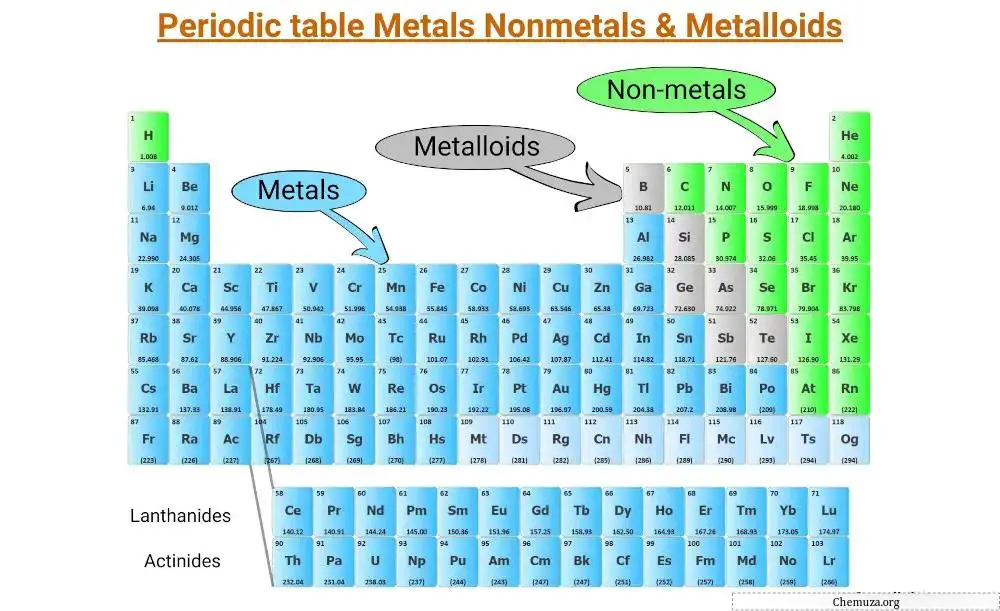
周期表のすべての元素は、3 つの主要なカテゴリに分類できます。
- 金属
- 非金属および
- 半金属
金属は一般に光沢があり、導電性があり、延性があり、周期表の左側の元素の大部分を占めます。
一方、非金属は壊れやすく(一部は気体)、導電性が低い傾向があり、主に表の右側に位置します。
半金属は金属と非金属と性質を共有しており、金属と非金属を隔てる「階段」に沿って位置しています。
周期表の金属、非金属、半金属についてさらに詳しく見てみましょう。
金属
金属は周期表の元素の大部分を占め、金属と非金属を分ける「階段」線の左側に位置します。
金属は、高い導電性、光沢、延性、展性などの特定の特性を共有しています。
金属には主に次の 5 種類があります。
- アルカリ金属は周期表の第 1 族に位置し、 水と激しく反応する柔らかく反応性の高い金属です。
- 2 族に属するアルカリ土類金属も非常に反応性が高いですが、アルカリ金属ほどではありません。それらは地殻中の鉱物の重要な成分です。
- 3 族から 11 族に位置する遷移金属は、鉄、金、銀などの最もよく知られた金属の一部です。それらは融点が高く、着色された化合物を含むことがよくあります。 [1]
- ブロック f に位置するランタニドとアクチニドは、「希土類金属」として知られています。それらは磁気特性や発光特性などのユニークな特性を持っています。 [2]
- d および f ブロックの外側にある遷移後金属には、アルミニウム、錫、鉛などの金属が含まれます。建設、輸送、エレクトロニクスなどの幅広い用途に使用されています。
全体として、金属は、建築構造物や機械から現代技術の必須コンポーネントになるまで、私たちの日常生活において多くの重要な用途を持っています。
非金属
非金属は、金属の性質を示さない化学元素のグループです。それらは、周期表の左上隅にある水素を除いて、右側に位置しています。
非金属は次のようないくつかのカテゴリに分類できます。
- 希ガス:これらは安定した不活性元素です。つまり、他の元素と容易に反応しません。希ガスには、ヘリウム、ネオン、アルゴン、クリプトン、キセノン、ラドンなどがあります。
- ハロゲン:これらは反応性の高い非金属であり、他の元素と容易に化合物を形成します。ハロゲンには、フッ素、塩素、臭素、ヨウ素、アスタチンが含まれます。
- その他の非金属:これらには、水素、炭素、窒素、酸素、リン、硫黄、セレンなどの元素が含まれます。
非金属には、金属とは区別されるいくつかの物理的および化学的特性があります。
たとえば、非金属は熱と電気の伝導性に劣る傾向があり、金属よりも融点と沸点が低くなります。
また、非金属は金属と反応すると陰イオンを形成する傾向があり、金属は陽イオンを形成する傾向があります。 [3]
半金属
半金属は、金属および非金属と特性を共有する元素です。
それらは、周期表の 2 つのカテゴリーを区切る「階段」に沿って位置しています。
半金属には次のような元素が含まれます。
半金属は、技術的および産業的用途に役立つ特性を備えている傾向があります。
たとえば、シリコンは半導体の重要な成分であり、ホウ素は強力で軽量な合金の製造に使用されます。 [4]
ヒ素は木材の防腐剤や殺虫剤などさまざまな用途に使用されてきましたが、現在では有毒物質として認識されています。 [5]
半金属の重要な特性の 1 つは、特定の条件下で電気を伝導する能力です。
たとえば、シリコンは半導体であるため、電子機器の電気の流れを制御するために使用できます。
また、半金属は一般に脆く、固体の非金属と同様に応力がかかると壊れる可能性があります。
全体として、半金属の独特の特性により、半金属はテクノロジーやエレクトロニクスなどのさまざまな用途において重要な要素となっています。
まとめ
周期表には、金属、非金属、半金属という 3 つの主要な元素カテゴリが含まれています。
金属は周期表の左側に位置し、高い導電性、光沢、延性、展性などの特性を持っています。
一方、非金属は周期表の右側に位置し、一般に壊れやすく、導電性が劣ります。
半金属は金属と非金属と特性を共有しており、2 つのカテゴリを隔てる「階段」に沿って位置しています。
