三臭化リン (PBr3) は、1 つのリン原子と 3 つの臭素原子からなる化合物です。さまざまな化学反応、特に有機化合物の合成における試薬として使用されます。
| IUPAC名 | 三臭化リン |
| 分子式 | PBr3 |
| CAS番号 | 7789-60-8 |
| 同義語 | 臭化リン(III)、臭化ブロモリン、トリブロモホスフィン |
| インチチ | InChI=1S/Br3P/c1-4(2)3 |
三臭化リンの性質
三臭化リンの配合
臭化リン(III)の式はPBr3です。 1 つのリン原子と 3 つの臭素原子から構成されます。この化合物は、リンが臭素と反応すると形成されます。式は化合物の組成を正確に表しています。
三臭化リンのモル質量
臭化リン(III)のモル質量は、構成元素の原子量を加算することで計算できます。リンの原子量は 1 モルあたり約 31.0 グラムですが、臭素の原子量は 1 モルあたり約 79.9 グラムです。リンの原子量に臭素の原子量の 3 倍を加えると、臭化リン(III) のモル質量が得られ、これは 1 モルあたり約 270.7 グラムになります。
三臭化リンの沸点
臭化リン(III)の沸点は約173℃です。これは、この温度を超える温度では、化合物が液体から気体への相変化を起こすことを意味します。沸点は、化合物を使用または精製できる条件を決定するのに役立つ重要な特性です。
三臭化リンの融点
臭化リン(III)の融点は約-41℃です。この温度は、化合物が固体状態から液体状態に変化する温度を示します。融点を知ることは、さまざまな化学プロセスで化合物を処理および操作するために非常に重要です。
三臭化リンの密度 g/mL
臭化リン(III)の密度は約2.85グラム/ミリリットル(g/mL)です。密度は、単位体積あたりの物質の質量を測定します。臭化リン(III)は比較的密度が高く、他の多くの一般的な液体よりも密度が高く、体積の割に比較的重いことを示しています。
三臭化リンの分子量
臭化リン(III)の分子量は1モルあたり約270.7グラムです。この値は、分子式 PBr3 に基づいて、化合物内のすべての原子の原子質量を加算することによって計算されます。分子量は、特定の質量中に存在する物質の量を決定するなど、さまざまな計算に役立ちます。
三臭化リンの構造
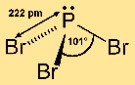
臭化リン(III)はピラミッド型の分子構造を持っています。それは、3 つの臭素原子に結合した中心のリン原子から構成されます。この配置により、分子は三角錐の形状となり、上部にリン原子、下部に臭素原子が配置されます。この構造は、化学反応における化合物の反応性と挙動を理解するために重要です。
三臭化リンの溶解度
臭化リン(III)は水に溶けにくいです。水と反応して臭化水素酸と亜リン酸を生成します。ただし、ベンゼンや四塩化炭素などの有機溶媒には可溶です。溶解度は、化合物が特定の溶媒にどの程度溶けるかを決定し、さまざまなプロセスでの用途や取り扱いに影響を与えます。
| 外観 | 無色の液体 |
| 比重 | 2.85g/ml |
| 色 | 無色 |
| 匂い | エーカー |
| モル質量 | 270.7g/モル |
| 密度 | 2.85g/ml |
| 融合点 | -41℃ |
| 沸点 | 173℃ |
| フラッシュドット | 利用不可 |
| 水への溶解度 | 反応する |
| 溶解性 | ベンゼン、四塩化炭素などの有機溶媒に可溶 |
| 蒸気圧 | 利用不可 |
| 蒸気密度 | 利用不可 |
| pKa | 利用不可 |
| pH | 利用不可 |
三臭化リンの安全性と危険性
臭化リン(III)は安全上のリスクを伴うため、慎重に取り扱う必要があります。腐食性があり、皮膚、目、呼吸器系に接触すると重度の火傷を引き起こす可能性があります。この化合物を吸入または直接摂取すると、呼吸器および胃腸への炎症を引き起こす可能性があります。水と激しく反応し、有毒なフュームを放出し、熱を発生します。臭化リン(III)を扱うときは、適切な換気と手袋やゴーグルなどの個人用保護具を使用する必要があります。さらに、潜在的な反応を避けるために、不適合物質から離して保管する必要があります。全体として、安全プロトコルを厳守し、この化合物に関連する危険性についての知識が安全な取り扱いには不可欠です。
| ハザードシンボル | 腐食性 |
| セキュリティの説明 | デポジット付きで対応します。皮膚、目、呼吸器系との接触を避けてください。適切な換気と個人用保護具を使用してください。混入しない物質から遠ざけて保管してください。 |
| 国連識別番号 | UN1805 |
| HSコード | 2812.90.90 |
| 危険等級 | 8 (腐食性) |
| 梱包グループ | Ⅱ |
| 毒性 | 吸入および経口摂取すると有毒。重度の火傷や炎症を引き起こす可能性があります。 |
三臭化リンの合成方法
臭化リン(III)を合成する一般的な方法では、反応容器は通常、制御された条件下で元素状のリンと臭素を直接混合します。反応は臭素原子がリン原子に移動して進行し、臭化リン(III) が生成します。
別の方法には、三塩化リン (PCl3)と臭化水素 (HBr)の反応が含まれます。このアプローチでは、三塩化リンが最初に臭化水素ガスと反応し、副生成物として臭化リン(III)と塩化水素ガスが生成されます。この方法は、臭化リン(III)を得る代替ルートを提供します。
「赤リン法」では、赤リンを臭素または臭化水素酸と組み合わせ、制御された条件下で反応を実行します。赤リンはリン源として機能し、臭素または臭化水素酸と反応して臭化リン(III)を生成します。
これらの合成方法は臭化リン(III) の製造に道を開きますが、それぞれに独自の利点と考慮事項があります。方法の選択は、試薬の入手可能性、望ましい収量、特定の反応条件などの要因によって異なります。これらの合成は、安全プロトコルと関係する化学物質の取り扱い手順を尊重し、設備の整った研究室で行うことが重要です。
三臭化リンの用途
臭化リン(III)は、その反応性と独特の特性により、さまざまな用途に使用されます。その用途の一部を次に示します。
- 有機合成: 化学者は、多くの有機化合物の合成における重要なステップであるアルコールを臭化アルキルに変換する有機合成の試薬として臭化リン(III) を広く使用しています。
- 製薬産業: 医薬品の製造は、さまざまな医薬品中間体および医薬品有効成分 (API) を合成するために臭化リン(III) に大きく依存しています。
- 難燃剤: メーカーは難燃剤の製造に臭化リン(III) を使用し、エレクトロニクスや繊維などの産業で使用する特定のポリマーの耐火特性を向上させます。
- 化学製造: 臭化リン(III) は、リン酸誘導体、ホスホン酸塩、リン酸塩などのリン化合物を含む他の化学物質の製造における貴重な中間体として機能します。
- 除草剤および殺虫剤: 除草剤および殺虫剤に使用される特定の有効成分の合成には、農業における雑草、害虫、病気を効果的に制御するために臭化リン(III)が使用されます。
- 実験室研究: 実験室では、研究者は通常、さまざまな実験や反応、特に臭素化や有機化合物の操作に関わる試薬として臭化リン(III) を使用します。
- 化学分析: 臭化リン(III) は化学分析技術に応用されており、臭素置換反応を通じて有機化合物中の特定の官能基の存在を測定できます。
これらの多様な用途は、有機合成、医薬品、難燃剤、化学製造、農業、実験室研究、化学分析における臭化リン(III)の重要性を浮き彫りにしています。その反応性と多用途性により、さまざまな産業や科学分野で貴重な化合物となっています。
質問:
Q: AlBr3 は臭化アルミニウムと呼ばれるのに対し、PBr3 は三臭化リンと呼ばれるのはなぜですか?
A: 金属が関与する化合物の命名規則では、通常、金属の元素名に続いて非金属の名前が使用されますが、PBr3 の場合、中心のリン原子の存在を示すためにリンが指定されます。
Q: 三臭化リンの形態を最もよく表す単語または 2 単語のフレーズはどれですか?
A: 臭化リン(III)の形状は、三角錐形として最もよく表現されます。
Q: 三臭化リン PBr3 の分子には価電子が何個ありますか?
A: 臭化リン(III) (PBr3) は 26 個の価電子を持っています。
Q: 三臭化リンはイオン性ですか、それとも共有結合性ですか?
A: 臭化リン(III) (PBr3) は共有結合性化合物です。
Q: 三臭化リンの化学式は何ですか?
A: 臭化リン(III)の化学式はPBr3です。
Q: 三臭化リン、PBr3 のルイス構造は何ですか?
A: PBr3 のルイス構造は、中心原子としてリンを示し、その周囲に 3 つの結合臭素原子が取り囲まれており、それぞれが単結合でつながっています。
Q: PBr3 は反転ですか?
A: いいえ、臭化リン(III) (PBr3) は反転を示しません。
Q: PBr3 は求電子剤ですか?
A: はい、PBr3 は特定の反応において求電子剤として作用し、電子を受け取ります。
Q: PBr3 の分子構造は何ですか?
A: PBr3 の分子構造は三角錐形です。
Q: PBr3 は極性ですか、それとも無極性ですか?
A: PBr3 は、極性のある P-Br 結合の存在によって電子密度が不均一に分布するため、極性分子です。
Q: PBr3 には 3.68 × 10^25 個の臭素原子が何モル含まれていますか?
A: モル数を決定するには、PBr3 のモル質量が必要です。次に、指定された臭素原子の数をアボガドロ数で割ります。
Q: PBr3 の正しい名前は何ですか?
A: PBr3 の正しい名前は臭化リン(III)です。
Q: PBr3 は極性がありますか?
A: はい、PBr3 は極性結合の存在と不均一な電子密度分布により極性分子です。
