三塩化ホウ素 (BCl3) は、1 つのホウ素原子に結合した 3 つの塩素原子を含む化合物です。触媒や有機合成の試薬など、さまざまな工業プロセスで使用されます。
| IUPAC名 | 三塩化ホウ素 |
| 分子式 | BCl3 |
| CAS番号 | 10294-34-5 |
| 同義語 | トリクロロボラン;塩化ホウ素(III)、トリクロロボラン、トリクロロボア |
| インチチ | InChI=1S/BCl3/c2-1(3)4 |
三塩化ホウ素の性質
三塩化ホウ素の配合
塩化ホウ素の式は BCl3 で、1 つのホウ素原子が 3 つの塩素原子に結合していることを表します。これは、この化合物の組成を説明する単純かつ単純な分子式です。
三塩化ホウ素モル質量
塩化ホウ素のモル質量は、構成元素の原子質量を加算することで計算できます。ホウ素の原子質量は 1 モルあたり約 10.81 グラム、各塩素原子の原子質量は 1 モルあたり約 35.45 グラムです。したがって、BCl3 のモル質量は 1 モルあたり約 117.17 グラムです。
三塩化ホウ素の沸点
塩化ホウ素は、他の多くの化合物に比べて沸点が比較的低いです。約摂氏-15.7度または華氏3.77度で沸騰します。これは、この温度を超える温度では、塩化ホウ素が液相から気相に変化することを意味します。
三塩化ホウ素 融点
塩化ホウ素の融点は比較的低いです。摂氏-107.5度または華氏-161.5度程度で溶けます。この温度より低い温度では、化合物は固体から液体の状態に変化します。
三塩化ホウ素の密度 g/mL
塩化ホウ素の密度は 1 ミリリットルあたり約 1.38 グラムです。この値は単位体積あたりの化合物の質量を示します。さまざまな用途における塩化ホウ素の挙動を決定し、その物理的特性を理解するのに役立ちます。
三塩化ホウ素の分子量
塩化ホウ素の分子量は、1 モルあたり約 117.17 グラムです。この値は、化合物の分子内のすべての原子の原子質量の合計を表し、特定のサンプル中の塩化ホウ素の量の決定など、さまざまな計算に役立ちます。
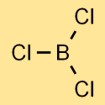
三塩化ホウ素の構造
塩化ホウ素は、三方晶系の平面分子構造を持っています。それは、三角形の形に配置された 3 つの塩素原子に結合した中心のホウ素原子から構成されます。この構造は、化合物の物理的および化学的特性に寄与します。
三塩化ホウ素の溶解度
塩化ホウ素は水への溶解度が低いです。これは難溶性であり、水溶液に限られた程度しか溶解しないことを意味します。ただし、ベンゼンや四塩化炭素などの有機溶媒にはよく溶けます。塩化ホウ素の溶解度は、さまざまな化学反応や工業プロセスにおけるその挙動に影響を与えます。
| 外観 | 無色の気体 |
| 比重 | 1,369g/mL |
| 色 | 無色 |
| 匂い | エーカー |
| モル質量 | 117.17 g/モル |
| 密度 | 1.38g/ml |
| 融合点 | -107.5℃ |
| 沸点 | -15.7℃ |
| フラッシュドット | 適用できない |
| 水への溶解度 | 反応する |
| 溶解性 | ベンゼン、四塩化炭素などの有機溶媒に可溶 |
| 蒸気圧 | 20℃で623mmHg |
| 蒸気密度 | 3.24 (空気 = 1) |
| pKa | 適用できない |
| pH | 適用できない |
三塩化ホウ素の安全性と危険性
塩化ホウ素は、安全性と危険性に関するいくつかの考慮事項を引き起こします。腐食性があり、接触すると皮膚、目、気道に重度の火傷を引き起こす可能性があります。その蒸気を吸入すると、呼吸器への刺激や肺の損傷を引き起こす可能性があります。この化合物は水との反応性も非常に高く、有毒な塩化水素ガスを発生します。塩化ホウ素は、適切な個人用保護具を使用し、適切な換気を確保して慎重に取り扱うことが不可欠です。誤って暴露した場合には、直ちに医師の診察が必要です。さらに、火災、爆発、有害ガスの放出の危険を避けるために、適切な保管および取り扱い手順に従う必要があります。
| ハザードシンボル | 腐食性(C) |
| セキュリティの説明 | 保護手袋/目の保護具/顔の保護具を着用してください。粉塵、煙霧、ガス、ミスト、蒸気、スプレーを吸入しないでください。換気の良い場所で取り扱ってください。 |
| 国連識別番号 | UN1741 |
| HSコード | 2827390000 |
| 危険等級 | 8 (腐食性物質) |
| 梱包グループ | Ⅱ |
| 毒性 | 摂取または吸入すると非常に有毒です。重度の火傷や呼吸器への刺激を引き起こす可能性があります。取り扱いには細心の注意を払ってください。 |
三塩化ホウ素の合成方法
塩化ホウ素を合成する方法の 1 つは、塩化アルミニウム (AlCl3)などの触媒の存在下で酸化ホウ素 (B2O3 ) と四塩化炭素 (CCl4) を反応させることです。 B2O3 と CCl4 は高温で反応し、副生成物として塩化ホウ素と二酸化炭素が生成されます。
もう 1 つのアプローチは、ホウ素と塩素ガスの直接反応です。制御された条件下では、ホウ素は塩素と反応し、塩化ホウ素が形成されます。この方法では、塩素ガスの危険な性質のため、慎重な取り扱いが必要です。
塩化チオニル (SOCl2) は、高温でホウ素と SOCl2 を反応させることにより塩化ホウ素の合成を可能にし、その結果、塩化ホウ素と二酸化硫黄ガスが生成されます。
これらの合成方法は、実験室と工業環境の両方で塩化ホウ素を製造するための実行可能なルートを提供します。換気の良い場所での作業や適切な保護具の使用など、合成中に適切な安全対策を確保することが重要です。このプロセスに含まれる試薬と製品には危険な性質があるため、これは重要です。
三塩化ホウ素の用途を書く
塩化ホウ素は、その独特の化学的特性と多用途性により、触媒、半導体製造、材料合成、その他のさまざまな産業で広く使用されています。
- 塩化ホウ素 (BCl3) は、さまざまな化学反応、特に有機合成における触媒として応用されています。医薬品、農薬、ファインケミカルの製造において、炭素-炭素結合および炭素-ヘテロ原子結合の形成を促進します。
- BCl3 は、難燃剤や高温コーティングに応用されるポリボラジレンなどのホウ素ベースのポリマーの合成における試薬として機能します。
- BCl3 は、その卓越した熱的および化学的安定性で知られる材料である窒化ホウ素の生成を促進し、高温用途や潤滑剤として広く使用されています。
- 半導体産業では、BCl3 をドーパントとして使用して、シリコン結晶にホウ素原子を組み込み、電気的特性を改善し、電子デバイスでの使用に適したものにしています。
- 冶金学では、BCl3 は金属の精製中に酸化物不純物を除去するフラックス剤として機能し、それによって金属の純度を向上させます。
- BCl3 は、セラミック鎧や切削工具の製造に広く使用されている軽量で強力な材料である炭化ホウ素の製造において中心的な役割を果たします。
- BCl3 は、ホウ素エステル、ボロン酸、ボランなどの多くのホウ素含有化合物の合成において重要な役割を果たします。これらの化合物は、化学研究や工業プロセスにおいて多くの用途があります。
- 石油産業では、BCl3 はガソリンのオクタン価を上げるための添加剤として使用されています。
これは、望ましい光学的および熱的特性を有するホウ素含有ガラスの製造におけるホウ素源として機能します。
質問:
Q: 三塩化ホウ素の式は何ですか?
A: 塩化ホウ素の式は BCl3 です。
Q: 三塩化ホウ素は極性がありますか?
A: はい、塩化ホウ素は、ホウ素原子上に遊離二重項が存在し、塩素原子が非対称に配置されているため、極性分子です。
Q: 三塩化ホウ素 (BCl3) におけるホウ素ハイブリダイゼーションとは何ですか?
A: BCl3 中のホウ素のハイブリダイゼーションは sp2 です。
Q: 三塩化ホウ素の分子の質量はいくらですか?
A: 塩化ホウ素 (BCl3) の分子の質量は、1 モルあたり約 117.17 グラムです。
Q: 三塩化ホウ素ハイブリダイゼーションとは何ですか?
A: 塩化ホウ素 (BCl3) におけるホウ素のハイブリダイゼーションは sp2 です。
Q: 三塩化ホウ素と水素を混合するとどうなりますか?
A: 塩化ホウ素 (BCl3) を水素 (H2) と混合すると、反応してホウ素と塩化水素ガス (HCl) が生成されます。
Q: 三塩化ホウ素はモノマーとして存在し、三塩化アルミニウムはダイマーとして存在するのはなぜですか?
A: ホウ素原子とアルミニウム原子のサイズと電子密度の違いにより、塩化ホウ素 (BCl3) は単量体として存在しますが、塩化アルミニウム (AlCl3) は配位結合を形成する能力により二量体を形成します。
Q: BCl3 はルイス酸ですか?
A: はい、BCl3 はルイス塩基から電子対を受け取ることができるため、ルイス酸です。
Q: BCl3 はイオン性ですか、それとも共有結合性ですか?
A: BCl3 は共有結合性化合物です。
Q: BCl3 は共有結合ですか?
A: はい、BCl3 はホウ素原子と塩素原子の間の共有結合で構成されています。
Q: BCl3 は気体ですか?
A: はい、BCl3 は標準温度および圧力 (STP) ガスです。
Q: BCl3 は極性分子ですか、それとも非極性分子ですか?
A: BCl3 は、ホウ素原子の周囲に塩素原子が非対称に配置されているために電子密度が不均一に分布しているため、極性分子です。
