ナトリウムエトキシドは、ナトリウムとエタノールの反応によって生成される強塩基です。有機合成では、エステル化や脱プロトン化などの反応を促進するために使用されます。
| IUPAC名 | ナトリウムエトキシド |
| 分子式 | C2H5NaO |
| CAS番号 | 141-52-6 |
| 同義語 | エタノール、ナトリウム塩;ナトリウムエトキシド;エチルナトリウム;エチレート;ナトリウムエチルアルコラート |
| インチチ | InChI=1S/C2H5O.Na/c1-2-3;/h2-3H,1H3;/q-1;+1 |
ナトリウムエトキシドの性質
ナトリウムエトキシドの配合
ナトリウムエトキシドの化学式はC2H5NaOです。 2 つの炭素原子 (C)、5 つの水素原子 (H)、1 つのナトリウム原子 (Na)、および 1 つの酸素原子 (O) で構成されています。この式はナトリウムエトキシドの分子内に存在する原子の割合を表します。
ナトリウムエトキシドのモル質量
ナトリウムエトキシドのモル質量は、その式内のすべての原子の原子質量を加算することによって計算されます。ナトリウム (Na) のモル質量は 22.99 g/mol、炭素 (C) のモル質量は 12.01 g/mol、水素 (H) のモル質量は 1.01 g/mol mol、酸素 (O) のモル質量は質量1.01 g/mol。質量16.00 g/mol。それらを加えると、ナトリウムエトキシドのモル質量は約 68.06 g/mol になります。
ナトリウムエトキシドの沸点
ナトリウムエトキシドの沸点は約 90 ~ 95°C (194 ~ 203°F) です。この温度は、標準大気圧下で加熱したときにナトリウムエトキシドが液相から気相に変化する温度を示します。
ナトリウムエトキシドの融点
ナトリウムエトキシドの融点は約 260 ~ 270°C (500 ~ 518°F) です。固体のナトリウムエトキシドが液体に変化する温度を意味します。
ナトリウムエトキシドの密度 g/mL
ナトリウムエトキシドの密度は約 0.868 g/mL です。密度は単位体積あたりの物質の質量を指し、同体積の水と比較した相対的な重さまたは軽さを決定するために使用できます。
ナトリウムエトキシドの分子量
ナトリウムエトキシドの分子量は分子量とも呼ばれ、約 68.06 g/mol です。ナトリウムエトキシドの分子に存在するすべての原子の原子質量を加算することによって計算されます。
ナトリウムエトキシドの構造
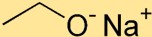
ナトリウムエトキシドは、ナトリウム原子(Na)と酸素原子(O)がイオン結合した構造をしています。 2 つの炭素 (C) 原子と 5 つの水素 (H) 原子からなるエトキシド基がナトリウム原子に結合しています。
ナトリウムエトキシドの溶解度
ナトリウムエトキシドは、エタノール (C2H5OH) やその他の有機溶媒などの極性溶媒によく溶けます。これらの溶媒に容易に溶解して無色透明の溶液を形成するため、さまざまな有機反応における試薬としての使用が容易になります。
| 外観 | 無色の固体 |
| 比重 | 0.868g/ml |
| 色 | 無色 |
| 匂い | 無臭 |
| モル質量 | 68.06g/モル |
| 密度 | 0.868g/ml |
| 融合点 | 260~270°C (500~518°F) |
| 沸点 | 90-95°C (194-203°F) |
| フラッシュドット | 適用できない |
| 水への溶解度 | 水と反応する |
| 溶解性 | エタノール (C2H5OH) およびその他の有機溶媒に可溶 |
| 蒸気圧 | 利用不可 |
| 蒸気密度 | 利用不可 |
| pKa | 利用不可 |
| pH | 塩基性(アルカリ性) |
ナトリウムエトキシドの安全性と危険性
ナトリウムエトキシドにはいくつかの安全上のリスクがあるため、取り扱いには注意が必要です。これは腐食性物質であり、皮膚、目、呼吸器系に重度の火傷を引き起こす可能性があります。直接接触は避け、手袋、ゴーグル、保護服を着用してください。水と激しく反応して可燃性の水素ガスを発生するため、湿気を避けて保管してください。ナトリウムエチラートは空気と激しく反応し、火災や爆発を引き起こす可能性があります。蒸気の蓄積を防ぐには、良好な換気が重要です。さらに、リスクを最小限に抑え安全性を確保するために、訓練を受けた職員がいる設備の整った実験室でナトリウム エトキシドを取り扱うことが重要です。
| ハザードシンボル | 腐食性 |
| セキュリティの説明 | – 重度の火傷を引き起こす<br>- 水と接触すると激しく反応する<br>- 湿気を避けて保管する<br>- 慎重に取り扱う<br>- 保護具を使用する<br>- 乾燥した場所に保管する<br>- 必ず確認してください通気性が良い |
| 国連識別番号 | UN2922 |
| HSコード | 2905.19.00 |
| 危険等級 | 8 (腐食性物質) |
| 梱包グループ | Ⅱ |
| 毒性 | 飲み込んだり吸入すると有毒 |
ナトリウムエトキシドの合成方法
ナトリウムエトキシドを合成するにはいくつかの方法があります。
ナトリウム エトキシドを合成する 1 つの方法には、金属ナトリウムとエタノールの反応が含まれます。金属ナトリウムは無水エタノールと酸化還元反応を起こし、ナトリウムエトキシドが形成されます。反応を実行するには、ナトリウム金属の小片を無水エタノールに加え、制御された条件下で混合物を還流します。
別の方法には、水酸化ナトリウム (NaOH)とエタノールの反応が含まれます。水酸化ナトリウムをエタノールに溶解し、加熱すると反応が促進されてナトリウムエトキシドが得られます。化学者は、金属ナトリウムとエタノールの直接反応を好まない場合に、この方法をよく使用します。
別の方法として、エタノールと炭酸ナトリウム (Na2CO3) を反応させてナトリウムエトキシドを調製することもできます。炭酸ナトリウムをエタノールに溶解し、加熱して混合物を撹拌します。このプロセスにより、ナトリウムエトキシドが生成されます。
これらの合成方法では、関与する化学物質の反応性のため、安全上の注意を厳守する必要があることに注意してください。可燃性物質の適切な取り扱い、保護具の使用、換気の良い場所での反応の実施は、個人の安全とナトリウム エトキシドの合成を成功させるために不可欠です。
ナトリウムエトキシドの用途
ナトリウムエトキシドは、その反応性と強塩基性によりさまざまな用途に使用されます。一般的な用途は次のとおりです。
- 有機合成: ナトリウムエトキシドは、有機合成において固体塩基として広く機能します。エステル化、縮合、脱プロトン化プロセスなどの反応を促進します。
- アルコキシド試薬: アルコキシド試薬として機能し、さまざまな有機化合物と反応してアルコキシドを形成できます。これらのアルコキシドは、多くの有機反応において重要な中間体です。
- 触媒: ナトリウム エトキシドは、いくつかの化学反応において触媒として機能します。アルコールやエステルなどの有機化合物の、対応するエーテルまたはエステル化生成物への変換を促進します。
- 脱水剤:水分子を除去することで有機化合物を脱水し、無水生成物の合成を促進します。
- 重合: ナトリウム エトキシドは、ポリエチレン テレフタレート (PET) やその他のポリエステル ポリマーの製造などの重合反応に関与します。
- 医薬品製造: 製薬産業において、エステル、エーテル、中間体などのさまざまな医薬化合物の合成に応用されています。
- バイオディーゼルの生産: エステル交換プロセスでは、ナトリウムエチラートを使用して、植物油または動物性脂肪を、再生可能で環境に優しい燃料であるバイオディーゼルに変換します。
- 実験用試薬: 研究者は通常、有機反応や実験装置の試薬としてナトリウム エトキシドを使用します。
質問:
Q: ナトリウムエトキシドベースですか?
A: はい、ナトリウムエトキシドは塩基です。
Q: ナトリウムエトキシドは強塩基ですか、それとも弱塩基ですか?
A: ナトリウムエトキシドは強塩基です。
Q: ナトリウムエトキシドを水に加えたらどうなるでしょうか?
A: ナトリウム エトキシドを水に加えると、激しく反応して水素ガスを放出し、水酸化ナトリウムが生成します。
Q: ナトリウムエトキシドは強塩基ですか、それとも弱塩基ですか?
A: ナトリウムエトキシドは強塩基です。
Q: ナトリウム エトキシドは強力な求核剤ですか?
A: はい、ナトリウム エトキシドは強力な求核剤です。
Q: 次のうち、ナトリウム エトキシドとの E2 反応が最も起こりやすいものはどれですか?
A: 第一級または第二級の脱離基を持つ化合物は、ナトリウム エトキシドとの E2 反応をより容易に受けます。
Q: ナトリウム エトキシドは強力な求核剤ですか?
A: はい、ナトリウム エトキシドは強力な求核剤です。
Q: ナトリウムエトキシドベースですか?
A: はい、ナトリウムエトキシドは塩基です。
Q: 次のうち、ナトリウム エトキシド (NaOCH2CH3) との E2 反応が最も起こりやすいのはどれですか?
A: 第一級または第二級の脱離基を持つ化合物は、ナトリウム エトキシドとの E2 反応をより容易に受けます。
Q: ナトリウムエトキシドは可燃性ですか?
A: ナトリウムエトキシド自体は可燃性ではありませんが、水と激しく反応して可燃性の水素ガスを発生します。
Q: エタノールと組み合わせると、ナトリウムエトキシドと水素が生成されますか?
A: 金属ナトリウムとエタノールを組み合わせると、ナトリウムエトキシドと水素ガスが生成されます。
Q: ナトリウムエトキシドを水に加えたらどうなるでしょうか?
A: ナトリウム エトキシドを水に加えると、激しく反応して水素ガスを放出し、水酸化ナトリウムが生成します。
