ナトリウムアミド (NaNH2) は化合物です。ナトリウム原子と窒素原子で構成されています。さまざまな化学反応において強塩基として使用されます。
| IUPAC名 | アミドナトリウム |
| 分子式 | NaNH2 |
| CAS番号 | 7782-92-5 |
| 同義語 | ソーダミド、アザニドナトリウム、ナトリウムアミド、窒化ナトリウム |
| インチチ | InChI=1S/NaN2/c2-1-3/q-1 |
ナトリウムアミドの性質
ナトリウムアミドの式
ナトリウムアミドの式はNaNH2です。ナトリウム原子(Na)、水素原子(H)、窒素原子(N)から構成されています。この化学式はナトリウムアミドの組成を分子レベルで表しています。
アミドナトリウムのモル質量
アザニドナトリウムのモル質量は、その構成元素の原子質量を加算することによって計算されます。ナトリウムの原子量は 22.99 グラム/モル (g/mol)、窒素の原子量は 14.01 g/mol です。これらの値を加算すると、アザニドナトリウムのモル質量は約 39 g/mol であることがわかります。
ナトリウムアミドの沸点
アザニドナトリウムの沸点は、液体から気体に変化する温度です。アザニドナトリウムは、摂氏約 850 度 (°C) と比較的高い沸点を持っています。この温度では、アザニドナトリウム分子を保持する分子間力が克服され、液体状態から気体状態への変換が起こります。
ナトリウムアミド 融点
アザニドナトリウムの融点は、固体から液体に変化する温度です。アザニドナトリウムの融点は約 210 ℃ (°C) と比較的低いです。この温度では、固体のアザニドナトリウムの結晶格子構造が壊れ、粒子が自由に移動できるようになり、液体が形成されます。
ナトリウムアミドの密度 g/mL
アザニドナトリウムの密度は、単位体積あたりの質量の尺度です。アザニドナトリウムの密度は約 1.39 グラム/ミリリットル (g/mL) です。この値は、アザニドナトリウムが比較的密度の高い物質であることを示しています。
ナトリウムアミドの分子量
アザニドナトリウムの分子量は、その化学式に含まれるすべての原子の原子量の合計です。アザニドナトリウムの分子量は約 39 グラム/モル (g/mol) です。
ナトリウムアミドの構造
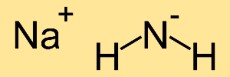
アザニドナトリウムの構造は、2 つの窒素 (N) 原子に結合した 1 つのナトリウム (Na) 原子で構成されています。窒素原子はナトリウム原子を中心に直線状に配置され、直線状の分子構造になります。
ナトリウムアミドの溶解度
アザニドナトリウムは水に溶けにくいです。水と反応して水酸化ナトリウム (NaOH) とアンモニア (NH3) を生成します。ただし、液体アンモニアや液体アルコールなどの一部の有機溶媒には可溶です。アザニドナトリウムはこれらの溶媒に溶解するため、さまざまな化学反応に使用できます。
| 外観 | 白色固体 |
| 比重 | 1.39g/ml |
| 色 | 白 |
| 匂い | アンモニアに似たもの |
| モル質量 | 39g/モル |
| 密度 | 1.39g/ml |
| 融合点 | 210℃ |
| 沸点 | 850℃ |
| フラッシュドット | 適用できない |
| 水への溶解度 | 反応する |
| 溶解性 | 液体アンモニアや液体アルコールなどの有機溶媒に可溶 |
| 蒸気圧 | 適用できない |
| 蒸気密度 | 適用できない |
| pKa | 適用できない |
| pH | アルカリ性(7以上) |
ナトリウムアミドの安全性と危険性
アザニドナトリウムは、考慮する必要がある特定の安全上のリスクと危険性をもたらします。水と激しく反応し、有毒なアンモニアガスと腐食性の水酸化ナトリウムを放出します。したがって、湿気や水に触れないよう細心の注意を払って取り扱う必要があります。アザニドナトリウムは強力な塩基でもあるため、皮膚や目に接触すると重度の火傷や目の損傷を引き起こす可能性があります。その粉塵や蒸気を吸入すると、呼吸器系を刺激する可能性があります。アザニドナトリウムを扱うときは、手袋、ゴーグル、呼吸用保護具などの適切な保護具を着用することをお勧めします。適切な換気と、不適合物質から遠ざけて保管することは、重要な安全対策です。
| ハザードシンボル | 腐食性、有害、有毒 |
| セキュリティの説明 | 取り扱いには細心の注意を払ってください。水/湿気との接触を避けてください。保護具を着用してください。適切な換気と保管が必要です。 |
| 国連識別番号 | 国連 1410 |
| HSコード | 28500020 |
| 危険等級 | 4.3 (濡れると危険)、6.1 (有毒)、8 (腐食性) |
| 梱包グループ | Ⅱ |
| 毒性 | 経口摂取、吸入、または皮膚/眼との接触により有毒 |
ナトリウムアミドの合成方法
アザニドナトリウムを合成するにはさまざまな方法があります。
一般的な方法は、金属ナトリウムとアンモニアガス (NH3)の反応です。このプロセスでは、制御された条件下で金属ナトリウムがアンモニアガスと反応して、アザニドナトリウムが生成されます。反応は通常、適切な安全対策を備えた反応容器内で行われます。
別の方法には、水素化ナトリウム (NaH) とアンモニアガスの反応が含まれます。固体化合物である水素化ナトリウムはアンモニアガスと反応して、アザニドナトリウムと水素ガスを生成します。望ましくない副反応を避けるために、この反応を実行するには不活性雰囲気がよく使用されます。
さらに、金属ナトリウムと液体アンモニアの反応により、アザニドナトリウムの調製が可能になります。この方法では、ナトリウム金属を液体アンモニアに溶解し、アザニドナトリウムと水素ガスが生成されます。
アザニドナトリウムを合成するには、アジ化ナトリウム (NaN3)を水酸化ナトリウム (NaOH) と反応させます。これら 2 つの化合物の反応により、アザニドナトリウムが生成され、窒素ガスが発生します。
アザニドナトリウムには反応性と危険性があるため、これらの合成方法には専門知識と適切な安全上の注意が必要であることに注意してください。
ナトリウムアミドの用途
アザニドナトリウムは、そのユニークな特性によりさまざまな分野で応用されています。その用途の一部を次に示します。
- 有機化学反応における強塩基: アザニドナトリウムは弱酸を脱プロトン化し、さまざまな有機化合物の合成を促進します。
- 反応における窒素源: アザニドナトリウムは有機分子に窒素原子を導入し、医薬品、染料、ポリマーの合成において重要な役割を果たします。
- 脱ハロゲン化水素: アザニドナトリウムは、脱ハロゲン化水素反応において有機化合物からハロゲン化水素を除去します。このプロセスにより、アルケン、アルキン、その他の不飽和化合物の調製が容易になります。
- 開環反応: アザニドナトリウムは、ガブリエル合成などの環状化合物の開環反応に関与し、環状アミンを第一級アミンに変換します。
- 脱硫: アザニドナトリウムは有機化合物から硫黄原子を除去し、脱硫反応を可能にします。これは、硫黄を含まない燃料の製造や、硫黄含有化合物の環境への影響の軽減に役立ちます。
- 水素貯蔵: 研究者らは、水素貯蔵システムにおけるアザニドナトリウムの使用の可能性を調査しました。水素ガスと反応して水素化ナトリウムを形成し、加熱すると水素を放出します。
- 触媒担体: アザニドナトリウムは触媒担体として機能し、特定の触媒反応の性能を向上させます。さまざまな化学変化における触媒の安定性を確保し、効率を向上させます。
全体として、アザニドナトリウムはその多用途な特性により、有機合成、窒素化学、その他の産業用途において価値のある化合物となっています。
質問:
Q: NaNH2 は何をするのですか?
A: NaNH2 は、弱酸を脱プロトン化し、さまざまな変換を促進するために有機化学反応で一般的に使用される強塩基です。
Q:NaNH2とは何ですか?
A: NaNH2 はナトリウムアミドであり、ナトリウム (Na) イオンとアザニド (NH2) イオンからなる化合物で、有機合成において試薬および強塩基としてよく使用されます。
Q: 過剰な NaNH2 は何に使用されますか?
A: 過剰な NaNH2 は、反応中の酸性水素原子のさらなる脱プロトン化を引き起こす可能性があり、それによって脱プロトン化の程度が増加し、反応の結果が変化する可能性があります。
Q: NaNH2 はアルケンに何をしますか?
A: NaNH2 はアルケンから水素原子を抽出することができ、その結果、アルカンとナトリウム アルコキシド化合物が形成されます。
Q: NaNH2 はブロモベンゼンに何をしますか?
A: NaNH2 は求核置換反応を通じてブロモベンゼンの臭素原子を置換することができ、その結果ナトリウム フェニルアミンが形成されます。
Q: NaNH2 は強塩基ですか?
A: はい、NaNH2 はプロトンを受け取り、アミド イオンの存在により弱酸を脱プロトン化できる強塩基です。
Q: NaNH2/NH3 混合物に H2O を加えるとどのような反応が起こりますか?
A: NaNH2/NH3 混合物に H2O を加えると、水と強塩基 NaNH2 の反応によりアンモニアガス (NH3) と水酸化ナトリウム (NaOH) が生成されます。
Q: この反応にはどの中間体が関与していますか: NaNH2 + 液体 NH3?
A: NaNH2 と液体 NH3 の反応に関与する中間体は、ナトリウムからアンモニアへの電子の供与によって形成される溶媒和電子です。
Q: NaNH2 は優れた求核剤ですか?
A: はい、NaNH2 は電子対を供与し、求核置換反応に参加する能力があるため、良好な求核剤として機能します。
Q: NaNH2 はイオン性ですか、それとも共有結合性ですか?
A: NaNH2 は、正に帯電したナトリウムイオン (Na+) と負に帯電したアミドイオン (NH2-) から構成されるイオン性化合物です。
Q: 2-ヘキシンはナトリウムアミドと反応しますか?
A: はい、2-ヘキシンはナトリウムアミドと反応し、ナトリウムアセチリドと対応するアルキン化合物が生成する可能性があります。
Q: ナトリウムアミドとナトリウムフェノキサートの中で最も強い塩基はどれですか?
A: アザニドナトリウムは、フェノックスイオン (C6H5O-) と比較してアミドイオン (NH2-) の塩基性が高いため、フェノキサートナトリウムよりも強い塩基です。
