チオ硫酸カルシウム (CaO3S2) は、カルシウム、酸素、硫黄から構成される化合物です。医療業界や農業業界で肥料や特定の病状の治療法として一般的に使用されています。
| IUPAC名 | チオ硫酸カルシウム |
| 分子式 | CaO3S2 |
| CAS番号 | 10124-41-1 |
| 同義語 | 次亜硫酸カルシウム;チオ硫酸カルシウム;硫水カルシウム;チオスルホン酸カルシウム |
| インチチ | InChI=1S/Ca.H2O3S2/c;1-4(2)3/h;(H2,1,2,3)/q+2;/p-2 |
チオ硫酸カルシウムの性質
チオ硫酸カルシウムの配合
チオ硫酸カルシウムの化学式は CaS2O3 です。分子内の原子の種類と数を示します。この式を使用して、化合物のモル質量およびその他の特性を決定できます。
チオ硫酸カルシウムのモル質量
CaO3S2 のモル質量は 152.18 g/mol です。 1 つのカルシウム原子、3 つの酸素原子、2 つの硫黄原子で構成されています。モル質量は、化学計算で使用される重要な特性です。たとえば、特定の反応を起こすためにどれだけの物質が必要かを決定します。
チオ硫酸カルシウムの沸点
CaO3S2 は沸騰する前に分解するため、明確な沸点がありません。 75℃付近で分解が始まり、二酸化硫黄を放出します。物質の沸点は、特定の圧力下で液体から気体に変化する温度です。
チオ硫酸カルシウム 融点
CaO3S2の融点は155℃です。この温度では、固体化合物は固体から液体に変化します。融点は、物質を識別および分類するために使用される重要な特性です。
チオ硫酸カルシウムの密度 g/mL
CaO3S2 の密度は 2.67 g/mL です。密度は単位体積あたりの質量です。物質の密度を使用して、その物質が水などの別の物質に浮くか沈むかを判断できます。
チオ硫酸カルシウムの分子量
CaO3S2 の分子量は 152.18 g/mol です。これは、分子内のすべての原子の原子量の合計です。分子量は、モル濃度や濃度など、物質のさまざまな特性を計算するために使用されます。
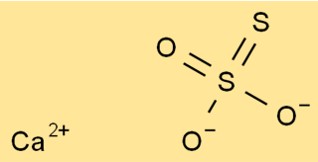
チオ硫酸カルシウムの構造
CaO3S2 の構造は、1 つの Ca2+ イオンと 1 つの S2O32- イオンで構成されます。チオ硫酸イオンは中心に硫黄原子があり、それに 4 つの酸素原子が結合しています。酸素原子のうち 2 つは二重結合、2 つは単結合です。
チオ硫酸カルシウムの溶解度
CaO3S2 は水にわずかに溶け、室温での溶解度は約 16 g/L です。冷水よりも熱水の方が溶けやすいです。溶解度は、特定の温度および圧力で特定の溶媒に溶解できる物質の最大量です。
| 外観 | 白色の結晶固体 |
| 比重 | 2.67g/ml |
| 色 | 白 |
| 匂い | 無臭 |
| モル質量 | 152.18 g/モル |
| 密度 | 2.67g/ml |
| 融合点 | 155℃ |
| 沸点 | 沸騰する前に分解してしまう |
| フラッシュドット | 適用できない |
| 水への溶解度 | 室温で16 g/L |
| 溶解性 | 水にわずかに溶ける |
| 蒸気圧 | 適用できない |
| 蒸気密度 | 適用できない |
| pKa | 7.2 (チオ硫酸の解離) |
| pH | 6.0~8.5(1%水溶液) |
チオ硫酸カルシウムの安全性と危険性
CaO3S2 は一般に、適切に取り扱われ、使用されれば安全であると考えられています。ただし、吸入すると皮膚や目の炎症、呼吸困難を引き起こす可能性があります。また、摂取すると胃腸炎を引き起こす可能性があります。この化合物を取り扱うときは、手袋や保護眼鏡などの適切な個人用保護具を着用することが重要です。皮膚に付着した場合は、多量の水で洗い流す必要があります。目に入った場合は、少なくとも 15 分間水で洗い流してください。飲み込んだり吸入した場合は、直ちに医師の診察を受けてください。 CaO3S2 は、不適合物質から離れた、涼しく乾燥した換気の良い場所に保管する必要があります。
| ハザードシンボル | シー(イライラする) |
| セキュリティの説明 | 粉塵、煙霧、ガス、ミスト、蒸気、スプレーを吸入しないようにしてください。保護手袋/保護服/保護眼鏡/保護面を着用してください。 |
| 国連識別番号 | 規制されていません |
| HSコード | 2832.10.00 |
| 危険等級 | 6.1 (有毒) |
| 梱包グループ | Ⅲ |
| 毒性 | LD50 (経口、ラット) 1064 mg/kg; LC50 (吸入、ラット) >2,000 mg/m3 |
チオ硫酸カルシウムの合成方法
CaO3S2を合成するにはさまざまな方法が存在します。
1 つの方法では、水中で水酸化カルシウム (Ca(OH)2) をNa2S2O3と反応させて、CaO3S2 と水酸化ナトリウム (NaOH) を生成します。
別の方法は、水中で硫酸カルシウム (CaSO4)を亜硫酸ナトリウム (Na2SO3) および硫黄 (S) と反応させて、CaO3S2 および硫酸ナトリウム (Na2SO4) を生成する方法です。
CaO3S2は、水中で硫黄(S)と酸素(O2)を酸化カルシウム(CaO)または炭酸カルシウム(CaCO3)と反応させることで得られます。この方法では、副産物として CaO3S2、硫酸カルシウム (CaSO4) 、二酸化炭素 (CO2) が生成されます。
CaO3S2 を合成するには、 Na2S2O3 を水中で塩化カルシウム (CaCl2) と反応させます。この方法では、副生成物として CaO3S2 と塩化ナトリウム (NaCl) が生成されます。
別の方法では、水中で水酸化カルシウム (Ca(OH)2)を二酸化硫黄 (SO2) および酸素 (O2) と反応させ、副生成物として CaO3S2 と亜硫酸カルシウム (CaSO3 ) を生成します。
チオ硫酸カルシウムの用途
CaO3S2 は、さまざまな業界でさまざまな用途に使用されます。その用途には次のようなものがあります。
- 農業 – 植物にカルシウムと硫黄を供給する肥料として使用されます。
- 写真 – 写真処理において、プリントやネガから余分なハロゲン化銀を除去するための定着剤として使用されます。
- 水処理 – 水から塩素を除去し、廃水中の塩素を中和するために使用されます。
- 薬 – シアン化物と反応して毒性の低いチオシアン酸塩を生成するため、シアン化物中毒の治療法として使用されます。
- 産業 – 紙パルプ製造、石油精製、繊維加工などのさまざまな産業プロセスで使用されます。
- 食品産業 – 細菌の増殖を防ぎ、食品の鮮度を維持するための食品保存料として使用されます。
- 動物の健康 – 動物にカルシウムと硫黄を供給するための栄養補助食品として使用されます。
- 化粧品 – ヘアコンディショニング剤および皮膚保湿剤として化粧品に使用されます。
質問:
Q: チオ硫酸カルシウムとチオ硫酸ストロンチウムではどちらが水に溶けやすいですか?
A: CaO3S2 はチオ硫酸ストロンチウムよりも水に溶けやすいです。
Q: チオ硫酸ストロンチウムとチオ硫酸カルシウムではどちらが水に溶けやすいと思いますか?
A: CaO3S2 はチオ硫酸ストロンチウムよりも水に溶けやすいはずです。
Q: チオ硫酸カルシウムの脱塩素原子は何で構成されますか?
A: CaO3S2 脱塩素原子は、1 つのカルシウム原子、3 つの酸素原子、2 つの硫黄原子、および 2 つのチオ硫酸イオンで構成されます。
Q: チオ硫酸カルシウムはどうやって識別するのですか?
A: CaO3S2 は、その物理的および化学的特性のほか、赤外分光法や X 線回折などのさまざまな分析手法によって同定できます。
Q: チオ硫酸カルシウムの数字は何を意味しますか?
A: CaO3S2 の数字は、化合物中に存在する各元素の原子の数を指します。たとえば、CaO3S2 は、カルシウム原子が 1 つ、酸素原子が 3 つ、硫黄原子が 2 つあることを示します。
Q: チオ硫酸カルシウム水処理とは何ですか?
A: CaO3S2 は、水から塩素を除去し、廃水中の塩素を中和するために水処理に使用されます。
Q: チオ硫酸カルシウムの錠剤はありますか?
A: はい、CaO3S2 錠剤は動物にカルシウムと硫黄を供給する栄養補助食品として入手できます。
