硫酸銀 (Ag2SO4) は、写真や分析化学で使用される白色の固体です。水に溶け、加熱すると酸化銀と三酸化硫黄に分解します。
| IUPAC名 | 硫酸銀 |
| 分子式 | Ag2SO4 |
| CAS番号 | 10294-26-5 |
| 同義語 | 硫酸銀、硫酸二銀、硫酸銀、一硫酸二銀 |
| インチチ | InChI=1S/2Ag.H2O4S/c;;1-5(2,3)4/h;;(H2,1,2,3,4)/q2*+1;/p-2 |
硫酸銀の性質
硫酸銀の配合
二二硫酸塩の化学式は Ag2SO4 です。これは、1 つの硫黄 (S) 原子と 4 つの酸素 (O) 原子に結合した 2 つの銀 (Ag) 原子で構成されています。この式は二二硫酸塩の分子内の原子の比率を表します。
硫酸銀のモル質量
硫酸二銀のモル質量は、その構成元素の原子質量を加算することによって計算されます。銀の原子量は 107.87 グラム/モル (g/mol)、硫黄の原子量は 32.07 g/mol、酸素の原子量は 16.00 g/mol です。それらを合計すると、二二硫酸塩のモル質量は約 311.81 g/mol になります。
硫酸銀の沸点
ダイアジェント硫酸塩は沸点に達する前に分解するため、明確な沸点を持ちません。加熱すると熱分解が起こり、酸化銀(Ag2O)と三酸化硫黄(SO3)に分解されます。したがって、二硫酸塩の沸点は適用されません。
硫酸銀 融点
二二硫酸塩の融点は約摂氏 652 度 (華氏 1,206 度) です。この温度では、二硫酸塩は固体状態から溶融液体状態に変化します。融点は二二硫酸塩サンプルの純度に応じてわずかに異なる可能性があることに注意することが重要です。
硫酸銀の密度 g/mL
二二硫酸塩の密度は約 5.45 グラム/ミリリットル (g/mL) です。この値は単位体積あたりの二硫酸塩の質量を示します。一般に物質の密度は温度に依存するため、二硫酸塩の密度を測定する際には条件を考慮することが重要です。
硫酸銀の分子量
二二硫酸塩の分子量は、式の化学量論を考慮して、その構成元素の原子量を加算することによって計算されます。硫酸二銀 (Ag2SO4) の場合、分子量は約 311.81 グラム/モル (g/mol) です。
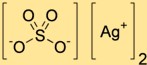
硫酸銀の構造
硫酸二銀は銀陽イオン(Ag+)と硫酸陰イオン(SO4^2-)からなる結晶構造を持っています。銀カチオンは硫酸アニオンの酸素原子に囲まれ、三次元ネットワークを形成しています。
硫酸銀の溶解度
ダイアジェント硫酸塩は水に溶けにくいです。溶解度は限られており、室温で水 100 ミリリットルに約 0.8 グラムが溶解します。溶解度は、温度や溶液中の他の溶質の存在などの要因によって影響を受ける可能性があります。
| 外観 | 白色固体 |
| 比重 | 該当なし |
| 色 | 白 |
| 匂い | 無臭 |
| モル質量 | 311.81 g/モル |
| 密度 | 5.45g/ml |
| 融合点 | 652°C (1206°F) |
| 沸点 | 分解された |
| フラッシュドット | 該当なし |
| 水への溶解度 | 難溶性 |
| 溶解性 | 水に溶解します。酸、アルコール、アセトン、エーテル、酢酸塩、アミド |
| 蒸気圧 | 該当なし |
| 蒸気密度 | 該当なし |
| pKa | 該当なし |
| pH | 該当なし |
硫酸銀の安全性と危険性
ダイアジェント硫酸塩には安全上のリスクがあり、取り扱いには注意が必要です。吸入、摂取、または皮膚や目との接触を避けることが重要です。二二硫酸塩を取り扱うときは、手袋、ゴーグル、白衣などの適切な個人用保護具を着用することをお勧めします。誤って触れた場合は、患部を水でよく洗い流してください。ダイアジェント硫酸塩は皮膚や目に炎症を引き起こす可能性があり、長期間または繰り返し暴露すると感作を引き起こす可能性があります。また、吸入の危険性を最小限に抑えるために、二二硫酸塩は換気の良い場所で取り扱う必要があります。安全性を確保するために、適切な保管、ラベル貼付、廃棄手順に従う必要があります。
| ハザードシンボル | 記号なし |
| セキュリティの説明 | 吸入、摂取、皮膚や目との接触を避けてください。 PPEを着用してください。換気の良い場所で取り扱ってください。適切な保管、ラベル貼付、廃棄。 |
| 国連識別番号 | 該当なし |
| HSコード | 28429090 |
| 危険等級 | 該当なし |
| 梱包グループ | 該当なし |
| 毒性 | 皮膚や目に刺激性があります。長期間/繰り返し暴露すると、感作を引き起こす可能性があります。 |
硫酸銀の合成方法
二放射性硫酸塩を合成するにはいくつかの方法があります。
一般的な方法には、硝酸銀 (AgNO3)と硫酸 (H2SO4)の反応が含まれます。研究室で、科学者はかき混ぜながら硝酸銀を硫酸溶液にゆっくりと加えます。その結果、二二硫酸塩と呼ばれる白い沈殿物が形成されます。沈殿物を収集し、洗浄し、乾燥させて純粋な二二硫酸塩を得る。
科学者はまた、酸化銀(Ag2O)を硫酸に加え、混合物を撹拌しながら加熱することによって硫酸銀を入手します。このプロセスでは、沈殿として二二硫酸塩が生成され、これを濾過、洗浄、乾燥して最終製品が得られます。
さらに、科学者は塩化銀(AgCl)と濃硫酸の混合物を加熱することで硫酸銀を得ることができます。塩化銀を硫酸に加え、混合物に熱を加えます。この反応により、硫酸銀が沈殿物として形成され、これを収集し、洗浄し、乾燥させることができる。
これらの合成方法は、適切な保護具の使用や換気の良い場所での作業など、適切な安全対策を講じて実行する必要があることに注意することが重要です。
硫酸銀の用途
硫酸二銀は、その独特の特性により、さまざまな分野でいくつかの用途があります。一般的なアプリケーションのいくつかを次に示します。
- 写真: 白黒写真では、写真家は感光性乳剤の成分として二硫酸塩を使用し、光と反応して画像をキャプチャおよび現像します。
- 分析化学: さまざまな分析方法では、沈殿反応を通じて塩化物イオンや臭化物イオンなどのハロゲン化物を検出および定量するための試薬として硫酸銀を使用します。
- 電気メッキ: 電気メッキプロセスでは、二放射性硫酸塩を使用して導電性表面に銀の層を堆積させ、宝飾品、電子機器、その他の物体に装飾または保護コーティングを作成します。
- 抗菌剤: 二ジアジェント硫酸塩は、その抗菌特性により、包帯、軟膏、医療機器の配合に応用されています。感染症を予防し、治癒を促進します。
- 電池産業: 電池産業では、電子機器や医療機器で普及している銀亜鉛電池や銀カドミウム電池を製造するための電極材料の重要な成分として使用されています。
- 実験室試薬: 硫酸二銀は、他の銀化合物の合成や有機化学反応など、さまざまな実験室での試薬として使用されます。
- ガラス製造: ガラス製造において、銀メッキミラーや導電性窓コーティングなどの特殊ガラスの製造において重要な役割を果たします。メーカーは、これらの望ましい特性を達成するために、二放射性硫酸塩の薄い層を塗布します。
- 触媒: 硫酸二銀は、酸化反応や重合プロセスなどの特定の化学反応において触媒として機能します。
質問:
Q: 硝酸銀と硫酸カリウムの置換反応では他に何が生成されますか?
A: AgNO3 と K2SO4 の置換反応では、硝酸カリウム (KNO3) と二二硫酸塩 (Ag2SO4) が生成します。
Q: 固体の硫酸銀を溶液に追加すると溶解しますか?
A: はい、追加の固体硫酸二銀は水に溶けにくいため、溶液に溶解します。
Q: 硝酸銀+硫酸ナトリウムの場合、沈殿は起こりますか?
A: はい、AgNO3 が硫酸ナトリウムと反応すると沈殿が発生し、固体の Ag2SO4 沈殿物が形成されます。
Q: 硫酸銀中の銀の割合は何パーセントですか?
A: 二二硫酸塩中の Ag の割合は約 63.48% です。
Q: 硫酸銀は可溶性ですか、不溶性ですか?
A: ダイアジェント硫酸塩は水に溶けにくいです。
Q: 硫酸銀の化学式はどうやって調べますか?
A: 硫酸二銀の化学式は Ag2SO4 で、Ag+ カチオンと SO4-2 アニオンの価数に基づいて決定できます。
Q: Ag2SO4 の色は何ですか?
A: 硫酸二銀 (Ag2SO4) は白色の固体です。
Q: 5.49 g が 1.00 L の水に溶ける場合、Ag2SO4 の Ksp 値はいくらですか?
A: Ag2SO4 の溶解度積定数 (Ksp) 値は、提供された情報を使用して計算できますが、これには水中での Ag2SO4 の解離に関する追加データが必要です。
Q: Ag2SO4 のモル質量はどれくらいですか?
A: Ag2SO4 のモル質量は約 311.81 g/mol です。
Q: 2.7gを100mlの水に溶解すると、固体のAg2SO4が形成されますか?
A: はい、100 ml の水に対する二二硫酸塩の溶解限度を超えると、固体の Ag2SO4 が生成する可能性があります。
