上の画像はもう見たはずですよね?
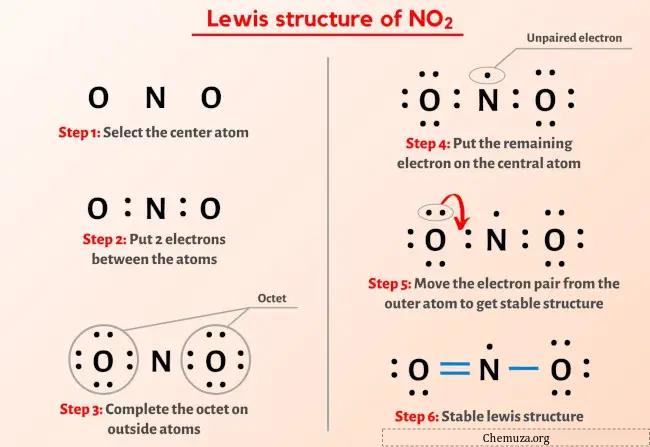
上の画像について簡単に説明します。
NO2 のルイス構造は、中心に窒素 (N) 原子があり、その周りを 2 つの酸素 (O) 原子が取り囲んでいます。窒素 (N) 原子と各酸素 (O) 原子の間には、二重結合が 1 つと単結合が 1 つあります。窒素 (N) 原子上には 1 つの非共有電子対、二重結合酸素 (O) 原子上には 2 つの非共有電子対、単結合酸素 (O) 原子上には 3 つの非共有電子対があります。 。
上の NO2 (二酸化窒素) のルイス構造の図を見て何も理解できなかった場合は、このまま読んでください。NO2 (二酸化窒素) の構造を描く方法について、段階的に詳細に説明します。 NO2のルイス。
それでは、NO2 のルイス構造を描く手順に進みましょう。
NO2 ルイス構造を描く手順
ステップ 1: NO2 分子内の価電子の総数を見つける
NO2 (二酸化窒素) 分子内の価電子の総数を求めるには、まず窒素原子と炭素原子に存在する価電子を知る必要があります。酸素。
(価電子は、原子の最も外側の軌道に存在する電子です。)
ここでは、周期表を使って窒素と酸素の価電子を簡単に求める方法を説明します。
NO2 分子内の総価電子
→ 窒素原子によって与えられる価電子:
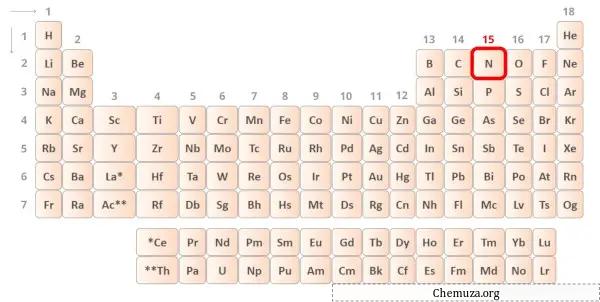
窒素は、周期表の第 15 族の元素です。[1]したがって、窒素中に存在する価電子は5です。

上の画像に示すように、窒素原子には 5 つの価電子が存在することがわかります。
→ 酸素原子によって与えられる価電子:

酸素は、周期表の第 16 族の元素です。 [2]したがって、酸素に存在する価電子は6です。
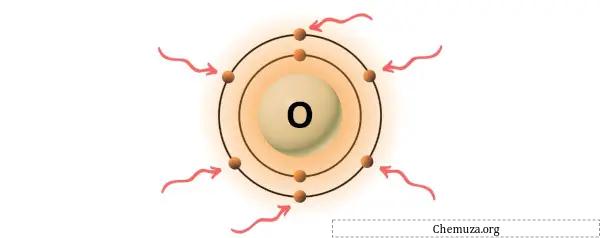
上の画像に示すように、酸素原子には 6 つの価電子が存在することがわかります。
それで、
NO2 分子内の総価電子= 1 つの窒素原子によって供与される価電子 + 2 つの酸素原子によって供与される価電子 = 5 + 6(2) = 17 。
ステップ 2: 中心原子を選択する
中心原子を選択するには、最も電気陰性度の低い原子が中心に残ることを覚えておく必要があります。
ここで、指定された分子は NO2 (二酸化窒素) であり、窒素 (N) 原子と酸素 (O) 原子が含まれています。
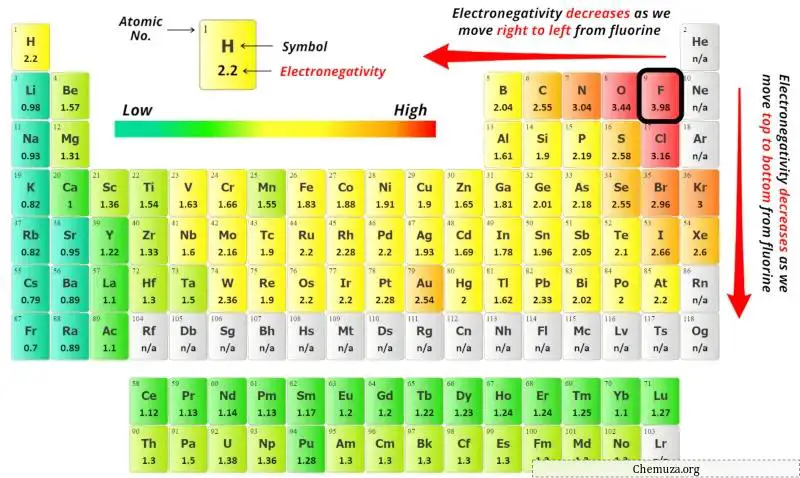
上記の周期表で窒素(N)原子と酸素(O)原子の電気陰性度の値を確認できます。
窒素(N)と酸素(O)の電気陰性度の値を比較すると、窒素原子の方が電気陰性度が低くなります。
ここで、窒素 (N) 原子が中心原子であり、酸素 (O) 原子が外側の原子です。

ステップ 3: 各原子の間に電子対を配置して各原子を接続する
ここで、NO2 分子では、窒素 (N) 原子と酸素 (O) 原子の間に電子対を配置する必要があります。
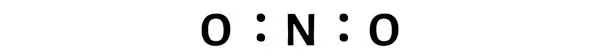
これは、NO2 分子内で窒素 (N) と酸素 (O) が化学結合していることを示しています。
ステップ 4: 外部原子を安定化します。残りの価電子対を中心原子に配置します。
このステップでは、外部原子の安定性をチェックする必要があります。
ここの NO2 分子のスケッチでは、外側の原子が酸素原子であることがわかります。
これらの外部酸素原子はオクテットを形成するため、安定しています。

さらに、ステップ 1 では、NO2 分子内に存在する価電子の総数を計算しました。
NO2 分子には合計17 個の価電子があり、上の図ではそのうち16 個だけが使用されています。
したがって、残っている電子の数 = 17 – 16 = 1 となります。
この1 つの電子を、NO2 分子の上の図の中央の窒素原子に配置する必要があります。
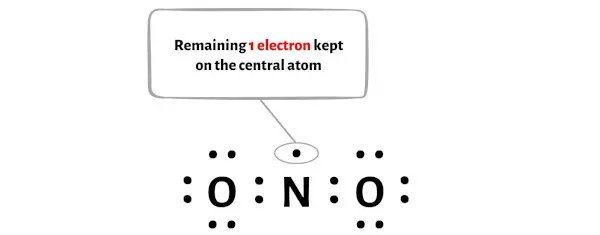
次のステップに進みましょう。
ステップ 5: 中心原子のオクテットを確認します。オクテットがない場合は、非共有電子対を移動して二重結合または三重結合を形成します。
このステップでは、中心の窒素 (N) 原子が安定であるかどうかを確認する必要があります。
中心の窒素 (N) 原子の安定性を確認するには、それがオクテットを形成しているかどうかを確認する必要があります。
残念ながら、ここでは窒素原子はオクテットを形成しません。窒素は電子が 5 個しかなく、不安定です。
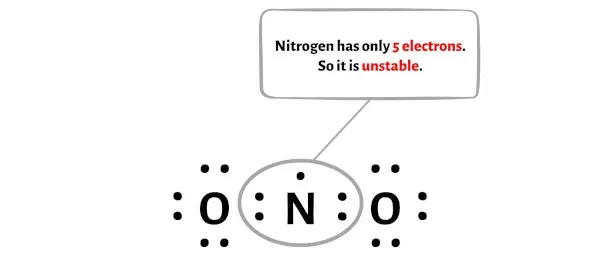
さて、この窒素原子を安定させるには、外側の酸素原子から電子対を移動させて窒素原子をより安定させる必要があります。
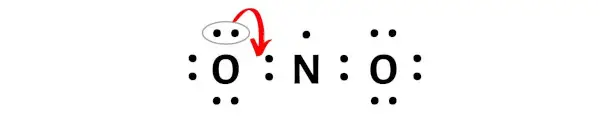
この電子対を移動させた後、中心の窒素原子はさらに 2 個の電子を受け取り、その合計電子数は 7 になります。
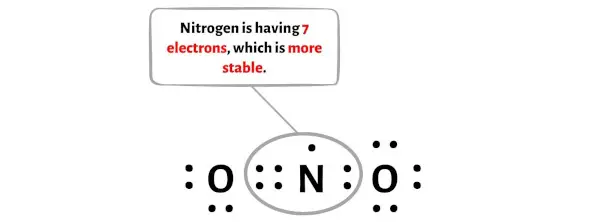
窒素はオクテットを形成していないことがわかります (電子が 7 つあるため)。ここで電子対をさらに動かそうとすると、7 + 2 = 9 個の電子が存在することになります。
そして窒素原子には9個の電子を保持する能力はありません。したがって、NO2 (窒素原子上に 7 つの電子を持つ) の上記のルイス構造は安定です。
上記の NO2 のルイス ドット構造では、結合電子の各ペア (:) を単結合(|) として表すこともできます。そうすると、NO2 は次のようなルイス構造になります。
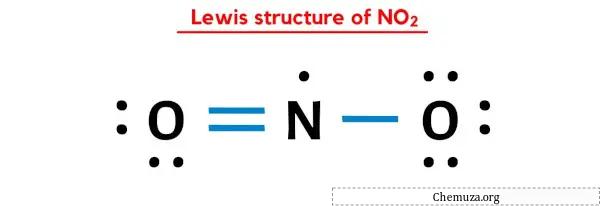
上記の手順をすべて完全に理解していただければ幸いです。
さらに練習して理解を深めたい場合は、以下にリストされている他のルイス構造を試してみてください。
理解を深めるために、次のルイス構造を試してください (または少なくとも見てください)。
