二硫化炭素は、炭素と硫黄が結合して形成される揮発性化合物です。工業プロセス、溶剤、レーヨン繊維の製造に使用されます。
| IUPAC名 | 二硫化炭素 |
| 分子式 | CS2 |
| CAS番号 | 75-15-0 |
| 同義語 | 二硫化炭素、ジチオカルブ、二硫化炭素 |
| インチチ | InChI=1S/CS2/c2-1-3 |
二硫化炭素の性質
二硫化炭素の式
二硫化炭素の化学式はCS2です。 1 つの炭素原子と 2 つの硫黄原子が直線状に結合して構成されています。この単純な式は、化合物の基本組成を理解するために不可欠です。
二硫化炭素のモル質量
二硫化炭素のモル質量は約 76.14 g/mol です。これを計算するには、1 つの炭素原子 (12.01 g/mol) と 2 つの硫黄原子 (それぞれ 32.06 g/mol) の原子量を追加します。モル質量を知ることは、さまざまな化学計算に役立ちます。
二硫化炭素の沸点
二硫化炭素の沸点は約 46.3°C (115.3°F) と比較的低くなります。この特性により、揮発性が高く蒸発しやすくなります。沸点が低いということは、急速な蒸発を必要とする工業プロセスや用途において重要です。
二硫化炭素の融点
二硫化炭素の融点は約 -110.8°C (-187.4°F) です。この温度以下では固体状態を維持しますが、加熱すると液体状態に変化します。融点を理解することは、取り扱いと保管の際に非常に重要です。
二硫化炭素の密度 g/mL
二硫化炭素の密度は室温で約 1.26 g/mL です。この値は単位体積あたりの質量を意味します。水よりも密度が高いため、混合すると沈み、その密度はさまざまな溶媒への溶解性に影響します。
二硫化炭素の分子量
二硫化炭素の分子量は、化学式から計算すると約 76.14 g/mol です。この値は、化学量論および化学反応における化合物の量を決定する際に重要な役割を果たします。
二硫化炭素の構造
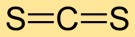
二硫化炭素は、中心に炭素原子、両側に硫黄原子を持つ直線状の分子構造を持っています。この単純な配置は、その化学的挙動や他の物質との相互作用を理解するために非常に重要です。
二硫化炭素の溶解度
二硫化炭素は水に溶けにくく、室温では水 100 ml あたりわずか約 0.2 g です。ただし、ベンゼンやエタノールなどの有機溶媒には非常によく溶けます。この溶解挙動は、化学や産業におけるさまざまな用途に不可欠です。
| 外観 | 無色の液体 |
| 比重 | 1.26 |
| 色 | 無色 |
| 匂い | 刺激的で甘い香り |
| モル質量 | 76.14g/モル |
| 密度 | 1.26g/ml |
| 融合点 | -110.8°C (-187.4°F) |
| 沸点 | 46.3°C (115.3°F) |
| フラッシュドット | -30°C (-22°F) |
| 水への溶解度 | 0.2g/100ml(20℃) |
| 溶解性 | ベンゼンやエタノールなどの有機溶媒に可溶 |
| 蒸気圧 | 318mmHg(20℃) |
| 蒸気密度 | 2.62 (空気 = 1) |
| pKa | ~ -2 |
| pH | 中性(pH7) |
二硫化炭素の安全性と危険性
二硫化炭素は重大な安全上のリスクをもたらします。引火性が高く、その蒸気は空気中で爆発性混合物を形成する可能性があります。長時間暴露すると、めまい、頭痛、さらには意識喪失を引き起こす可能性があります。また、水生生物や環境にも有害です。リスクを最小限に抑えるには、適切な換気、個人用保護具、耐火性の保管場所が不可欠です。刺激や損傷を引き起こす可能性があるため、皮膚や目との接触を避けてください。取り扱いは十分に管理された環境で行う必要があり、流出は迅速に阻止される必要があります。二硫化炭素を取り扱う際の事故を防止し、安全な作業環境を確保するには、安全上の指示を理解して従うことが不可欠です。
| ハザードシンボル | 可燃性、有害 |
| セキュリティの説明 | 引火性の高い液体および蒸気。吸入したり飲み込んだりすると有害です。皮膚や目の炎症を引き起こします。 |
| 国連識別番号 | UN1131 |
| HSコード | 2813.10.1000 |
| 危険等級 | 3 (引火性液体) |
| 梱包グループ | II(中危険) |
| 毒性 | 中程度の毒性 |
二硫化炭素の合成方法
いくつかの有効な方法により、二硫化炭素の合成が可能になります。
一般的な方法では、硫黄とメタンまたは天然ガスを高温で反応させ、生成物として CS2 を生成します。
別のアプローチは、硫黄蒸気を高温の石炭と反応させることです。さらに、触媒上で一酸化炭素と硫黄蒸気が結合すると、二硫化炭素が生成される可能性があります。
さらに、高温で炭素が硫黄蒸気と反応すると、CS2 の直接合成が発生する可能性があります。研究室では、化学者はザントゲン酸カリウムと硫酸の反応を利用して二硫化炭素を小規模に製造します。
二硫化炭素は引火性が高く有毒な性質があるため、各方法では適切な安全上の注意が必要です。これらの合成方法の多用途性により、溶媒としての使用、化学プロセスの原料としての使用、レーヨン繊維の製造など、さまざまな産業用途が可能になります。
二硫化炭素の用途
二硫化炭素はその多用途な特性により、さまざまな用途に使用されます。その用途の一部を次に示します。
- 研究および実験室での応用: 研究室では、有機金属化合物の合成を含むさまざまな化学反応の試薬として二硫化炭素を使用します。
- エッセンシャルオイルの抽出: 二硫化炭素は植物からのエッセンシャルオイルの抽出に応用され、目的の芳香族化合物の分離を促進します。
- 油の抽出: 産業では、二硫化炭素の溶解性と沸点の低さから、種子や野菜から油を抽出するために二硫化炭素が使用されています。
- レーヨン繊維の製造: 二硫化炭素はセルロースの溶解を助けるため、レーヨン繊維の製造において重要な役割を果たします。二硫化炭素はセルロースを押し出し、織物に使用される合成繊維を形成します。
- 産業用途: 二硫化炭素は、殺虫剤、燻蒸剤、ゴム用化学薬品の製造に貢献します。さらに、硫酸や四塩化炭素の製造において触媒としても作用します。
- 溶剤: 二硫化炭素は、オイル、グリース、ゴム、樹脂、硫黄などのさまざまな物質の溶剤として機能します。そのため、セルロースベースの製品の製造に一般的に使用されています。
- 化学プロセス: 四塩化炭素、チオカルバミン酸塩、ジチオカルバミン酸塩などの有機化合物の合成の原料として機能します。これらの化合物は、農業および製薬産業で応用されています。
- ゴムの加硫:二硫化炭素はゴムの加硫プロセスに関与し、ゴムの強度、弾性、耐摩耗性を向上させます。
これらの多様な用途は、繊維や農業から研究や製造に至るまで、複数の産業における二硫化炭素の重要性を浮き彫りにしています。
質問:
Q: 次の分子のうち極性があるのはどれですか? A. アンモニア B. オクタン c.水 d.二硫化炭素
A: a、水 (H2O) は、その湾曲した分子形状と電子の共有が不均等であるため、極性があります。
Q: 二硫化炭素 (CS2) 分子の炭素と硫黄の結合間の角度はどれくらいですか?
A: CS2 の炭素と硫黄の結合間の角度は 180 度で、直線状の形状を形成しています。
Q: 1 モルの二硫化炭素には合計何個の原子が含まれていますか?
A: 1 モルの二硫化炭素には 6.02 x 10^23 個の分子が含まれており、各分子には 3 つの原子 (炭素 1 個と硫黄 2 個) があります。
Q: 次の元素のうち、非極性溶媒である二硫化炭素 CS2 に溶けると思うのはどれですか?
A: オクタン (b) のような非極性物質は、二硫化炭素 (CS2) に可溶である必要があります。
Q: 二硫化炭素の標準沸点は何度ですか?
A: 二硫化炭素の標準沸点は約 46.3°C (115.3°F) です。
Q: 二硫化炭素は極性ですか、それとも無極性ですか?
A: 二硫化炭素 (CS2) は、その直線状の形状と電子の均等な共有により、無極性分子です。
Q: 二硫化炭素の式は何ですか?
A: 二硫化炭素の化学式は CS2 です。
Q: 二硫化炭素とは何ですか?
A: 二硫化炭素 (CS2) は、1 つの炭素原子と 2 つの硫黄原子で構成される揮発性化合物で、さまざまな産業用途に使用されます。
Q: 二硫化炭素が水よりも密度が高いという事実はどの程度重要ですか?
A: 水に比べて二硫化炭素の密度が高いため、混合しにくく、結合したときに明確な層を形成します。
Q: 人間はどのようにして二硫化炭素に遭遇するのでしょうか?
A: 人間は、工業プロセス、化学用途、または特定の製品の取り扱いを通じて二硫化炭素に接触する可能性があります。
Q: 二硫化炭素を摂取するとどうなりますか?
A: 二硫化炭素を摂取すると、吐き気、頭痛、神経系への影響などの健康上の問題を引き起こす可能性があり、人間の健康に危険をもたらします。
Q: 二硫化炭素は水より密度が高いのですか?
A: はい、二硫化炭素は水よりも密度が高く、水の密度 1 g/mL と比較して密度は約 1.26 g/mL です。
