エタンは、化学式 C2H6 の炭化水素です。それは燃料として一般的に使用され、天然ガスの成分です。エタンには 2 つの炭素原子と 6 つの水素原子があります。
| IUPAC名 | エタン |
| 分子式 | C2H6 |
| CAS番号 | 74-84-0 |
| 同義語 | ジエチル、ジメチル、水素化エチル、メチルメタン |
| インチチ | InChI=1S/C2H6/c1-2/h1-2H3 |
エタンの性質
エタンの式
エタンの化学式は C2H6 です。これは、各エタン分子が 2 つの炭素原子と 6 つの水素原子で構成されていることを示しています。この式は、エタンの組成とその構造配置を理解するのに役立ちます。
エタンモル質量
水素化エチルのモル質量は、その構成要素の原子質量を加算することによって計算されます。炭素の原子質量は 12.01 g/mol、水素の原子質量は 1.008 g/mol です。原子質量にそれぞれの数を掛けて加算すると、水素化エチルのモル質量が得られ、これは約 30.07 g/mol になります。
エタンの沸点
水素化エチルの沸点は摂氏-88.6度です。これは、標準大気圧では、その温度まで加熱すると水素化エチルが液体から気体に変化することを意味します。沸点は、水素化エチルが蒸発できる条件を決定するため、重要な特性です。
エタンの融点
水素化エチルの融点は摂氏-182.8度です。この温度より低い温度では、水素化エチルは固体の形で存在します。この温度以上に加熱すると、水素化エチルは固体から液体に相変化します。融点は、冷却または加熱プロセス中の水素化エチルの物理的挙動を理解するために重要です。
エタン密度 g/mL
水素化エチルの密度は、標準温度および圧力で約 0.55 g/mL です。密度は、特定の体積内に存在する質量の量の尺度です。水素化エチルの場合、分子がどの程度密に詰まっているかがわかり、その物理的特性についての洞察が得られます。
エタンの分子量
水素化エチルの分子量は 30.07 g/mol です。これは、単一の水素化エチル分子内のすべての原子の原子質量の合計です。分子量は、特定の質量または体積中にどれだけの水素化エチルが存在するかを判断するのに役立ちます。
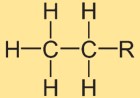
エタンの構造
水素化エチルの構造は、単共有結合で結合した 2 つの炭素原子から構成されます。各炭素原子は 3 つの水素原子に囲まれています。構造配置は直線的で、水素原子が炭素-炭素結合の周りに対称的に配置されています。
エタンの溶解度
水素化エチルは水にあまり溶けません。水は極性溶媒であるのに対し、それは非極性分子です。水素化エチルのような非極性分子は分子間力が弱く、極性溶媒には容易に溶解しません。ただし、水素化エチルはヘキサンやベンゼンなどの他の非極性溶媒に溶解します。
| 外観 | 無色の気体 |
| 比重 | 1.038g/L |
| 色 | 該当なし |
| 匂い | 無臭 |
| モル質量 | 30.07g/モル |
| 密度 | 0.55g/ml |
| 融合点 | -182.8℃ |
| 沸点 | -88.6℃ |
| フラッシュドット | -135℃ |
| 水への溶解度 | 不溶性 |
| 溶解性 | 非極性溶媒に可溶 |
| 蒸気圧 | 46.9 psi (21°C 時) |
| 蒸気密度 | 1.52 (空気 = 1) |
| pKa | ~50 |
| pH | 該当なし |
エタンの安全性と危険性
水素化エチルには、いくつかの安全上の考慮事項と危険性があります。可燃性が高く、空気と爆発性混合物を形成する可能性があります。炎や熱源にさらされると、水素化エチルが発火し、火災や爆発を引き起こす可能性があります。水素化エチルは、発火源から離れた換気の良い場所で取り扱い、保管することが重要です。水素化エチルは密閉空間内の酸素を置換するため、窒息の危険性もあります。高濃度の水素化エチルを吸入すると、めまい、吐き気、さらには意識喪失を引き起こす可能性があります。これらのリスクを軽減するために、水素化エチルを扱う、またはその近くで作業する場合は、適切な個人用保護具を使用し、安全手順に従うことが不可欠です。
| ハザードシンボル | 可燃性ガス |
| セキュリティの説明 | 熱、火花、裸火から遠ざけてください。換気の良い場所で使用してください。火災や爆発の危険を避けるため、適切な予防措置を講じて取り扱ってください。 |
| 国連識別番号 | UN1035 |
| HSコード | 29011000 |
| 危険等級 | 2.1 (可燃性ガス) |
| 梱包グループ | 適用できない |
| 毒性 | エタンは毒性が強いとは考えられていません。ただし、高濃度を吸入すると窒息を引き起こす可能性があります。適切な換気を行いながら使用し、長時間の暴露を避けてください。 |
エタンの合成法
水素化エチルはさまざまな方法で合成されます。
一般的な方法は蒸気分解プロセスであり、蒸気の存在下で炭化水素(通常は水素化エチルまたはより重い炭化水素)を高温(約 750 ~ 900 °C)で加熱します。このプロセスにより、熱分解や転位などの反応が引き起こされ、水素化エチル、エチレン、プロピレンが生成されます。
別の方法には、アセチレンの接触水素化が含まれます。この方法では、アセチレンガスがパラジウムやニッケルなどの適切な触媒上で水素と反応し、水素化エチルが生成されます。この方法は、反応性が高く潜在的に危険なアセチレンを、より安定で反応性の低い水素化エチルに選択的に変換します。
エタンは、極低温抽出によって天然ガスから得ることもできます。天然ガス(主に水素化メチル)は低温高圧にさらされ、水素化エチルが分離・回収されます。天然ガス処理プラントでは、さまざまな産業用途に貴重な水素化エチルを抽出するためにこのプロセスが一般的に使用されています。
さらに、石油精製および一部の石油化学プロセスでは副産物として水素化エチルが生成されます。蒸留や吸収などの技術により、水素化エチルが他の炭化水素流から分離されます。
全体として、これらの合成方法は、幅広い化学物質、プラスチック、燃料の製造に重要な原料である水素化エチルの生産を可能にし、世界中の多くの産業に貢献しています。
エタンの用途
水素化エチルは、その多用途な特性により、さまざまな産業で応用されています。水素化エチルの主な用途をいくつか紹介します。
- 石油化学産業: 水素化エチルは、プラスチック、樹脂、合成繊維の基礎となるエチレンの製造に不可欠な原料です。これは、世界で最も使用されているプラスチックの 1 つであるポリエチレンの製造における重要な要素です。
- 燃料とエネルギー: 水素化エチルは、特定の産業プロセスに燃料を供給し、動力を供給する役割を果たしており、天然ガスの構成成分です。産業では水素化エチルを燃焼させて熱や電気を生成し、住宅、商業、産業用途のエネルギー源として機能します。
- 冷凍: 低温システムなどの一部の用途では、水素化エチルが冷媒として機能し、効率的な冷却機能を提供します。効率的な冷却機能を提供し、環境への影響がより高い他の冷媒の代替品となります。
- 溶媒: 水素化エチルは、特に実験室で非極性溶媒として機能します。水素化エチルは、抽出、精製、分析などのプロセスを容易にします。
- 校正ガス: 水素化エチルは、ガス検出器および分析装置の混合ガスの校正の成分として機能し、ガス検出装置の校正と検証を可能にします。
- エアゾール噴射剤: 水素化エチルはさまざまな製品でエアゾール噴射剤として機能し、圧力が解放されると内容物を容器から放出します。化粧品、塗料、家庭用品などの物質をスプレーするのに必要な力を与えます。
- 化学合成: 水素化エチルは、エタノール、エチレンオキシド、塩化ビニルなどのさまざまな有機化学物質を合成するための原料として機能します。これらの化学物質は、溶剤、プラスチック、洗剤、PVC パイプなどの製造に応用されています。
これらの多様な用途は、複数の業界にわたる水素化エチルの重要性を浮き彫りにし、現代の製造業や日常生活において重要な要素となっています。
質問:
Q: C2H6 は極性ですか、それとも無極性ですか?
A: C2H6 (水素化エチル) は、炭素と水素の電気陰性度の差が小さく、電子密度が均一に分布するため、無極性分子です。
Q: 0.500 モルの C2H6 には何モルの炭素原子がありますか?
A: C2H6 の各分子には 2 つの炭素原子が含まれるため、0.500 モルの C2H6 には 1.00 モルの炭素原子が存在します。
Q: C2H6 の実験式は何ですか?
A: C2H6 の実験式は CH3 で、これは分子内に存在する原子の最も単純な比率を表します。
Q:C2H6とは何ですか?
A: C2H6 は、燃料および天然ガスの成分として一般に使用されるガス状炭化水素である水素化エチルの化学式です。
Q: エタン (C2H6) にはなぜ構造異性体がないのですか?
A: 水素化エチル (C2H6) には、その炭素原子が単結合で結合されており、他の配置のない直鎖構造となっているため、構造異性体がありません。
Q: C2H6 には水素結合がありますか?
A: C2H6 (水素化エチル) には、窒素、酸素、フッ素などの電気陰性度の高い元素に結合する水素原子が欠けているため、水素結合がありません。
Q: C2H6 はイオン性ですか、それとも共有結合性ですか?
A: C2H6 は、炭素原子と水素原子の間の電子の共有によって形成されるため、共有結合性化合物です。
Q: C2H6 は水に溶けますか?
A: C2H6 は非極性分子であり、極性溶媒には容易に溶解しないため、水に不溶です。
Q: 混合ガスには CH4 と C2H6 が等モル比で含まれていますか?
A: はい、ガス混合物に CH4 と C2H6 が等モル比率で含まれている場合、混合物中の CH4 のモル数が C2H6 のモル数と等しいことを意味します。
