アニリン (C6H5NH2) は、染料、医薬品、ゴム用化学薬品の製造に使用される芳香族アミンです。独特の臭気があり、さまざまな有機化合物の前駆体です。
| IUPAC名 | アニリン |
| 分子式 | C6H7N |
| CAS番号 | 62-53-3 |
| 同義語 | アミノベンゼン、ベンゼンアミン |
| インチチ | InChI=1S/C6H7N/c7-6-4-2-1-3-5-6/h1-5H,7H2 |
アニリンの性質
アニリン式
アニリンの化学式は C6H7N です。 6 個の炭素原子、7 個の水素原子、1 個の窒素原子で構成されています。これらの原子の配置により、アニリンに独特の化学的特性が与えられます。
アニリンのモル質量
C6H5NH2 のモル質量は、そのすべての構成要素の原子質量を加算することによって計算されます。 C6H5NH2 のモル質量は、1 モルあたり約 93.13 グラム (g/mol) です。この値は、C6H5NH2 を含むさまざまな化学計算や反応に役立ちます。
アニリンの沸点
C6H5NH2 の沸点は約 184 ℃です。この温度では、C6H5NH2 は液体から気体に相変化します。沸点は、C6H5NH2 が気化できる条件を決定する重要な特性です。
アニリンの融点
C6H5NH2 の融点は約 -6 ℃です。これは、固体の C6H5NH2 が液体状態に変化する温度です。融点は、さまざまな温度条件下での C6H5NH2 の物理的状態を決定する際に重要です。
アニリン密度 g/mL
C6H5NH2 の密度は約 1.02 グラム/ミリリットル (g/mL) です。密度は単位体積あたりの物質の質量を表します。 C6H5NH2 の密度値は、空間の所定の体積における C6H5NH2 の緻密性または濃度に関する情報を提供します。
アニリンの分子量
C6H5NH2 の分子量は約 93.13 グラム/モル (g/mol) です。これは、C6H5NH2 の化学式に含まれるすべての原子の原子量の合計です。分子量は、化学量論計算や反応に必要な C6H5NH2 の量の決定において重要な役割を果たします。
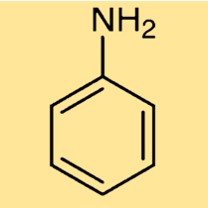
アニリン構造
C6H5NH2は、ベンゼン環(炭素原子の六角形の環)に水素原子の代わりにアミノ基(-NH2)がついた構造をしています。この構造により、C6H5NH2 に芳香族および塩基性の特性が与えられ、さまざまな産業用途に役立ちます。
アニリンの溶解度
C6H5NH2 は水には溶けにくいですが、エタノール、エーテル、クロロホルムなどの有機溶媒には簡単に溶けます。その溶解度は、C6H5NH2 と溶媒の間の極性と分子間力によって影響されます。この特性により、C6H5NH2 をさまざまな化学プロセスや配合に簡単に組み込むことができます。
| 外観 | 無色~淡黄色の液体 |
| 比重 | 1.02g/ml |
| 色 | 無色~淡黄色 |
| 匂い | 特有の臭気 |
| モル質量 | 93.13 g/モル |
| 密度 | 1.02g/ml |
| 融合点 | -6℃ |
| 沸点 | 184℃ |
| フラッシュドット | 70℃ |
| 水への溶解度 | 難溶性 |
| 溶解性 | 有機溶剤に可溶 |
| 蒸気圧 | 5.60mmHg |
| 蒸気密度 | 3.24 (空気=1) |
| pKa | 4.61 |
| pH | ほぼ中立 |
アニリンの安全性と危険性
C6H5NH2 は潜在的な安全上のリスクを引き起こすため、慎重に取り扱う必要があります。飲み込んだり、吸入したり、皮膚から吸収されたりすると有害です。 C6H5NH2 に直接接触すると、目、皮膚、呼吸器系に炎症を引き起こす可能性があります。長期間または繰り返し暴露すると、皮膚炎や血液疾患などのより深刻な影響を引き起こす可能性があります。 C6H5NH2 も可燃性であり、その蒸気は空気中で爆発性混合物を形成する可能性があります。 C6H5NH2 を扱う場合は、適切な換気と個人用保護具を使用する必要があります。リスクを最小限に抑え、人々と環境の安全を確保するには、適切な保管、取り扱い、廃棄の実践が不可欠です。
| ハザードシンボル | て、ん |
| セキュリティの説明 | 皮膚や目との接触を避けてください。換気の良い場所で使用してください。手袋と保護服を着用して取り扱ってください。 |
| 国連識別番号 | 国連 1547 |
| HSコード | 2921.43.0000 |
| 危険等級 | 6.1 (有毒物質) |
| 梱包グループ | Ⅲ |
| 毒性 | 飲み込んだり、吸入したり、皮膚から吸収した場合は有毒です。炎症、皮膚炎、血液疾患を引き起こす可能性があります。 |
アニリンの合成法
C6H5NH2 はさまざまな方法で合成できます。
一般的な方法はニトロベンゼン還元です。このプロセスでは、鉄やすりやスズなどの還元剤が、塩酸などの強酸の存在下でニトロベンゼンと反応します。この反応により、ニトロ基 (-NO2) がアミノ基 (-NH2) に変換され、C6H5NH2 が生成されます。
別の方法では、パラジウムや白金などの触媒上で水素ガスを使用してニトロベンゼンを還元します。 C6H5NH2を製造する工業的方法では、接触水素化と呼ばれるプロセスが広く使用されています。
C6H5NH2 を得るには、ニトロベンゼンの還元に硫化ナトリウムまたは重亜硫酸ナトリウムを使用できます。これらの還元剤は、ニトロ基のアミノ基への変換を促進します。
C6H5NH2 を合成するには、水酸化ナトリウムなどの強塩基の存在下でクロロベンゼンをアンモニアで処理します。サンドマイヤー反応として知られるこのプロセスでは、塩素がアミノ基に置換され、C6H5NH2 が生成されます。
さらに、アゾベンゼンまたはアゾキシベンゼンを還元することによって C6H5NH2 を調製できます。これには、窒素-窒素結合を切断してアミノ基を形成することが含まれます。
これらの合成方法は、C6H5NH2 を得るさまざまなアプローチを提供し、実験室規模および工業規模での生産を可能にします。方法の選択は、原料の入手可能性、反応条件、最終生成物の望ましい純度などの要因によって異なります。
アニリンの用途
C6H5NH2 は、その多様な特性により、さまざまな産業で応用されています。一般的な用途のいくつかを次に示します。
- 染料の製造: C6H5NH2 は、繊維、皮革、製紙産業で使用される合成染料や顔料を含む、多くの染料製造の重要な原料として機能します。
- 製薬産業: C6H5NH2 誘導体は、鎮痛剤、解熱剤、抗マラリア剤などの医薬品の合成において重要です。
- ゴム用化学物質: C6H5NH2 は、ゴム産業における促進剤や酸化防止剤の製造において重要な成分として、ゴム製品の性能と耐久性を積極的に向上させます。
- 除草剤および殺虫剤: 農家は除草剤および殺虫剤の配合に C6H5NH2 誘導体を積極的に使用しており、それによって農業における雑草や害虫を効果的に防除しています。
- ポリウレタンの製造: C6H5NH2 は、建設業界や自動車業界で広く使用されているポリウレタン フォーム、コーティング、接着剤の合成に不可欠な成分です。
- 化学中間体: C6H5NH2 は、ゴム化学薬品、医薬品、農薬などのさまざまな有機化合物を合成するための多用途の構成要素として機能します。
- さまざまな物質の溶剤:C6H5NH2は、油脂、ワックス、樹脂などさまざまな物質を積極的に溶解します。
- 実験室試薬: 有機合成の実験室での実験では、研究者は C6H5NH2 を試薬として使用し、一部の反応では触媒として使用します。
- 写真用薬品: C6H5NH2 誘導体は、現像液や染料などの写真用薬品の製造に積極的に貢献しています。
- 重合開始剤: C6H5NH2 は特定の重合反応において開始剤として機能し、特定の特性を持つポリマーの形成を可能にします。
これらの多様な用途は、繊維、製薬から農業、製造に至るまでの産業における C6H5NH2 の重要性を浮き彫りにしています。
質問:
Q: アニリンより塩基性の高い化合物はどれですか?
A: アンモニア (NH3) は C6H5NH2 よりも塩基性です。
Q:アニリンステッチとは何ですか?
A: C6H5NH2 点は、等量の C6H5NH2 と特定の溶媒が完全に混和する最低温度です。
Q:アニリンとは何ですか?
A: アニリンは化学式 C6H7N を持つ芳香族アミンで、染料、医薬品、ゴムの化学薬品に一般的に使用されます。
Q: ナフタレンとアニリンを分離するにはどうすればよいですか?
A: ナフタレンと C6H5NH2 は、沸点の違いを利用した分別蒸留と呼ばれる方法で分離できます。
Q: アニリンからフェノールはどのように調製されますか?
A: フェノールは、ジアゾ化と呼ばれるプロセスによって C6H5NH2 から合成され、その後加水分解されてフェノールが生成されます。
Q: アニリンレザーのお手入れ方法は?
A: C6H5NH2 レザーをきれいにするには、柔らかく湿らせた布を使用して汚れを優しく取り除き、刺激の強い化学物質や過度の湿気を避けてください。
Q: 安息香酸の共役塩基とアニリンの共役酸は何ですか?
A: 安息香酸の共役塩基は安息香酸イオン (C6H5COO-) であり、C6H5NH2 の共役酸はアニリニウムイオン (C6H5NH3+) です。
Q:アニリンレザーとは何ですか?
A: C6H5NH2 レザーは、C6H5NH2 染料で染色された革の一種で、革の自然な質感と外観を保ちながら、柔らかく高級感を保ちます。
