Il tribromuro di fosforo (PBr3) è un composto costituito da un atomo di fosforo e tre atomi di bromo. Viene utilizzato come reagente in varie reazioni chimiche, soprattutto nella sintesi di composti organici.
| Nome IUPAC | Tribromuro di fosforo |
| Formula molecolare | PBr3 |
| numero CAS | 7789-60-8 |
| Sinonimi | Bromuro di fosforo (III), bromuro di bromofosforo, tribromofosfina |
| InChI | InChI=1S/Br3P/c1-4(2)3 |
Proprietà del tribromuro di fosforo
Formula del tribromuro di fosforo
La formula del bromuro di fosforo (III) è PBr3. È costituito da un atomo di fosforo e tre atomi di bromo. Questo composto si forma quando il fosforo reagisce con il bromo. La formula rappresenta accuratamente la composizione del composto.
Massa molare del tribromuro di fosforo
La massa molare del bromuro di fosforo (III) può essere calcolata sommando le masse atomiche dei suoi elementi costitutivi. Il fosforo ha una massa atomica di circa 31,0 grammi per mole, mentre il bromo ha una massa atomica di circa 79,9 grammi per mole. Aggiungendo tre volte la massa atomica del bromo alla massa atomica del fosforo si ottiene la massa molare del bromuro di fosforo (III), che è di circa 270,7 grammi per mole.
Punto di ebollizione del tribromuro di fosforo
Il bromuro di fosforo (III) ha un punto di ebollizione di circa 173 gradi Celsius. Ciò significa che a temperature superiori a questo punto, il composto subirà un cambiamento di fase da liquido a gassoso. Il punto di ebollizione è una caratteristica importante che aiuta a determinare le condizioni in cui il composto può essere utilizzato o purificato.
Punto di fusione del tribromuro di fosforo
Il punto di fusione del bromuro di fosforo (III) è di circa -41 gradi Celsius. Questa temperatura indica il punto in cui il composto passa dallo stato solido a quello liquido. Conoscere il punto di fusione è fondamentale per gestire e manipolare il composto in vari processi chimici.
Densità del tribromuro di fosforo g/mL
La densità del bromuro di fosforo (III) è di circa 2,85 grammi per millilitro (g/mL). La densità misura la massa di una sostanza per unità di volume. Con la sua densità relativamente elevata, il bromuro di fosforo (III) è più denso di molti altri liquidi comuni, indicando che è relativamente pesante rispetto al suo volume.
Peso molecolare del tribromuro di fosforo
Il peso molecolare del bromuro di fosforo (III) è di circa 270,7 grammi per mole. Questo valore si calcola sommando le masse atomiche di tutti gli atomi presenti nel composto, in base alla formula molecolare PBr3. Il peso molecolare è utile in vari calcoli, inclusa la determinazione della quantità di sostanza presente in una data massa.
Struttura del tribromuro di fosforo
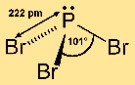
Il bromuro di fosforo (III) ha una struttura molecolare piramidale. È costituito da un atomo di fosforo centrale legato a tre atomi di bromo. Questa disposizione conferisce alla molecola una forma piramidale trigonale, con l’atomo di fosforo in alto e gli atomi di bromo alla base. Questa struttura è importante per comprendere la reattività e il comportamento del composto nelle reazioni chimiche.
Solubilità del tribromuro di fosforo
Il bromuro di fosforo (III) è scarsamente solubile in acqua. Reagisce con l’acqua per produrre acido bromidrico e acido fosforoso. Tuttavia, è solubile in solventi organici come benzene e tetracloruro di carbonio. La solubilità determina la misura in cui un composto può dissolversi in un particolare solvente, il che ha implicazioni per le sue applicazioni e la sua manipolazione in vari processi.
| Aspetto | Liquido incolore |
| Peso specifico | 2,85 g/ml |
| Colore | Incolore |
| Odore | Acri |
| Massa molare | 270,7 g/mole |
| Densità | 2,85 g/ml |
| Punto di fusione | -41°C |
| Punto di ebollizione | 173°C |
| Punto flash | Non disponibile |
| solubilità in acqua | Reagisce |
| Solubilità | Solubile in solventi organici come benzene e tetracloruro di carbonio |
| Pressione del vapore | Non disponibile |
| Densità del vapore | Non disponibile |
| pKa | Non disponibile |
| pH | Non disponibile |
Sicurezza e pericoli del tribromuro di fosforo
Il bromuro di fosforo (III) comporta alcuni rischi per la sicurezza e deve essere maneggiato con cautela. È corrosivo e può provocare gravi ustioni a contatto con la pelle, gli occhi o il sistema respiratorio. L’inalazione o l’ingestione diretta di questo composto può causare irritazione respiratoria e gastrointestinale. Reagisce violentemente con l’acqua liberando fumi tossici e generando calore. Quando si lavora con il bromuro di fosforo (III) è necessario utilizzare una ventilazione adeguata e dispositivi di protezione individuale, come guanti e occhiali. Inoltre, dovrebbe essere conservato lontano da sostanze incompatibili per evitare potenziali reazioni. Nel complesso, il rigoroso rispetto dei protocolli di sicurezza e la conoscenza dei pericoli associati a questo composto sono essenziali per una manipolazione sicura.
| Simboli di pericolo | Corrosivo |
| Descrizione della sicurezza | Maniglia con cauzione. Evitare il contatto con la pelle, gli occhi e le vie respiratorie. Utilizzare una ventilazione adeguata e dispositivi di protezione individuale. Conservare lontano da sostanze incompatibili. |
| Numeri di identificazione delle Nazioni Unite | ONU1805 |
| Codice SA | 2812.90.90 |
| Classe di pericolo | 8 (Corrosivo) |
| Gruppo di imballaggio | II |
| Tossicità | Tossico per inalazione e ingestione. Può causare gravi ustioni e irritazioni. |
Metodi per la sintesi del tribromuro di fosforo
In un metodo comune di sintesi del bromuro di fosforo (III), il recipiente di reazione combina direttamente fosforo elementare e bromo, solitamente in condizioni controllate. La reazione procede con il trasferimento degli atomi di bromo agli atomi di fosforo, dando luogo alla formazione di bromuro di fosforo (III).
Un altro metodo prevede la reazione tra tricloruro di fosforo (PCl3) e acido bromidrico (HBr) . In questo approccio, il tricloruro di fosforo reagisce prima con il gas di acido bromidrico, producendo bromuro di fosforo (III) e gas di acido cloridrico come sottoprodotti. Questo metodo offre una via alternativa per ottenere il bromuro di fosforo (III).
Nel “metodo del fosforo rosso”, il fosforo rosso viene combinato con bromo o acido bromidrico e la reazione viene condotta in condizioni controllate. Il fosforo rosso funge da fonte di fosforo, reagendo con il bromo o l’acido bromidrico per produrre bromuro di fosforo (III).
Questi metodi sintetici aprono strade per la produzione di bromuro di fosforo (III), ciascuno con i propri vantaggi e considerazioni. La scelta del metodo dipende da fattori quali la disponibilità dei reagenti, la resa desiderata e le condizioni specifiche di reazione. È importante eseguire queste sintesi in un laboratorio ben attrezzato, rispettando i protocolli di sicurezza e le procedure per la manipolazione delle sostanze chimiche coinvolte.
Usi del tribromuro di fosforo
Il bromuro di fosforo (III) trova varie applicazioni grazie alla sua reattività e proprietà uniche. Ecco alcuni dei suoi usi:
- Sintesi organica: i chimici utilizzano ampiamente il bromuro di fosforo (III) come reagente nella sintesi organica per convertire gli alcoli in bromuri alchilici, un passaggio chiave nella sintesi di molti composti organici.
- Industria farmaceutica: la produzione di prodotti farmaceutici fa molto affidamento sul bromuro di fosforo (III) per sintetizzare vari farmaci intermedi e ingredienti farmaceutici attivi (API).
- Ritardanti di fiamma: i produttori utilizzano bromuro di fosforo (III) nella produzione di ritardanti di fiamma, migliorando le proprietà resistenti al fuoco di alcuni polimeri per l’uso in settori come quello elettronico e tessile.
- Produzione chimica: il bromuro di fosforo (III) funge da prezioso intermedio nella produzione di altri prodotti chimici, inclusi composti del fosforo come derivati dell’acido fosforico, fosfonati e fosfati.
- Erbicidi e pesticidi: la sintesi di ingredienti attivi specifici utilizzati negli erbicidi e nei pesticidi utilizza il bromuro di fosforo (III) per controllare efficacemente le erbe infestanti, i parassiti e le malattie in agricoltura.
- Ricerca di laboratorio: in laboratorio, i ricercatori usano comunemente il bromuro di fosforo (III) come reagente in vari esperimenti e reazioni, in particolare quelli che coinvolgono la bromurazione e la manipolazione di composti organici.
- Analisi chimiche: il bromuro di fosforo(III) trova applicazione nelle tecniche di analisi chimica, consentendo la determinazione della presenza di gruppi funzionali specifici nei composti organici attraverso reazioni di sostituzione del bromo.
Questi diversi usi evidenziano l’importanza del bromuro di fosforo (III) nella sintesi organica, nei prodotti farmaceutici, nei ritardanti di fiamma, nella produzione chimica, nell’agricoltura, nella ricerca di laboratorio e nell’analisi chimica. La sua reattività e versatilità lo rendono un composto prezioso in vari settori e discipline scientifiche.
Domande:
D: Perché AlBr3 è chiamato bromuro di alluminio mentre PBr3 è tribromuro di fosforo?
R: La convenzione di denominazione per i composti che coinvolgono metalli utilizza generalmente il nome elementare del metallo seguito dal nome del non metallo, mentre nel caso di PBr3, il fosforo viene specificato per indicare la presenza di un atomo di fosforo centrale.
D: Quale parola o frase di due parole descrive meglio la forma del tribromuro di fosforo?
R: La forma del bromuro di fosforo (III) è meglio descritta come piramidale trigonale.
D: Quanti elettroni di valenza ci sono nella molecola del tribromuro di fosforo, PBr3?
R: Il bromuro di fosforo (III) (PBr3) ha 26 elettroni di valenza.
D: Il tribromuro di fosforo è ionico o covalente?
R: Il bromuro di fosforo(III) (PBr3) è un composto covalente.
D: Qual è la formula chimica del tribromuro di fosforo?
R: La formula chimica del bromuro di fosforo (III) è PBr3.
D: Struttura di Lewis per il tribromuro di fosforo, PBr3?
R: La struttura di Lewis di PBr3 mostra il fosforo come atomo centrale circondato da tre atomi di bromo legati, ciascuno collegato da un singolo legame.
D: PBr3 è un’inversione?
R: No, il bromuro di fosforo(III) (PBr3) non presenta inversione.
D: PBr3 è un elettrofilo?
R: Sì, PBr3 può agire come un elettrofilo in alcune reazioni, dove accetta elettroni.
D: Qual è la geometria molecolare di PBr3?
R: La geometria molecolare di PBr3 è trigonale piramidale.
D: PBr3 è polare o non polare?
R: PBr3 è una molecola polare a causa della distribuzione non uniforme della densità elettronica causata dalla presenza di legami polari P-Br.
D: Quante moli di PBr3 contengono 3,68 × 10 ^ 25 atomi di bromo?
R: Per determinare il numero di moli, abbiamo bisogno della massa molare di PBr3, quindi dividiamo il numero dato di atomi di bromo per il numero di Avogadro.
D: Qual è il nome corretto per PBr3?
R: Il nome corretto per PBr3 è bromuro di fosforo (III).
D: PBr3 è polare?
R: Sì, PBr3 è una molecola polare a causa della presenza di legami polari e di una distribuzione non uniforme della densità elettronica.
