Il toluene è un liquido incolore con un odore dolce e pungente. È ampiamente utilizzato come solvente, nonché nella produzione di prodotti chimici, coloranti e prodotti farmaceutici. Può essere dannoso se ingerito o inalato in grandi quantità.
| Nome IUPAC | Metilbenzene |
| Formula molecolare | C7H8 |
| numero CAS | 108-88-3 |
| Sinonimi | Toluolo, fenilmetano, metilbenzene, tolu-sol, toluene, metilbenzene, olio di toluolo, anisen, antisale 1A, benzene, metile, mono-metilbenzene |
| InChI | InChI=1S/C7H8/c1-7-5-3-2-4-6-7/h2-6H,1H3 |
Proprietà del toluene
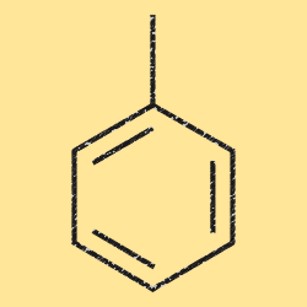
Struttura del toluene
Il toluene ha una struttura chimica semplice, costituita da un anello benzenico a cui è attaccato un singolo gruppo metilico. La molecola è planare e ha un legame elettronico pi delocalizzato. Questa struttura unica rende il toluene una materia prima utile nella produzione di vari prodotti chimici, come benzene e xilene, nonché nella sintesi di prodotti farmaceutici, coloranti e polimeri.
Formula del toluene
La formula chimica del toluene è C7H8, che rappresenta il numero e il tipo di atomi presenti nella molecola. Questa formula è importante in varie applicazioni industriali perché può aiutare a prevedere le proprietà fisiche e chimiche del composto, come il punto di fusione, il punto di ebollizione e la reattività in diverse reazioni chimiche.
Densità del toluene g/ml
La densità del toluene è di circa 0,87 grammi per millilitro a temperatura e pressione standard. Questa densità relativamente bassa è dovuta alla bassa massa molare e alle piccole dimensioni molecolari del toluene. La densità del toluene è importante in molti processi industriali perché può influenzare la solubilità e la reattività del composto in varie reazioni chimiche.
Massa molare del toluene
Il toluene, con la formula molecolare C7H8, ha una massa molare di circa 92,14 grammi per mole. Questo valore può essere ottenuto sommando le masse atomiche degli atomi che costituiscono la molecola. La massa molare relativamente bassa del toluene lo rende un composto volatile e molto mobile, che contribuisce al suo utilizzo come solvente in vari processi industriali.
Punto di ebollizione del toluene
Il toluene ha un punto di ebollizione di circa 110,6 gradi Celsius alla pressione atmosferica standard. Questo punto di ebollizione relativamente basso lo rende facile da evaporare e da utilizzare come solvente in una varietà di applicazioni industriali, incluso come diluente in vernici e rivestimenti e nella produzione di fibre sintetiche e gomma.
Punto di fusione del toluene
Il punto di fusione del toluene è di circa -95 gradi Celsius. Ciò lo rende un liquido a temperatura e pressione standard, ma può essere facilmente solidificato raffreddandolo al di sotto del punto di fusione. Il basso punto di fusione del toluene è dovuto alle deboli forze di attrazione intermolecolari tra le sue molecole, che sono principalmente forze di Van der Waals.
Peso molecolare del toluene
Il peso molecolare del toluene è 92,14 grammi per mole, calcolato sommando le masse atomiche degli atomi nella molecola. Questo valore è importante in varie applicazioni industriali perché può influenzare le proprietà fisiche e chimiche del composto, inclusi il punto di ebollizione, il punto di fusione e la solubilità in diversi solventi.
| Aspetto | Liquido incolore |
| Peso specifico | 0,866 |
| Colore | Incolore |
| Odore | Dolce, piccante |
| Massa molare | 92,14 g/mole |
| Densità | 0,87 g/ml a 25°C |
| Punto di fusione | -95°C |
| Punto di ebollizione | 110,6°C |
| Punto flash | 4,4°C |
| solubilità in acqua | 0,052 g/100 ml a 25°C |
| Solubilità | Solubile in solventi organici |
| Pressione del vapore | 22 mmHg a 25°C |
| Densità del vapore | 3.1 (aria = 1) |
| pKa | 44 |
| pH | Non applicabile |
Nota: alcuni valori possono variare a seconda della sorgente e delle condizioni di misurazione.
Sicurezza e pericoli del toluene
Il metilbenzene può comportare diversi rischi per la sicurezza se maneggiato in modo errato. È infiammabile e può formare miscele esplosive con l’aria, quindi va tenuto lontano da fonti di calore, scintille e fiamme. L’inalazione di vapori di metilbenzene può causare irritazione del sistema respiratorio, mal di testa, vertigini e sonnolenza e l’esposizione cronica può provocare cambiamenti neurologici e comportamentali. Il contatto prolungato o ripetuto con la pelle può provocare dermatiti. È stato dimostrato anche che il metilbenzene ha effetti sulla riproduzione e sullo sviluppo degli animali ed è classificato come cancerogeno di categoria 2. Quando si maneggia il metilbenzene è necessario utilizzare dispositivi di protezione e ventilazione adeguati per ridurre al minimo i danni. esposizione ai suoi effetti pericolosi.
| Simboli di pericolo | Xn, F |
| Descrizione della sicurezza | Tenere lontano da fonti di calore/scintille/fiamme libere/superfici calde. Utilizzare apparecchiature elettriche/di ventilazione/illuminazione a prova di esplosione. Tieni il contenitore chiuso ermeticamente. Non respirare i vapori. Indossare guanti/indumenti protettivi/proteggere gli occhi/il viso. |
| Numeri di identificazione delle Nazioni Unite | ONU 1294 |
| Codice SA | 2902.2 |
| Classe di pericolo | 3 |
| Gruppo di imballaggio | II |
| Tossicità | Il metilbenzene può causare irritazione agli occhi, al naso e alla gola, nonché mal di testa, vertigini e sonnolenza. L’esposizione cronica può portare a cambiamenti neurologici e comportamentali. Il contatto prolungato o ripetuto con la pelle può provocare secchezza, screpolature e dermatiti. È stato dimostrato che il metilbenzene ha effetti sulla riproduzione e sullo sviluppo degli animali. È classificato come cancerogeno di categoria 2 dall’Agenzia internazionale per la ricerca sul cancro (IARC). Quando si maneggia il metilbenzene è necessario utilizzare dispositivi di protezione e ventilazione adeguati per ridurre al minimo l’esposizione. |
Metodi di sintesi del toluene
L’industria chimica produce tipicamente metilbenzene mediante una serie di metodi di sintesi, tra cui il reforming catalitico della nafta, il cracking catalitico delle frazioni di petrolio greggio e la sproporzione del metilbenzene.
Il reforming catalitico della nafta è uno dei metodi più comunemente utilizzati per produrre metilbenzene perché produce una miscela di idrocarburi aromatici che possono essere separati e purificati. Il processo prevede la reazione della nafta con un catalizzatore in presenza di idrogeno, che produce una miscela di composti aromatici compreso il metilbenzene.
Il cracking catalitico delle frazioni di petrolio greggio può anche produrre metilbenzene, così come altri idrocarburi aromatici e non aromatici. Questo processo prevede la reazione di frazioni di petrolio greggio ad alto punto di ebollizione con un catalizzatore ad alta temperatura e pressione. Questo scompone le molecole in frammenti più piccoli che possono essere separati e purificati.
La disproporzione del metilbenzene è un processo che converte il metilbenzene in una miscela di benzene e xileni. La reazione viene tipicamente condotta a temperatura e pressione elevate in presenza di un catalizzatore e può essere utilizzata per produrre benzene e xileni di elevata purezza da utilizzare in varie applicazioni industriali.
Usi del toluene
Il metilbenzene ha vari usi industriali e commerciali, grazie alle sue proprietà uniche come liquido volatile, incolore con un odore distinto. Alcune delle sue principali applicazioni includono:
- I produttori di solventi utilizzano ampiamente il toluene come solvente nella produzione di vernici, rivestimenti, adesivi e altri prodotti. È apprezzato per la sua capacità di dissolvere un’ampia gamma di composti organici, nonché per la sua tossicità relativamente bassa e l’elevato tasso di evaporazione.
- Il toluene migliora le prestazioni e l’efficienza dei motori a combustione interna, motivo per cui viene utilizzato come componente ad alto numero di ottano nella benzina.
- I produttori utilizzano il toluene come intermedio chiave nella produzione di vari prodotti chimici, tra cui benzene, xilene e vari altri composti aromatici. Queste sostanze chimiche vengono utilizzate nella produzione di plastica, fibre sintetiche, gomma e altri materiali.
- Alcune applicazioni mediche e farmaceutiche utilizzano il toluene, anche come componente di alcuni farmaci topici e come solvente per alcuni composti medici.
- I ricercatori utilizzano il toluene come solvente e reagente in varie applicazioni di ricerca di laboratorio, grazie alla sua capacità di dissolversi e reagire con un’ampia gamma di composti organici.
Domande:
Toluene ad alcool benzilico
Un processo in più fasi realizza la conversione del metilbenzene in alcol benzilico. Un approccio comune prevede i seguenti passaggi:
- Ossidazione del metilbenzene a benzil cloruro: il metilbenzene può essere ossidato a benzil cloruro utilizzando cloro gassoso e un catalizzatore come cloruro di ferro o alluminio. Questa reazione comporta la sostituzione di un atomo di idrogeno sul gruppo metilico del metilbenzene con un atomo di cloro.
- Idrolisi del cloruro di benzile in alcool benzilico: il cloruro di benzile può essere idrolizzato in alcool benzilico utilizzando una soluzione acquosa di idrossido di sodio. Questa reazione comporta la sostituzione del gruppo cloruro del cloruro di benzile con un gruppo ossidrile.
- Purificazione dell’alcol benzilico: l’alcol benzilico risultante può essere purificato mediante distillazione o altri metodi per rimuovere tutte le impurità.
Toluene a benzaldeide
La conversione del metilbenzene in benzaldeide può essere ottenuta attraverso un processo a più fasi. Un approccio comune prevede i seguenti passaggi:
- Ossidazione del metilbenzene in alcol benzilico: il metilbenzene può essere ossidato in alcol benzilico utilizzando un agente ossidante come il permanganato di potassio o l’acido cromico. Questa reazione comporta la sostituzione di un atomo di idrogeno sul gruppo metilico del metilbenzene con un gruppo ossidrile per formare alcol benzilico.
- Ossidazione dell’alcol benzilico in benzaldeide: l’alcol benzilico può essere ulteriormente ossidato in benzaldeide utilizzando un agente ossidante come il permanganato di potassio o il clorito di sodio. Questa reazione comporta la rimozione del gruppo ossidrile sull’alcol benzilico per formare un gruppo carbonilico sulla benzaldeide.
- Purificazione della benzaldeide: la benzaldeide risultante può essere purificata mediante distillazione o altri metodi per rimuovere tutte le impurità.
