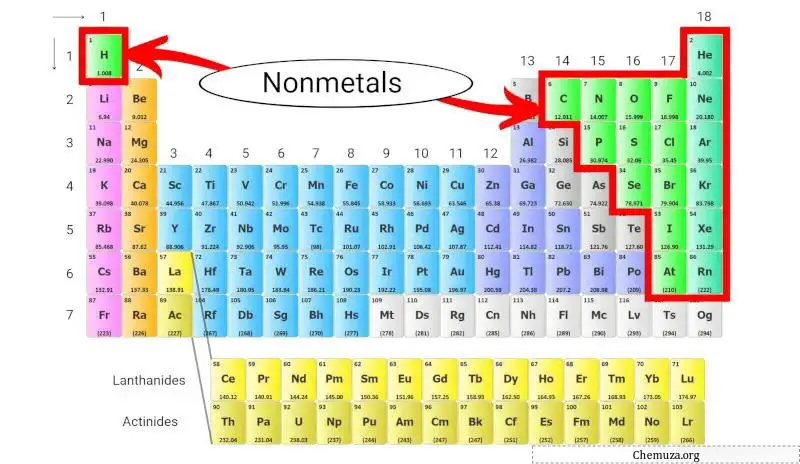
I non metalli sono un gruppo di elementi che non hanno le proprietà dei metalli, come l’elevata conduttività elettrica e la lucentezza. Questi non metalli si trovano sul lato destro della tavola periodica , ad eccezione dell’idrogeno .
I non metalli possono essere trovati in una varietà di forme, inclusi gas come ossigeno e cloro , liquidi come bromo e solidi come zolfo e carbonio . [1]
Vediamo cose più importanti sui non metalli.
Cosa sono esattamente i non metalli?
I non metalli sono elementi che tendono ad acquisire elettroni durante le reazioni chimiche, formando ioni o anioni caricati negativamente.
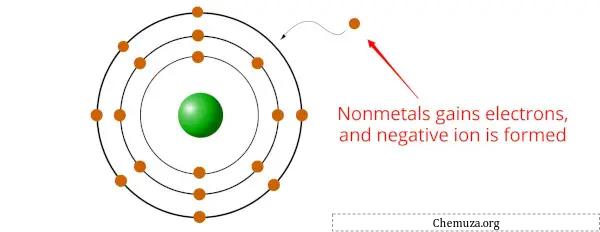
Questo perché i non metalli generalmente hanno un’elettronegatività maggiore rispetto ai metalli, [2] il che significa che hanno una maggiore attrazione per gli elettroni.
Quando i non metalli si legano ai metalli , l’elemento non metallico guadagna uno o più elettroni dal metallo per formare un composto stabile.
Ad esempio, il cloro acquista un elettrone dal sodio per formare il composto ionico cloruro di sodio (NaCl).
Si può anche dire che – I non metalli sono un gruppo di elementi chimici che non hanno le proprietà fisiche e chimiche dei metalli.
Bene, vediamo l’elenco dei non metalli presenti nella tavola periodica.
Elenco dei non metalli presenti nella tavola periodica
Ecco un elenco dei non metalli presenti nella tavola periodica:
- Idrogeno (H)
- Elio (Lui)
- Carbonio (C)
- Azoto (N)
- Ossigeno (O)
- Fluorite (F)
- Neon (Ne)
- Fosforo (P)
- Zolfo (S)
- Cloro (Cl)
- Argon (Ar)
- Selenio (Se)
- Bromo (Br)
- Kripton (Kr)
- Iodio (I)
- Xeno (Xe)
- Astato (At)
- Radon (Rn)
Questi non metalli si trovano sul lato destro della tavola periodica, ad eccezione dell’idrogeno, che si trova nella parte superiore della tavola periodica sopra i metalli alcalini .
Stato dei non metalli (solido, liquido o gassoso?)
I non metalli possono esistere in tutti e tre gli stati della materia: solido, liquido e gassoso.
Lo stato di un non metallo dipende dalle condizioni di temperatura e pressione a cui è esposto.
Tra tutti i non metalli della tavola periodica;
- 11 non metalli sono allo stato gassoso a temperatura ambiente. [3]
- Il bromo (Br) è un non metallo che si trova allo stato liquido a temperatura ambiente.
- Il resto dei non metalli sono solidi a temperatura ambiente.
Il non metallo più reattivo
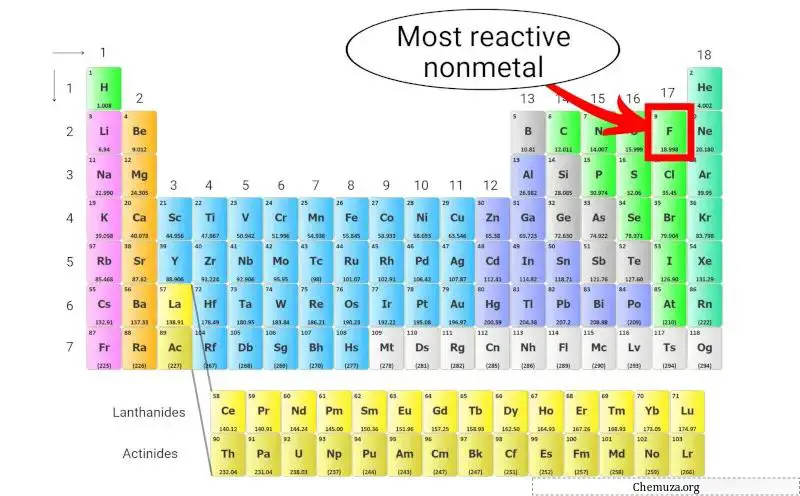
Il fluoro (F) è il non metallo più reattivo presente nella tavola periodica.
Ma perché? Perché il fluoro è il più reattivo?
Questo perché ha la più alta elettronegatività tra tutti gli elementi, il che significa che ha una forte attrazione per gli elettroni.
Il fluoro ha sette elettroni nel suo livello energetico più esterno e richiede un elettrone aggiuntivo per riempire il suo guscio di valenza e raggiungere una configurazione stabile.
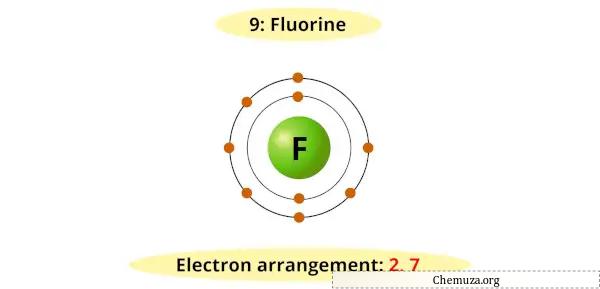
Pertanto, accetta prontamente un elettrone da altri elementi per formare uno ione fluoruro (F-).
A causa della sua elevata reattività, il fluoro può reagire in modo esplosivo con molti altri elementi e composti, tra cui acqua, metalli e persino vetro. [4]
Il fluoro è così reattivo che viene generalmente immagazzinato e trasportato in contenitori specializzati realizzati con materiali resistenti alle sue proprietà corrosive.
Ruolo dei non metalli nelle applicazioni ambientali e industriali
I non metalli sono utilizzati in vari processi industriali e applicazioni ambientali grazie alle loro proprietà uniche. Ecco alcuni esempi:
- Controllo dell’inquinamento atmosferico: i non metalli come l’azoto e l’ossigeno svolgono un ruolo vitale nel controllo dell’inquinamento atmosferico. Gli ossidi di azoto (NOx) sono inquinanti nocivi rilasciati dai veicoli e dai processi industriali. I catalizzatori non metallici vengono utilizzati per convertire gli NOx in gas innocui come azoto e acqua. Allo stesso modo, l’ossigeno viene utilizzato nei processi di combustione per ridurre le emissioni nocive.
- Fertilizzante: azoto, fosforo e zolfo sono nutrienti essenziali per la crescita delle piante. I fertilizzanti non metallici come il nitrato di ammonio e il superfosfato sono ampiamente utilizzati in agricoltura per aumentare i raccolti.
- Batterie: nelle batterie vengono utilizzati elementi non metallici come zolfo, carbonio e litio. Le batterie agli ioni di litio sono comunemente utilizzate nei dispositivi elettronici, nei veicoli elettrici e nei sistemi di energia rinnovabile.
- Purificazione dell’acqua: i non metalli come cloro e iodio sono comunemente usati come disinfettanti nei sistemi di purificazione dell’acqua. Uccidono batteri e virus dannosi e rendono l’acqua sicura da bere. [5]
- Produzione chimica: i non metalli come lo zolfo e il cloro sono ampiamente utilizzati nella produzione di prodotti chimici come acido solforico, acido cloridrico e solventi a base di cloro.
Riepilogo
I non metalli non hanno le proprietà dei metalli come l’elevata conduttività elettrica e la lucentezza e si trovano sul lato destro della tavola periodica, ad eccezione dell’idrogeno. Esistono in tutti e tre gli stati della materia a seconda delle condizioni di temperatura e pressione.
Il fluoro è il non metallo più reattivo a causa della sua elevata elettronegatività e accetta facilmente un elettrone da altri elementi per formare uno ione fluoruro (F-).
I non metalli hanno diversi usi in applicazioni ambientali e industriali, tra cui il controllo dell’inquinamento atmosferico, i fertilizzanti, le batterie, la purificazione dell’acqua e la produzione chimica.
