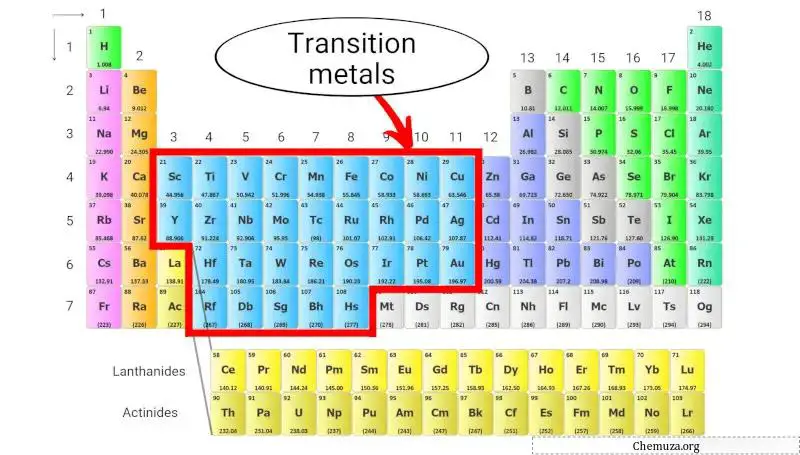
I metalli di transizione sono un gruppo di elementi metallici che si trovano al centro della tavola periodica , in particolare i gruppi da 3 a 11. [1]
Hanno anche orbitali D parzialmente riempiti, consentendo loro di formare facilmente composti complessi e di esibire un’ampia gamma di stati di ossidazione .
Esploriamo di più sui metalli di transizione della tavola periodica.
Cosa sono i metalli di transizione?
Gli elementi di transizione (o metalli di transizione) sono quegli elementi che si sono parzialmente riempiti di orbitali, sia nella loro forma elementare (M) che nei loro stati di ossidazione più comuni (M+, M2 + , M3 ) . + , ecc. ).
Lasciatemelo spiegare in parole semplici con esempi.
Innanzitutto lo stato elementare è così: M;
E lo stato di ossidazione più comune può essere così: M + , M 2+ , M 3+ , ecc.
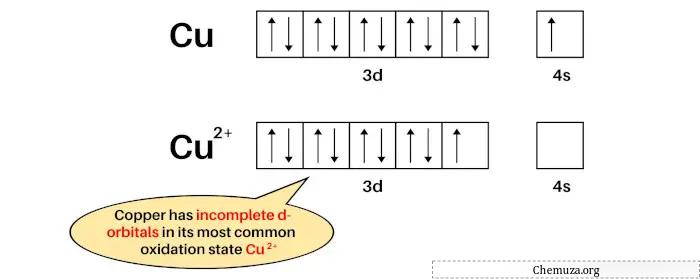
Esempio 1: Rame
La configurazione elettronica del Cu è: [Ar] 3d 10 4s 1 e
La configurazione elettronica di Cu 2+ è: [Ar] 3d 9 .
Il rame è un metallo di transizione perché nel suo stato di ossidazione più comune (Cu 2+ ) ha gli orbitali D parzialmente riempiti.
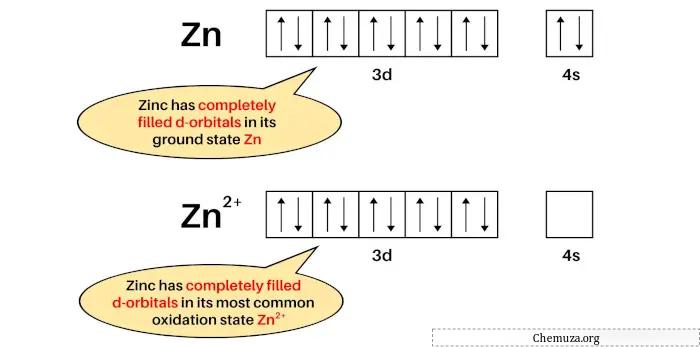
Esempio 2: zinco
La configurazione elettronica di Zn è: [Ar] 3d 10 4s 2 e
La configurazione elettronica di Zn 2+ è: [Ar] 3d 10 .
Lo zinco non è un metallo di transizione perché il suo stato fondamentale (Zn) e il suo stato di ossidazione più comune (Zn 2+ ) hanno orbitali D riempiti completamente.
Perché i metalli di transizione si chiamano così?
I metalli di transizione sono così chiamati perché le loro proprietà riflettono una transizione dalla loro natura metallica a quella non metallica mentre ci si sposta da sinistra a destra sulla tavola periodica.
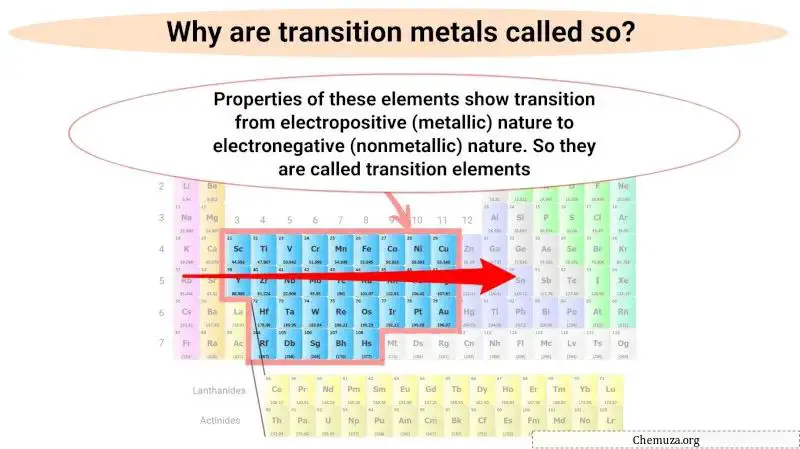
Questa transizione graduale dal comportamento metallico a quello non metallico è dovuta al cambiamento della configurazione elettronica degli elementi mentre ci si sposta da sinistra a destra attraverso il blocco.
Gli orbitali D svolgono un ruolo chiave in questa transizione, poiché possono partecipare ai legami chimici in vari modi, portando alla formazione di ioni e composti complessi.
Fatti sui metalli di transizione
Ecco alcuni fatti sui metalli di transizione.
- I metalli di transizione si trovano al centro della tavola periodica, riflettendo le loro proprietà elettroniche e chimiche uniche.
- Alcuni metalli di transizione hanno più stati di ossidazione , il che significa che possono formare ioni con cariche diverse a seconda delle condizioni di reazione.
- Alcuni metalli di transizione sono ottimi conduttori di calore ed elettricità, il che li rende importanti in molte applicazioni industriali.
- I metalli di transizione hanno un’ampia gamma di stati di ossidazione, consentendo loro di formare una varietà di composti con proprietà chimiche diverse.
- I metalli di transizione includono alcuni dei metalli più preziosi, come oro , argento e platino , che hanno importanti applicazioni in gioielleria, valute e industria.
Usi dei metalli di transizione
Ecco gli usi di alcuni metalli di transizione.
- Il ferro viene utilizzato per produrre l’acciaio, che viene utilizzato nell’edilizia, nei trasporti e in molti altri settori.
- Il rame viene utilizzato nei cavi elettrici, negli impianti idraulici e in altre applicazioni che richiedono una buona conduttività.
- Il titanio è utilizzato in applicazioni aerospaziali e militari, nonché in impianti medici, grazie alla sua robustezza, leggerezza e resistenza alla corrosione.
- Il nichel è utilizzato nell’acciaio inossidabile e in altre leghe, nonché nelle batterie e nella galvanica.
- L’argento viene utilizzato in gioielleria, monete e altri oggetti decorativi, nonché nell’elettronica, nei pannelli solari e nei prodotti antibatterici.
- L’oro viene utilizzato in gioielleria, valuta e altri oggetti decorativi, nonché nell’elettronica, nell’aerospaziale e nella medicina.
- Il platino viene utilizzato nei convertitori catalitici , nei gioielli e in altre applicazioni industriali per la sua resistenza alla corrosione e la capacità di catalizzare le reazioni.
- Il manganese viene utilizzato nella produzione dell’acciaio, nelle batterie e in altre applicazioni che richiedono metalli resistenti e leggeri.
- Il cobalto viene utilizzato nei magneti , nelle batterie e in altre applicazioni che richiedono materiali resistenti e durevoli.
Riepilogo
I metalli di transizione sono un gruppo di elementi metallici che si trovano al centro della tavola periodica con orbitali D parzialmente riempiti che consentono loro di formare facilmente composti complessi e di esibire un’ampia gamma di stati di ossidazione.
Le loro proprietà riflettono una transizione nella loro natura da metallica a non metallica mentre ci si sposta da sinistra a destra nella tavola periodica. Alcuni metalli di transizione hanno più stati di ossidazione e sono ottimi conduttori di calore ed elettricità.
Includono metalli preziosi e preziosi come oro, argento e platino. I metalli di transizione sono utilizzati in varie applicazioni come l’edilizia, i trasporti, i cavi elettrici, gli impianti idraulici, l’aerospaziale, la medicina e i convertitori catalitici industriali.
