Quindi hai già visto l’immagine qui sopra, giusto?
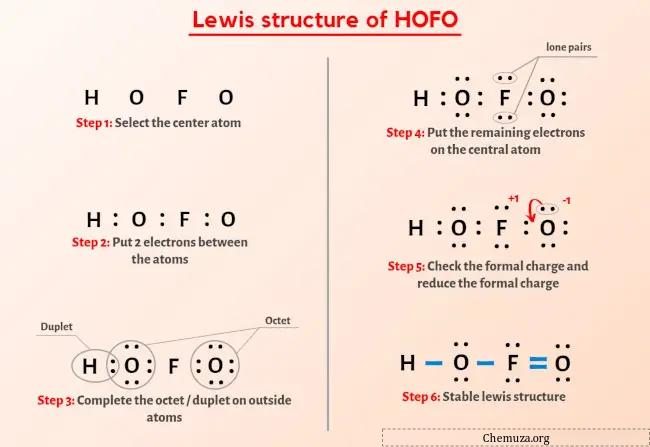
Lasciatemi spiegare brevemente l’immagine sopra.
La struttura HOFO Lewis ha un atomo di fluoro (F) al centro circondato da un atomo di ossigeno (O) e un gruppo OH. C’è 1 doppio legame tra l’atomo di fluoro (F) e l’atomo di ossigeno (O) e il resto degli altri atomi hanno un legame singolo.
Se non hai capito nulla dall’immagine sopra della struttura HOFO Lewis, resta con me e otterrai la spiegazione dettagliata passo passo su come disegnare una struttura HOFO Lewis.
Passiamo quindi ai passaggi per disegnare la struttura di Lewis di HOFO.
Passaggi di disegno della struttura HOFO Lewis
Passaggio 1: trovare il numero totale di elettroni di valenza nella molecola HOFO
Per trovare il numero totale di elettroni di valenza in una molecola HOFO, è necessario prima conoscere gli elettroni di valenza presenti nell’atomo di idrogeno, nell’atomo di fluoro e nell’atomo di ossigeno.
(Gli elettroni di valenza sono gli elettroni presenti nell’orbita più esterna di qualsiasi atomo.)
Qui ti dirò come trovare facilmente gli elettroni di valenza dell’idrogeno, del fluoro e dell’ossigeno utilizzando una tavola periodica.
Elettroni di valenza totali nella molecola HOFO
→ Elettroni di valenza dati dall’atomo di idrogeno:
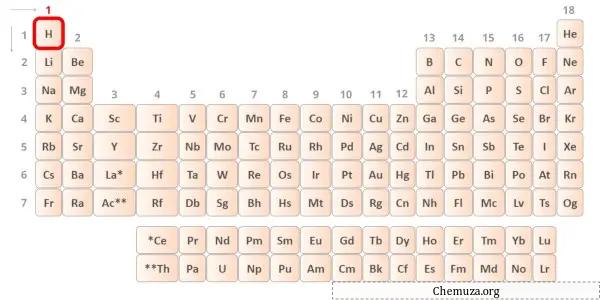
L’idrogeno è un elemento del gruppo 1 della tavola periodica. [1] Pertanto, l’elettrone di valenza presente nell’idrogeno è 1 .

Puoi vedere che nell’atomo di idrogeno è presente un solo elettrone di valenza, come mostrato nell’immagine sopra.
→ Elettroni di valenza dati dall’atomo di ossigeno:

L’ossigeno è un elemento del gruppo 16 della tavola periodica. [2] Pertanto, gli elettroni di valenza presenti nell’ossigeno sono 6 .
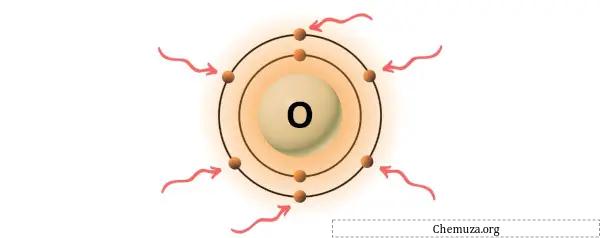
Puoi vedere i 6 elettroni di valenza presenti nell’atomo di ossigeno come mostrato nell’immagine sopra.
→ Elettroni di valenza dati dall’atomo di fluoro:
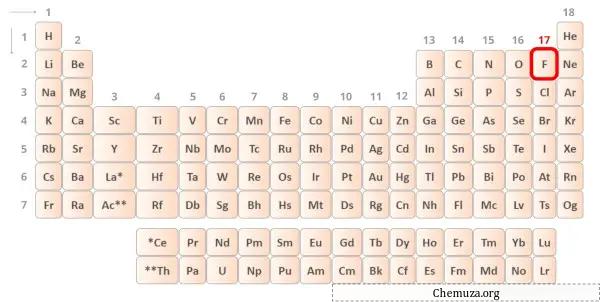
La fluorite è un elemento del gruppo 17 della tavola periodica. [3] Pertanto, l’elettrone di valenza presente nella fluorite è 7 .
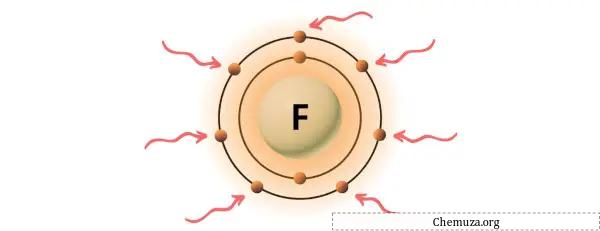
Puoi vedere i 7 elettroni di valenza presenti nell’atomo di fluoro come mostrato nell’immagine sopra.
COSÌ,
Elettroni di valenza totali nella molecola HOFO = elettroni di valenza donati da 1 atomo di idrogeno + elettroni di valenza donati da 1 atomo di fluoro + elettroni di valenza donati da 2 atomi di ossigeno = 1 + 7 + 6(2) = 26 .
Passaggio 2: seleziona l’atomo centrale
Per selezionare l’atomo centrale dobbiamo ricordare che al centro rimane l’atomo meno elettronegativo .
(Ricorda: se nella molecola data è presente idrogeno, metti sempre l’idrogeno all’esterno.)
Ora qui la molecola data è HOFO e contiene un atomo di idrogeno (H), un atomo di fluoro (F) e atomi di ossigeno (O).
Quindi secondo la regola dobbiamo tenere fuori l’idrogeno.
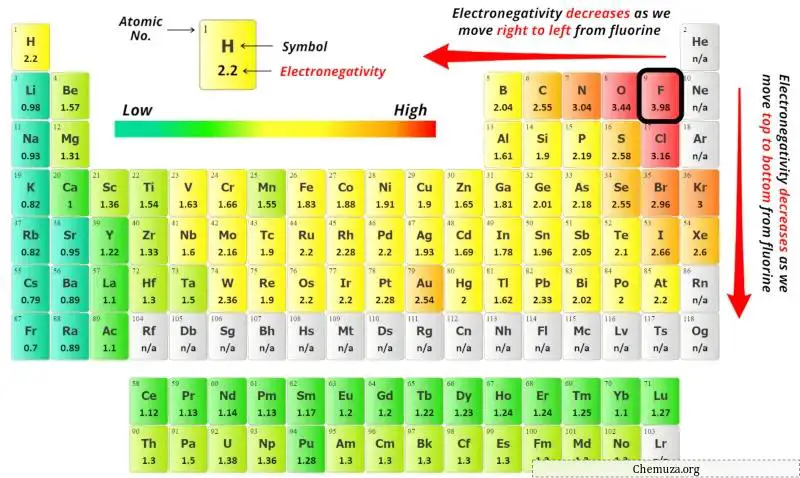
Ora puoi vedere i valori di elettronegatività dell’atomo di fluoro (F) e dell’atomo di ossigeno (O) nella tavola periodica qui sopra.
Se confrontiamo i valori di elettronegatività del fluoro (F) e dell’ossigeno (O), allora l’ atomo di fluoro è meno elettronegativo .
Qui, l’atomo di fluoro (F) è l’atomo centrale e gli atomi di ossigeno (O) sono l’atomo esterno.

Passaggio 3: collega ciascun atomo posizionando una coppia di elettroni tra di loro
Ora, nella molecola HOFO, è necessario posizionare le coppie di elettroni tra gli atomi di ossigeno (O) e idrogeno (H) e tra gli atomi di ossigeno (O) e fluoro (F).

Ciò indica che questi atomi sono legati chimicamente tra loro in una molecola HOFO.
Passaggio 4: rendere stabili gli atomi esterni
In questo passaggio è necessario verificare la stabilità degli atomi esterni.
Qui nello schizzo della molecola HOFO puoi vedere che gli atomi esterni sono atomi di idrogeno e ossigeno.
Questi atomi di idrogeno e ossigeno formano rispettivamente un dupletto e un ottetto e sono quindi stabili.
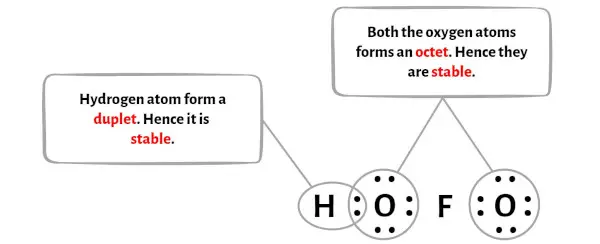
Inoltre, nel passaggio 1, abbiamo calcolato il numero totale di elettroni di valenza presenti nella molecola HOFO.
La molecola HOFO ha un totale di 20 elettroni di valenza e di questi, solo 16 elettroni di valenza vengono utilizzati nel diagramma sopra.
Quindi il numero di elettroni rimanenti = 20 – 16 = 4 .
Devi mettere questi 4 elettroni sugli atomi di fluoro nello schizzo sopra della molecola HOFO.
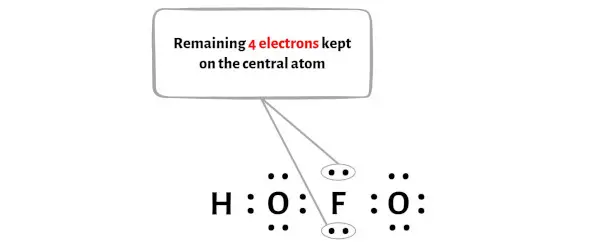
Ora passiamo al passaggio successivo.
Passaggio 5: controlla l’ottetto sull’atomo centrale
In questo passaggio, è necessario verificare se l’atomo centrale del fluoro (F) è stabile o meno.
Per verificare la stabilità dell’atomo centrale del fluoro (F), dobbiamo verificare se forma un ottetto o meno.
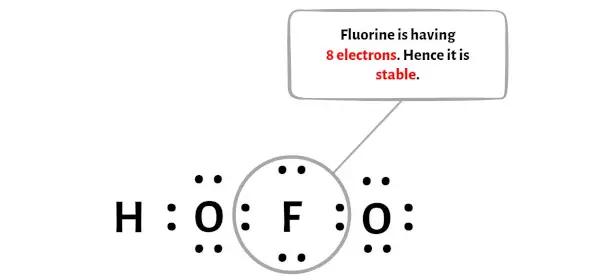
Nell’immagine sopra puoi vedere che l’atomo di fluoro forma un ottetto. Ciò significa che ha 8 elettroni.
E quindi l’atomo centrale del fluoro è stabile.
Passiamo ora all’ultimo passaggio per verificare se la struttura di Lewis di HOFO è stabile o meno.
Passaggio 6: verificare la stabilità della struttura di Lewis
Ora sei arrivato all’ultimo passaggio in cui devi verificare la stabilità della struttura di Lewis di HOFO.
La stabilità della struttura di Lewis può essere verificata utilizzando un concetto formale di carica .
In breve, dobbiamo ora trovare la carica formale sugli atomi di idrogeno (H), fluoro (F) e ossigeno (O) presenti nella molecola HOFO.
Per calcolare l’imposta formale, è necessario utilizzare la seguente formula:
Carica formale = Elettroni di valenza – (Elettroni di legame)/2 – Elettroni non di legame
Puoi vedere il numero di elettroni di legame e di elettroni non di legame per ciascun atomo della molecola HOFO nell’immagine qui sotto.
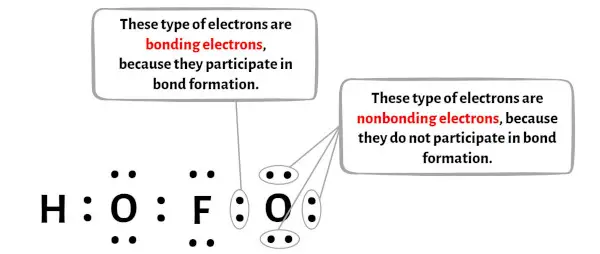
Per l’atomo di idrogeno (H):
Elettrone di valenza = 1 (perché l’idrogeno è nel gruppo 1)
Elettroni di legame = 2
Elettroni non leganti = 0
Per l’atomo di fluoro (F):
Elettroni di valenza = 7 (perché la fluorite è nel gruppo 17)
Elettroni di legame = 4
Elettroni non leganti = 4
Per l’atomo di ossigeno (O):
Elettroni di valenza = 6 (perché l’ossigeno è nel gruppo 16)
Elettroni di legame = 2
Elettroni non leganti = 6
Per l’atomo di ossigeno (O) (dal gruppo OH):
Elettroni di valenza = 6 (perché l’ossigeno è nel gruppo 16)
Elettroni di legame = 4
Elettroni non leganti = 4
| Accusa formale | = | elettroni di valenza | – | (Elettroni leganti)/2 | – | Elettroni non leganti | ||
| H | = | 1 | – | 2/2 | – | 0 | = | 0 |
| F | = | 7 | – | 4/2 | – | 4 | = | +1 |
| OH | = | 6 | – | 2/2 | – | 6 | = | -1 |
| O (dal gruppo OH) | = | 6 | – | 4/2 | – | 4 | = | 0 |
Dai calcoli formali sulla carica di cui sopra, puoi vedere che l’atomo di fluoro (F) ha una carica di +1 e l’atomo di ossigeno esterno (O) ha una carica di -1 .
Per questo motivo, la struttura di Lewis dell’HOFO ottenuta sopra non è stabile.
Queste cariche devono quindi essere minimizzate spostando la coppia elettronica verso l’atomo di fluoro.

Dopo aver spostato le coppie di elettroni dagli atomi di ossigeno all’atomo di fluoro, la struttura di Lewis di HOFO diventa più stabile.

Nella struttura a punti di Lewis di HOFO sopra, puoi anche rappresentare ciascuna coppia di elettroni di legame (:) come un singolo legame (|). Ciò si tradurrà nella seguente struttura di Lewis di HOFO.
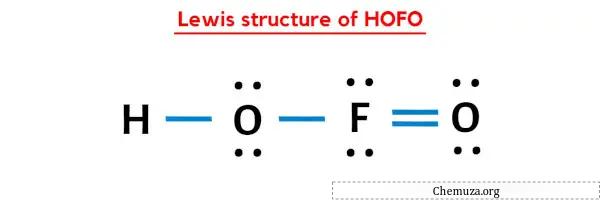
Spero che tu abbia compreso completamente tutti i passaggi precedenti.
Per fare più pratica e comprendere meglio, puoi provare altre strutture di Lewis elencate di seguito.
Prova (o almeno vedi) queste strutture di Lewis per una migliore comprensione:
