La sodio azide (NaN3) è un composto chimico. È altamente tossico ed esplosivo. Viene utilizzato negli airbag per generare rapidamente azoto da gonfiare in caso di impatto.
| Nome IUPAC | Sodio azide |
| Formula molecolare | NaN3 |
| numero CAS | 26628-22-8 |
| Sinonimi | Azio, sale sodico dell’acido idrazoico, trinitruro di sodio |
| InChI | InChI=1S/3HNO.Na/c1-4-2;2-1-3;/h3*1H;/q;;;+1/p-1 |
Proprietà della sodio azide
Formula di sodio azide
La formula della sodio azide è NaN3. È costituito da un atomo di sodio (Na) e tre atomi di azoto (N). L’atomo di sodio è carico positivamente, mentre gli atomi di azoto sono carichi negativamente. La formula rappresenta il rapporto tra atomi di sodio e di azoto nel composto.
Massa molare della sodio azide
La massa molare della sodioazide si calcola sommando le masse atomiche dei suoi costituenti. Il sodio ha una massa molare di 22,99 g/mol e l’azoto ha una massa molare di 14,01 g/mol. Poiché nella sodio azide ci sono tre atomi di azoto, moltiplichiamo la massa molare dell’azoto per tre. L’aggiunta di questi valori dà una massa molare di circa 65,01 g/mol per la sodioazide.
Punto di ebollizione della sodio azide
La sodioazide ha un punto di ebollizione elevato. Quando riscaldato, subisce la decomposizione anziché l’ebollizione. A temperature superiori a 275 gradi Celsius (527 gradi Fahrenheit), si decompone rapidamente in sodio metallico e azoto gassoso. Il suo punto di ebollizione non è quindi ben definito.
Sodio azide Punto di fusione
Il punto di fusione della sodioazide è relativamente basso rispetto al suo punto di ebollizione. Si scioglie a circa 275 gradi Celsius (527 gradi Fahrenheit). A questa temperatura il composto passa da solido a liquido. Tuttavia, è importante maneggiare la sodioazide con cautela a causa della sua natura tossica ed esplosiva.
Densità della sodio azide g/mL
La densità della sodioazide è solitamente espressa in grammi per millilitro (g/mL). La densità approssimativa della sodioazide solida è di circa 1,85 g/mL. Tuttavia, va notato che la densità può variare leggermente a seconda di fattori quali temperatura e pressione.
Peso molecolare della sodio azide
Il peso molecolare della sodioazide è la somma delle masse atomiche dei suoi elementi costitutivi. Come accennato in precedenza, la sodio azide è costituita da un atomo di sodio e tre atomi di azoto. Aggiungendo le masse atomiche di questi elementi si ottiene un peso molecolare di circa 65,01 grammi per mole (g/mol).
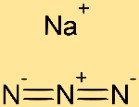
Struttura della sodio azide
La struttura della sodioazide è costituita dall’alternanza di cationi sodio (Na+) e anioni azide (N3-). Lo ione sodio è circondato da tre atomi di azoto, ciascuno dei quali condivide una coppia di elettroni con l’atomo di sodio. Questa disposizione crea una struttura reticolare cristallina stabile per la sodioazide.
Solubilità della sodio azide
La sodioazide è moderatamente solubile in acqua. Si dissolve in acqua per formare una soluzione limpida. La solubilità della sodioazide aumenta con temperature più elevate. Tuttavia, è importante maneggiare la soluzione con cura a causa della natura tossica ed esplosiva della sodioazide.
| Aspetto | Solido bianco |
| Peso specifico | 1,85 g/ml |
| Colore | Incolore |
| Odore | Inodore |
| Massa molare | 65,01 g/mole |
| Densità | 1,85 g/ml |
| Punto di fusione | 275°C |
| Punto di ebollizione | Decomposto |
| Punto flash | Non applicabile |
| solubilità in acqua | Moderatamente solubile |
| Solubilità | Solubile in solventi polari come l’ammoniaca |
| Pressione del vapore | Non applicabile |
| Densità del vapore | Non applicabile |
| pKa | Non applicabile |
| pH | Neutro |
Sicurezza e pericoli della sodio azide
La sodioazide presenta rischi significativi per la sicurezza e deve essere maneggiata con estrema cautela. È altamente tossico se ingerito, inalato o assorbito attraverso la pelle. L’esposizione alla sodioazide può causare gravi rischi per la salute, inclusi problemi respiratori, vertigini e persino la morte. Costituisce anche un potenziale pericolo di esplosione, in particolare se esposto a calore, urti o contatto con determinati metalli. Quando si lavora con sodio azide, le persone devono indossare adeguati dispositivi di protezione individuale, inclusi guanti e occhiali di sicurezza. È fondamentale conservare e maneggiare questo composto in aree ben ventilate, lontano da fonti di ignizione e sostanze incompatibili per ridurre al minimo il rischio di incidenti e garantire la sicurezza sul lavoro.
| Simboli di pericolo | Tossico, esplosivo |
| Descrizione della sicurezza | Maneggiare con estrema cautela. Sostanza tossica ed esplosiva. |
| Numeri di identificazione delle Nazioni Unite | UN1687 (per sodioazide, solidi tossici, inorganici, nas) |
| Codice SA | 28500090 |
| Classe di pericolo | 6.1 (Sostanze tossiche) |
| Gruppo di imballaggio | II (sostanza moderatamente pericolosa) |
| Tossicità | Molto tossico |
Metodi per la sintesi della sodio azide
Esistono alcuni metodi comuni per sintetizzare la sodioazide.
Un metodo prevede la reazione tra l’ammide di sodio (NaNH2) e l’acido idrazoico (HN3). In questo metodo, sciogliere l’ammide di sodio nell’ammoniaca liquida e quindi aggiungere lentamente l’acido idrazoico. La reazione ha luogo e porta alla formazione di sodio azide e cloruro di ammonio come sottoprodotti.
Un altro metodo di sintesi prevede la reazione tra nitrito di sodio (NaNO2) e sodio azide (NaN3). In una soluzione acquosa, la reazione controlla attentamente l’aggiunta di nitrito di sodio a una soluzione di sodio azide, portando alla formazione di sodio azide e nitrato di sodio.
Per sintetizzare la sodio azide, il cianuro di sodio (NaCN) può essere fatto reagire con il protossido di azoto (N2O) ad alta temperatura. Durante questa reazione, come sottoprodotti si formano sodio azide e sodio cianato.
Seguire sempre le opportune precauzioni di sicurezza per ridurre al minimo i rischi associati al processo di sintesi. Ciò include l’uso di dispositivi di protezione individuale e il rispetto dei protocolli di gestione.
Usi della sodio azide
La sodioazide ha diversi usi importanti in vari settori. Ecco alcune app degne di nota:
- Gonfiaggio degli airbag: la sodioazide è un componente chiave degli airbag delle automobili. Durante una collisione, una piccola quantità di sodio azide reagisce rapidamente per generare azoto gassoso, gonfiando l’airbag e proteggendo i passeggeri.
- Ricerca biochimica: i ricercatori utilizzano la sodioazide per inibire enzimi, come la citocromo ossidasi, facilitando lo studio dei processi cellulari e delle vie metaboliche.
- Conservazione dei campioni biologici: la sodioazide preserva i campioni biologici, come gli anticorpi, prevenendo la crescita batterica e mantenendone la stabilità.
- Innesco esplosivo: la sodioazide funge da esplosivo primario in alcuni dispositivi pirotecnici, detonatori e iniziatori esplosivi a causa della sua natura esplosiva.
- Sintesi chimica: la sodioazide agisce come precursore in varie reazioni chimiche, consentendo la sintesi di composti organici, prodotti farmaceutici e coloranti.
- Prevenzione della corrosione: le industrie utilizzano l’azoturo di sodio come inibitore della corrosione per proteggere le superfici metalliche dal degrado causato dall’ossidazione o dall’esposizione ad agenti corrosivi.
- Industria mineraria: la sodioazide aiuta a separare i minerali preziosi dalle sostanze indesiderate nelle operazioni minerarie come depressore nei processi di flottazione dei minerali.
- Industria dei polimeri: la sodioazide agisce come agente espandente nella produzione di schiume poliuretaniche, facilitando la formazione di bolle di gas che conferiscono alla schiuma la struttura desiderata.
- Chimica analitica: la sodioazide funge da reagente per varie analisi chimiche, tra cui spettrofotometria, gascromatografia e spettrometria di massa.
- Medicina veterinaria: in alcuni casi nella pratica veterinaria i veterinari utilizzano la sodioazide come agente di eutanasia per gli animali.
Queste applicazioni evidenziano le diverse utilità della sodioazide, ma è fondamentale maneggiare questo composto con cura e seguire i protocolli di sicurezza a causa della sua natura tossica ed esplosiva.
Domande
D: Come testare la sodio azide?
R: La sodioazide può essere testata utilizzando tecniche analitiche appropriate come spettroscopia, cromatografia o test di reattività chimica.
D: La sodio azide viene ancora utilizzata negli airbag?
R: Sì, la sodioazide è ancora utilizzata negli airbag come propellente per un rapido gonfiaggio in caso di impatto.
D: Quanti grammi di sodio azide sono necessari per produrre 30,5 g di azoto?
R: Per produrre 30,5 grammi di azoto sono necessari circa 34 grammi di sodio azide.
D: Dove acquistare sodio azide?
R: La sodioazide può essere acquistata da fornitori di prodotti chimici, fornitori di laboratorio o mercati chimici online.
D: Come si prepara una soluzione di sodio azide allo 0,01% in PBS?
R: Per preparare una soluzione di sodio azide allo 0,01% in PBS, sciogliere 0,01 grammi di sodio azide in 100 ml di soluzione salina tamponata con fosfato (PBS).
D: Qual è il ruolo della sodio azide negli esperimenti?
R: La sodioazide è comunemente usata come inibitore o conservante negli esperimenti destinati a inibire l’attività enzimatica o prevenire la crescita batterica.
D: Come posso eliminare la sodio azide da un campione?
R: La sodioazide può essere eliminata da un campione mediante lavaggio accurato o risciacquo con solventi appropriati oppure sottoponendolo a decomposizione ad alta temperatura.
D: In che modo la sodio azide influisce sull’ETC?
R: La sodioazide inibisce la catena di trasporto degli elettroni (ETC) nei mitocondri bloccando l’enzima citocromo ossidasi, interrompendo così il flusso di elettroni e la produzione di ATP.
D: Quanti grammi di sodio si formano quando reagiscono 93 grammi di sodio azide?
R: Quando reagiscono 93 grammi di sodio azide si formano 35,9 grammi di sodio.
D: La decomposizione esplosiva della sodio azide è un cambiamento fisico nell’attivazione dell’airbag?
R: No, la decomposizione esplosiva della sodio azide per gonfiare l’airbag di un’automobile è un cambiamento chimico.
D: Come preparare la sodio azide?
R: La sodioazide viene solitamente preparata mediante metodi di sintesi chimica che comportano reazioni tra precursori adatti, come l’ammide di sodio e l’acido idrazoico.
D: Quanto sodio azide è tossico?
R: La sodioazide è altamente tossica e anche piccole quantità, come pochi grammi, possono comportare rischi significativi per la salute se ingerita, inalata o assorbita attraverso la pelle.
D: A cosa serve la sodio azide?
R: La sodioazide viene utilizzata in una varietà di applicazioni tra cui il gonfiaggio degli airbag, la ricerca biochimica, la sintesi chimica e come conservante o inibitore nei campioni biologici.
D: La sodio azide reagisce con gli acidi?
R: Sì, la sodio azide può reagire con acidi, come l’acido cloridrico (HCl), formando gas tossici come l’idrogeno azide (HN3). È necessario adottare precauzioni adeguate quando si maneggia la sodioazide e gli acidi.
