L’ossido di fosforo (P2O5) è un composto chimico. È formato dalla combinazione di due atomi di fosforo e cinque atomi di ossigeno.
| Nome dell’IUPAC | Anidride fosforica |
| Formula molecolare | P2O5 |
| numero CAS | 1314-56-3 |
| Sinonimi | Anidride fosforica, ossido di fosforo (V), pentossido di difosforo |
| InChI | InChI=1S/2O.P2/c2*1-3-2 |
Proprietà dell’ossido di fosforo
Formula dell’ossido di fosforo
La formula dell’pentossido di difosforo è P2O5. È composto da due atomi di fosforo e cinque atomi di ossigeno. Questa formula chimica rappresenta il rapporto degli elementi nel composto.
Massa molare dell’ossido di fosforo
La massa molare dell’pentossido di difosforo (P2O5) si calcola sommando le masse atomiche dei suoi elementi costitutivi. Il fosforo ha una massa atomica di circa 31,0 grammi per mole, mentre l’ossigeno ha una massa atomica di circa 16,0 grammi per mole. La massa molare di P2O5 è quindi di circa 141,9 grammi per mole.
Punto di ebollizione dell’ossido di fosforo
L’pentossido di difosforo non ha un punto di ebollizione specifico. Subisce invece una reazione chimica quando viene riscaldato, trasformandosi in acido fosforico (H3PO4) e rilasciando calore nel processo. Pertanto non ha un punto di ebollizione ben definito come molti altri composti.
Punto di fusione dell’ossido di fosforo
L’pentossido di difosforo (P2O5) ha un punto di fusione di circa 340 gradi Celsius (644 gradi Fahrenheit). A questa temperatura il composto solido si trasforma nello stato liquido. È importante notare che il pentossido di difosforo è altamente igroscopico, il che significa che assorbe facilmente l’umidità dall’aria.
Densità dell’ossido di fosforo g/mL
La densità del pentossido di difosforo è di circa 2,39 grammi per millilitro (g/mL). La densità è una misura della massa per unità di volume e questo valore indica quanto è pesante o compatta la sostanza. La densità del pentossido di difosforo contribuisce alle sue proprietà fisiche e al suo comportamento in varie applicazioni.
Peso molecolare dell’ossido di fosforo
Il peso molecolare dell’pentossido di difosforo (P2O5) è di circa 141,9 grammi per mole. Questo valore rappresenta la somma delle masse atomiche di fosforo e ossigeno nel composto. Il peso molecolare viene spesso utilizzato nei calcoli che coinvolgono reazioni chimiche e la stechiometria dei composti.
Struttura dell’ossido di fosforo
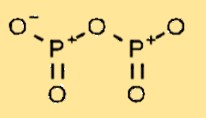
L’pentossido di difosforo ha una struttura molecolare costituita da due atomi di fosforo legati a cinque atomi di ossigeno. La disposizione degli atomi forma una struttura ciclica, con ciascun atomo di fosforo legato a due atomi di ossigeno e condividendo un doppio legame con l’atomo di fosforo vicino.
Solubilità dell’ossido di fosforo
Il pentossido di difosforo non è solubile in acqua. Reagisce vigorosamente con l’acqua per formare acido fosforico, liberando calore. Tuttavia, è solubile in alcuni solventi organici come il disolfuro di carbonio e il cloroformio. Le caratteristiche di solubilità del pentossido di difosforo giocano un ruolo nella sua reattività chimica e nelle sue applicazioni.
| Aspetto | Solido cristallino bianco |
| Peso specifico | 2,39 g/ml |
| Colore | Incolore |
| Odore | Inodore |
| Massa molare | 141,9 g/mole |
| Densità | 2,39 g/ml |
| Punto di fusione | 340°C (644°F) |
| Punto di ebollizione | Reagisce per formare acido fosforico |
| Punto flash | Non applicabile |
| solubilità in acqua | Reagisce con l’acqua per formare acido fosforico |
| Solubilità | Solubile in solventi organici come solfuro di carbonio, cloroformio |
| Pressione del vapore | Non applicabile |
| Densità del vapore | Non applicabile |
| pKa | Non applicabile |
| pH | Non applicabile |
Sicurezza e pericoli dell’ossido di fosforo
L’pentossido di difosforo (P2O5) comporta alcuni rischi per la sicurezza e occorre prestare attenzione quando lo si maneggia. Reagisce violentemente con l’acqua, liberando calore e formando acido fosforico, che può provocare ustioni e irritazioni alla pelle, agli occhi e alle vie respiratorie. È importante evitare il contatto con la sostanza e utilizzare dispositivi di protezione adeguati, come guanti, occhiali e un respiratore, quando si lavora con pentossido di difosforo. Inoltre, è fondamentale conservare il composto in un contenitore ermeticamente chiuso, lontano da umidità e materiali incompatibili. È necessario garantire una ventilazione adeguata per evitare l’accumulo di vapori.
| Simboli di pericolo | Corrosivo, nocivo |
| Descrizione della sicurezza | – Provoca gravi ustioni cutanee e gravi lesioni oculari – Può essere nocivo se ingerito o inalato – Reagisce violentemente con l’acqua – Tenere lontano dall’umidità e da materiali incompatibili |
| Numeri di identificazione delle Nazioni Unite | Un 1807 |
| Codice SA | 2819.10.90 |
| Classe di pericolo | Classe 8 (materie corrosive) |
| Gruppo di imballaggio | PG II (pericolo medio) |
| Tossicità | Tossico per gli organismi acquatici, può provocare effetti negativi a lungo termine nell’ambiente acquatico |
Metodi di sintesi dell’ossido di fosforo
Vari metodi possono essere utilizzati per sintetizzare il pentossido di difosforo (P2O5).
Un metodo comune prevede la combustione del fosforo in presenza di ossigeno in eccesso. Questa reazione produce pentossido di fosforo sotto forma di un residuo solido bianco. L’equazione per questo processo è P4 + 5O2 → 2P2O5.
Un altro metodo prevede l’ossidazione controllata dei composti del fosforo, come il tricloruro di fosforo (PCl3) o il tribromuro di fosforo (PBr3) , utilizzando ossigeno o aria. La reazione avviene solitamente ad alte temperature e il prodotto risultante è l’anidride fosforica.
Per ottenere l’pentossido di difosforo, l’acido fosforico (H3PO4) può essere disidratato riscaldandolo ad alta temperatura. Questo processo rimuove le molecole d’acqua e provoca la formazione di pentossido di fosforo.
Un altro metodo per preparare l’pentossido di difosforo prevede la decomposizione termica di alcuni sali fosfatici. Ad esempio, il riscaldamento del fosfato monobasico di ammonio (NH4H2PO4) o del fosfato di ammonio ((NH4)3PO4) porta alla formazione di pentossido di fosforo.
Quando si sintetizza il pentossido di difosforo, è fondamentale prestare attenzione a causa della sua reattività e della generazione di calore durante reazioni specifiche. È necessario seguire le opportune precauzioni di sicurezza, come lavorare in un’area ben ventilata e indossare dispositivi di protezione adeguati.
Questi metodi sintetici forniscono strade per l’acquisizione di pentossido di difosforo, che trova applicazioni in vari campi, tra cui la produzione di acido fosforico, fertilizzanti e intermedi chimici.
Usi dell’ossido di fosforo
L’pentossido di difosforo (P2O5) trova varie applicazioni in diversi settori grazie alle sue proprietà uniche. Ecco alcuni usi comuni del pentossido di difosforo:
- Produzione di acido fosforico: la produzione di acido fosforico utilizza ampiamente il pentossido di difosforo come precursore chiave. L’acido fosforico ha molte applicazioni nei fertilizzanti, negli additivi alimentari e nei detergenti.
- Produzione di fertilizzanti: l’pentossido di difosforo svolge un ruolo essenziale nella produzione di vari fertilizzanti fosfatici, compresi i fertilizzanti superfosfato e fosfato di ammonio. Questi fertilizzanti forniscono alle piante nutrienti essenziali per promuovere una crescita sana.
- Intermedi chimici: la sintesi di vari composti organici, come prodotti farmaceutici, pesticidi e ritardanti di fiamma, si riferisce al pentossido di difosforo come intermedio chimico.
- Essiccante: il pentossido di difosforo ha una forte affinità per l’acqua e agisce come un essiccante. Viene utilizzato in diverse reazioni chimiche per rimuovere l’acqua e far avanzare le reazioni desiderate.
- Catalizzatore: il pentossido di difosforo agisce come catalizzatore in reazioni chimiche specifiche. Facilita queste reazioni riducendo l’energia di attivazione e quindi aumentando la velocità di reazione.
- Essiccante: la natura igroscopica del pentossido di difosforo lo rende adatto all’uso come essiccante in applicazioni sensibili all’umidità. Assorbe e rimuove efficacemente l’umidità dall’ambiente.
- Produzione del vetro: le formulazioni del vetro incorporano pentossido di difosforo per modificarne le proprietà, tra cui l’espansione termica e l’indice di rifrazione. Gli occhiali speciali, come i vetri ottici e i vetri al borosilicato, lo utilizzano attivamente.
- Trattamento della superficie metallica: i trattamenti della superficie metallica, come la fosfatazione, utilizzano pentossido di difosforo per migliorare la resistenza alla corrosione e migliorare l’adesione della vernice alle superfici metalliche.
Queste diverse applicazioni evidenziano l’importanza del pentossido di difosforo in settori che vanno dall’agricoltura al settore farmaceutico, rendendolo un composto prezioso e ampiamente utile.
Domande:
D: Qual è il numero di ossidazione del fosforo nello ione PO?
R: Il numero di ossidazione del fosforo nello ione PO è +5.
D: Qual è lo stato di ossidazione di un singolo atomo di fosforo in PO43−?
R: Lo stato di ossidazione di un singolo atomo di fosforo in PO43− è +5.
D: Qual è il numero di ossidazione del fosforo?
R: Il numero di ossidazione del fosforo può variare, ma generalmente appare +3 o +5.
D: Qual è il nome del composto P2O5?
R: Il nome del composto P2O5 è pentossido di fosforo (V).
D: Cos’è P2O5?
R: P2O5 è un composto chimico chiamato pentossido di fosforo (V).
D: Qual è il nome corretto per P2O5?
R: Il nome corretto per P2O5 è pentossido di fosforo (V).
D: Qual è il nome di P2O5?
R: Il nome di P2O5 è pentossido di fosforo (V).
D: P2O5 è anfotero?
R: No, P2O5 non è anfotero. È un ossido acido.
D: Cos’è il fertilizzante P2O5?
R: Il fertilizzante P2O5 si riferisce ai fertilizzanti che contengono pentossido di fosforo (V) (P2O5) come fonte di fosforo, che è importante per la crescita delle piante.
D: P2O5 è acido o basico?
R: P2O5 è un composto acido.
D: P2O5 è un composto ionico?
R: No, P2O5 è un composto covalente.
D: Come calcolare il P2O5 nei fertilizzanti?
R: Per calcolare la quantità di P2O5 in un fertilizzante, moltiplicare la percentuale di P2O5 per il peso del fertilizzante.
D: Proprietà di P2O5, solubile?
R: P2O5 è scarsamente solubile in acqua ma reagisce facilmente con l’acqua per formare acido fosforico.
D: Quanti chilogrammi di P sono contenuti nel 14% P2O5?
R: Per calcolare la quantità di fosforo (P) nel 14% P2O5, moltiplicare il peso del fertilizzante per 0,14.
