Il nitrato di nichel (Ni(NO₃)₂) è un composto chimico contenente ioni nichel e nitrato. È solubile in acqua e spesso utilizzato nei catalizzatori, nella galvanica e come precursore in altri composti del nichel.
| Nome IUPAC | Dinitrato di nichel |
| Formula molecolare | Ni(NO₃)₂ |
| numero CAS | 13138-45-9 |
| Sinonimi | Nitrato di nichel (II), nitrato di nichel, Dinitronickel, bis (nitrato) di nichel |
| InChI | InChI=1S/2NO3.Ni/c2 2-1(3)4;/q2 -1;+2 |
Proprietà del nitrato di nichel
Formula del nitrato di nichel
La formula chimica del dinitrato di nichel è Ni(NO₃)₂. Rappresenta un composto composto da cationi nichel (Ni) e anioni nitrato (NO₃). Il pedice “2” nella formula indica che ci sono due ioni NO3- per ciascun catione Ni+2.
Massa molare del nitrato di nichel
La massa molare del dinitrato di nichel può essere calcolata sommando le masse atomiche dei suoi elementi costitutivi. Il nichel (Ni) ha una massa molare di circa 58,69 g/mol, mentre il nitrato (NO₃) ha una massa molare di circa 62,00 g/mol. Sommandoli insieme, la massa molare del dinitrato di nichel è di circa 182,69 g/mol.
Punto di ebollizione del nitrato di nichel
Il punto di ebollizione del dinitrato di nichel si riferisce alla temperatura alla quale passa da liquido a gas. Il punto di ebollizione del dinitrato di nichel è di circa 136,7 gradi Celsius (278,06 gradi Fahrenheit). È fondamentale però notare che questo valore può variare leggermente a seconda della purezza del composto.
Punto di fusione del nitrato di nichel
Il punto di fusione del dinitrato di nichel è la temperatura alla quale passa dallo stato solido a quello liquido. Il punto di fusione del dinitrato di nichel è di circa 56,7 gradi Celsius (134,06 gradi Fahrenheit). Come il punto di ebollizione, il punto di fusione può essere influenzato dalla purezza del composto.
Densità del nitrato di nichel g/mL
La densità del dinitrato di nichel è una misura della sua massa per unità di volume. Il dinitrato di nichel ha una densità di circa 1,68 g/mL. Questo valore indica che è più denso dell’acqua, che ha una densità di 1 g/mL.
Peso molecolare del nitrato di nichel
Il peso molecolare del dinitrato di nichel è la somma dei pesi atomici di tutti gli atomi presenti nella sua formula chimica. Come accennato in precedenza, il peso molecolare del dinitrato di nichel è di circa 182,69 g/mol.
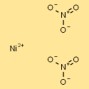
Struttura del nitrato di nichel
La struttura del dinitrato di nichel può essere visualizzata come cationi di nichel (Ni²⁺) circondati da due anioni nitrato (NO₃⁻) per catione. Gli ioni nitrato formano legami coordinati con i cationi nichel, creando un composto ionico stabile.
Solubilità del nitrato di nichel
Il dinitrato di nichel è molto solubile in acqua e forma una soluzione limpida blu-verdastra. La sua solubilità in acqua è una proprietà essenziale, poiché gli consente di essere facilmente utilizzato in varie applicazioni, come catalizzatori, galvanica e produzione di altri composti del nichel.
| Aspetto | Solido blu verdastro |
| Peso specifico | 1,68 g/ml |
| Colore | blu verdastro |
| Odore | Inodore |
| Massa molare | 182,69 g/mole |
| Densità | 1,68 g/ml |
| Punto di fusione | 56,7°C |
| Punto di ebollizione | 136,7°C |
| Punto flash | Non applicabile |
| solubilità in acqua | Molto solubile |
| Solubilità | Solubile in acqua e solventi organici come l’etanolo |
| Pressione del vapore | Non disponibile |
| Densità del vapore | Non disponibile |
| pKa | Non disponibile |
| pH | Neutro (circa 7) |
Si prega di notare che alcune proprietà potrebbero non essere disponibili o rilevanti per il diitrato di nichel.
Sicurezza e pericoli del nitrato di nichel
Il dinitrato di nichel presenta alcuni rischi per la sicurezza e occorre prestare attenzione quando lo si maneggia. Il contatto diretto con il composto può causare irritazione alla pelle e agli occhi. L’inalazione delle sue polveri o dei suoi fumi può causare irritazione respiratoria. È essenziale indossare dispositivi di protezione adeguati, come guanti e occhiali di sicurezza, quando si lavora con il dinitrato di nichel. Evitare l’ingestione poiché potrebbe essere dannoso per la salute. In caso di esposizione accidentale, consultare immediatamente un medico. Inoltre, un corretto stoccaggio in un’area ben ventilata, lontano da sostanze incompatibili, è fondamentale per ridurre al minimo i rischi potenziali e garantire una manipolazione sicura.
| Simboli di pericolo | Corrosivo, irritante, pericoloso per la salute |
| Descrizione della sicurezza | Provoca irritazione alla pelle e agli occhi. Nocivo se inalato o ingerito. Maneggiare con cura. Evitare il contatto diretto. Utilizzare dispositivi di protezione. |
| Numeri di identificazione delle Nazioni Unite | UN2724 |
| Codice SA | 2834.2990 |
| Classe di pericolo | 5.1 (Sostanze ossidanti) |
| Gruppo di imballaggio | II |
| Tossicità | Moderatamente tossico |
Metodi per la sintesi del nitrato di nichel
Esistono diversi metodi per sintetizzare il dinitrato di nichel. Un metodo comune prevede la reazione tra l’ossido di nichel (NiO) o l’idrossido di nichel (Ni(OH)₂) con acido nitrico (HNO₃). Durante questo processo, l’ossido di nichel o l’idrossido di nichel si dissolve nell’acido nitrico, portando alla formazione di dinitrato di nichel e acqua come sottoprodotti.
La reazione può assumere la seguente rappresentazione:
- Con ossido di nichel: NiO + 2HNO₃ → Ni(NO₃)₂ + H₂O
- Con idrossido di nichel: Ni(OH)₂ + 2HNO₃ → Ni(NO₃)₂ + 2H₂O
Un altro approccio prevede la reazione tra nichel metallico e acido nitrico concentrato, che provoca la formazione di dinitrato di nichel e biossido di azoto gassoso (NO₂) come sottoprodotto:
- Con nichel metallico: Ni + 4HNO₃ → Ni(NO₃)₂ + 2H₂O + 2NO₂
È importante effettuare queste reazioni in condizioni ben controllate perché l’acido nitrico è un forte agente ossidante e può essere pericoloso. Garantire un risultato sicuro e positivo durante il processo di sintesi impiegando attivamente misure e attrezzature di sicurezza adeguate. Inoltre, la scelta dei reagenti e delle condizioni di reazione può variare a seconda dell’applicazione specifica e delle proprietà desiderate del prodotto dinitrato di nichel.
Usi del nitrato di nichel
Il dinitrato di nichel trova molteplici applicazioni in vari settori grazie alle sue proprietà uniche. Ecco alcuni dei suoi principali utilizzi:
- Galvanotecnica: il dinitrato di nichel consente la deposizione di un sottile strato di nichel su vari metalli, migliorandone la resistenza alla corrosione e l’aspetto durante i processi di galvanica.
- Catalizzatore: svolge un ruolo cruciale come catalizzatore nelle reazioni chimiche, facilitando la conversione dei reagenti nei prodotti desiderati, soprattutto nella sintesi organica.
- Ceramica: l’industria ceramica utilizza il dinitrato di nichel per conferire colorazioni specifiche e migliorare le prestazioni dei materiali ceramici.
- Industria del vetro: i produttori dell’industria del vetro utilizzano il dinitrato di nichel per produrre vetro colorato con proprietà ottiche desiderabili.
- Produzione di batterie: i produttori utilizzano il dinitrato di nichel nella produzione di batterie a base di nichel, comprese le batterie al nichel-metallo idruro (NiMH).
- Celle a combustibile: il dinitrato di nichel funge da precursore nella produzione di elettrodi di ossido di nichel per celle a combustibile a ossido solido (SOFC).
- Pirotecnica: nella pirotecnica, il dinitrato di nichel funge da ossidante, producendo fiamme verdi nei fuochi d’artificio.
- Reagenti chimici: funziona come reagente in varie reazioni chimiche, in particolare quelle che coinvolgono complessi di nichel.
- Fertilizzanti: in agricoltura, il dinitrato di nichel viene occasionalmente utilizzato come fonte di nichel nei fertilizzanti per affrontare le carenze di nichel in alcune colture.
Le diverse applicazioni del dinitrato di nichel in diversi settori evidenziano la sua importanza come composto versatile con un’ampia varietà di usi pratici.
Domande:
D: Quando si mescolano soluzioni di fosfato di ammonio e nitrato di nichel (ii), cosa precipita?
A: Il fosfato di nichel (II) precipita.
D: Qual è la molarità di una soluzione contenente 5,8 grammi di nitrato di nichel in 500 ml?
R: La molarità è 0,2 M.
D: Quali lunghezze d’onda assorbe il nitrato di nichel?
R: Il dinitrato di nichel assorbe le lunghezze d’onda nelle regioni ultraviolette e visibili.
D: Il nitrato di nichel II è solubile?
R: Sì, il dinitrato di nichel (II) è solubile in acqua.
D: Qual è la formula del nitrato di nichel II?
R: La formula è Ni(NO₃)₂.
D: Qual è il colore del nitrato di nichel II?
A: Il colore del dinitrato di nichel (II) è blu verdastro.
D: Quanti atomi di azoto ci sono nella formula chimica Ni(NO₃)₂?
R: Ci sono quattro atomi di azoto.
D: Il Ni(NO₃)₂ è solubile in acqua?
R: Sì, Ni(NO₃)₂ è solubile in acqua.
D: Quale dei composti C4H10, BaCl2, Ni(NO₃)₂, SF6 dovrebbe esistere come unità della formula?
R: C4H10 (butano) e SF6 (esafluoruro di zolfo) dovrebbero esistere come unità della formula. BaCl2 e Ni(NO₃)₂ sono composti ionici.
