Il metossibenzene, noto anche come anisolo, è un composto aromatico con un gruppo metossi (-OCH3) attaccato ad un anello benzenico. È comunemente usato come solvente e agente aromatizzante.
| Nome IUPAC | Metossibenzene |
| Formula molecolare | C7H8O |
| numero CAS | 100-66-3 |
| Sinonimi | Anisolo, metossibenzene, metilanisolo, metilfenil etere, fenossimetano, alcol anisillico, anisolo, fenilmetil etere |
| InChI | InChI=1S/C7H8O/c1-8-7-5-3-2-4-6-7/h2-6H,1H3 |
Densità dell’anisolo g/ml
Il metossibenzene ha una densità di 0,995 g/mL a temperatura ambiente. La densità è la massa di una sostanza per unità di volume ed è una proprietà fisica importante nel determinare la purezza e la concentrazione di un campione. Il metossibenzene è meno denso dell’acqua, che ha una densità di 1 g/ml, e leggermente meno denso del benzene (0,879 g/ml).
Massa molare del metossibenzene
Il metossibenzene ha una massa molare di 108,14 g/mol. La massa molare è la massa di una mole di una sostanza e si calcola sommando i pesi atomici di tutti gli atomi della molecola. Nel metossibenzene, la formula molecolare è C7H8O, che contiene un totale di 7 atomi di carbonio, 8 atomi di idrogeno e 1 atomo di ossigeno. La massa molare del metossibenzene è utile per calcolare la quantità di sostanza in un dato campione, nonché per la conversione tra moli, massa e volume.
Punto di ebollizione del metossibenzene
Il metossibenzene ha un punto di ebollizione di 154,2°C (309,6°F). Il punto di ebollizione è la temperatura alla quale la pressione del vapore di un liquido eguaglia la pressione esterna, consentendo al liquido di trasformarsi in un gas. Il metossibenzene è un liquido relativamente volatile, il che significa che evapora facilmente a temperatura ambiente. Il suo punto di ebollizione è superiore a quello del benzene (80,1 °C) a causa della presenza del gruppo metossi (-OCH3), che aumenta le forze intermolecolari tra le molecole.
Punto di fusione del metossibenzene
Il metossibenzene ha un punto di fusione di -37,5°C (-35,5°F). Il punto di fusione è la temperatura alla quale una sostanza solida passa allo stato liquido. Il metossibenzene è un liquido incolore a temperatura ambiente, ma può solidificarsi a basse temperature. La presenza del gruppo metossi abbassa il punto di fusione del metossibenzene rispetto al benzene, che ha un punto di fusione di 5,5 °C.
Peso molecolare del metossibenzene
Il metossibenzene ha un peso molecolare di 108,14 g/mol. Il peso molecolare è la somma dei pesi atomici di tutti gli atomi presenti in una molecola. È un parametro utile per calcolare la stechiometria delle reazioni chimiche e per la conversione tra moli, massa e volume.
Struttura del metossibenzene
Il metossibenzene ha una struttura costituita da un anello benzenico con un gruppo metossi (-OCH3) attaccato a uno degli atomi di carbonio. Il gruppo metossi è un gruppo metilico (-CH3) legato ad un atomo di ossigeno (-O), che a sua volta è legato all’anello benzenico. Il metossibenzene è un composto aromatico, il che significa che ha una struttura planare e ciclica con alternanza di legami singoli e doppi.
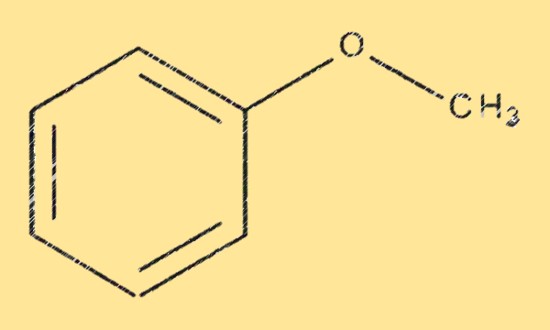
Formula del metossibenzene
Il metossibenzene ha una formula molecolare C7H8O, che indica il numero e il tipo di atomi nella molecola. La formula può essere utilizzata per calcolare la massa molare, la densità e altre proprietà fisiche del metossibenzene. Oltre alla sua formula molecolare, il metossibenzene è conosciuto anche con diversi nomi comuni e sinonimi, tra cui anisolo, metilfenil etere e fenossimetano.
| Aspetto | Liquido incolore |
| Peso specifico | 0,995 g/ml |
| Colore | Incolore |
| Odore | Aromatico, dolce, gradevole |
| Massa molare | 108,14 g/mole |
| Densità | 0,995 g/ml |
| Punto di fusione | -37,5°C (-35,5°F) |
| Punto di ebollizione | 154,2°C (309,6°F) |
| Punto flash | 58°C (136,4°F) |
| solubilità in acqua | 1,41 g/l a 20°C |
| Solubilità | Miscibile in alcool, etere, benzene, cloroformio |
| Pressione del vapore | 1,44 mmHg a 25°C |
| Densità del vapore | 3,74 (aria = 1) |
| pKa | 17 |
| pH | Non applicabile |
Sicurezza e pericoli del metossibenzene
Il metossibenzene, noto anche come anisolo, è generalmente considerato una sostanza a rischio da basso a moderato. Tuttavia, può causare irritazione agli occhi, alla pelle e al sistema respiratorio in caso di esposizione. Anche il metossibenzene è infiammabile e può accendersi se esposto al calore o a una fonte di accensione. Può anche emettere fumi tossici quando brucia. L’esposizione a lungo termine al metossibenzene può causare danni al fegato e ai reni. È importante seguire le adeguate precauzioni di sicurezza quando si maneggia o si lavora con il metossibenzene, compreso indossare dispositivi di protezione adeguati e conservarlo in un’area fresca, asciutta e ben ventilata, lontano da fonti di calore e infiammazioni.
| Simboli di pericolo | XI |
| Descrizione della sicurezza | S24/25: Evitare il contatto con la pelle e gli occhi. S37/39: Usare guanti adatti e proteggersi gli occhi/la faccia. |
| Identificatori AN | ONU 2222 |
| Codice SA | 29093000 |
| Classe di pericolo | 3 |
| Gruppo di imballaggio | III |
| Tossicità | Può causare irritazione agli occhi, alla pelle e al sistema respiratorio. L’esposizione a lungo termine può causare danni al fegato e ai reni. |
Metodi per la sintesi del metossibenzene
L’anisolo può essere sintetizzato con diversi metodi, inclusa la metilazione del fenolo con dimetil solfato o cloruro di metile in presenza di una base forte, come l’idrossido di sodio. Un altro metodo consiste nel far reagire l’anisaldeide con un agente riducente, come boroidruro di sodio, per ottenere l’anisolo.
Una reazione di Gattermann modificata può essere utilizzata anche per sintetizzare l’anisolo, che prevede la reazione dell’anisolo con acido cianidrico e acido cloridrico in presenza di polvere di rame. Questo metodo è utile per produrre anisolo in quantità maggiori.
Inoltre, l’anisolo può essere prodotto mediante la sintesi dell’etere Williamson facendo reagire metossido di sodio con bromobenzene. Questa reazione porta alla formazione di anisolo e bromuro di sodio come sottoprodotto.
Altri metodi di sintesi dell’anisolo includono l’uso del diazometano, la metanolisi dell’acetato di fenile e l’alchilazione del fenossido di sodio con ioduro di metile.
La scelta del metodo di sintesi dipende dalla purezza, dalla resa e dalla quantità di anisolo desiderate necessarie per una particolare applicazione. È necessario prestare attenzione durante la sintesi per garantire che vengano seguite le opportune precauzioni di sicurezza e che vengano utilizzati dispositivi di protezione adeguati per evitare il contatto con l’anisolo.
Usi del metossibenzene
L’anisolo, noto anche come anisolo, ha una vasta gamma di usi in vari settori. Una delle sue principali applicazioni è come solvente, in particolare nella produzione di resine, vernici e lacche. Viene anche utilizzato nella fabbricazione di vari prodotti farmaceutici, tra cui l’aspirina, come agente aromatizzante e nella produzione di profumi e fragranze.
L’anisolo viene utilizzato anche come intermedio nella produzione di altri prodotti chimici, come la p-anisidina, un componente chiave nella produzione di coloranti azoici. Viene anche utilizzato come materia prima per la sintesi di altri derivati dell’anisolo, tra cui p-metossifenolo e acido p-metossicinnamico, che hanno un’ampia gamma di applicazioni nell’industria chimica.
In laboratorio, l’anisolo viene utilizzato come standard nella gascromatografia e nella spettrometria di massa. Viene anche utilizzato come materiale di riferimento per la spettroscopia.
Inoltre, l’anisolo viene utilizzato nella produzione di vari aromi e fragranze, inclusa la vanillina, che viene utilizzata come agente aromatizzante in alimenti e bevande. Nel complesso, la natura versatile dell’anisolo lo rende un prodotto chimico prezioso in varie applicazioni, in particolare nell’industria chimica, farmaceutica e dei profumi.
