Il litio alluminio idruro (LiAlH4) è un potente agente riducente utilizzato in chimica organica per convertire i composti carbonilici in alcoli. Reagisce vigorosamente con l’acqua.
| Nome IUPAC | Litio alluminio idruro |
| Formula molecolare | LiAlH4 |
| numero CAS | 16853-85-3 |
| Sinonimi | Tetraidroalluminato di litio(III), litio alluminio(III) idruro |
| InChI | InChI=1S/Al.Li.4H |
Proprietà del litio alluminio idruro (LiAlH4)
Formula di litio alluminio idruro (LiAlH4).
La formula del tetraidriddoalluminato di litio (LiAlH4) rappresenta la sua composizione. È costituito da un atomo di litio (Li), un atomo di alluminio (Al) e quattro atomi di idrogeno (H). La formula è scritta LiAlH4, che indica la presenza di questi elementi.
Massa molare del litio alluminio idruro (LiAlH4).
La massa molare del tetraidroalluminato di litio (LiAlH4) è la somma delle masse atomiche dei suoi elementi costitutivi. Viene calcolato come segue:
- Il litio (Li) ha una massa molare di circa 6,94 g/mol.
- L’alluminio (Al) ha una massa molare di circa 26,98 g/mol.
- L’idrogeno (H) ha una massa molare di circa 1,01 g/mol.
Sommando questi valori, la massa molare di LiAlH4 è di circa 37,95 g/mol.
Litio alluminio idruro (LiAlH4) Punto di ebollizione
Il tetraidroalluminato di litio (LiAlH4) non ha un punto di ebollizione distinto perché si decompone prima di raggiungere il punto di ebollizione di uno qualsiasi dei suoi singoli componenti. Dopo il riscaldamento, LiAlH4 subisce una reazione di decomposizione, rilasciando gas idrogeno.
Litio alluminio idruro (LiAlH4) Punto di fusione
Il tetraidroalluminato di litio (LiAlH4) ha un punto di fusione relativamente basso. Si scioglie a circa 150-160°C (302-320°F). A questa temperatura, il solido LiAlH4 si trasforma in uno stato liquido, permettendogli di partecipare alle reazioni chimiche.
Litio alluminio idruro (LiAlH4) Densità g/mL
La densità del tetraidriddoalluminato di litio (LiAlH4) è di circa 0,917 g/mL. Questo valore di densità indica la massa di LiAlH4 presente in un volume specifico, con l’unità di grammi per millilitro.
Peso molecolare del litio alluminio idruro (LiAlH4).
Il peso molecolare del tetraidroalluminato di litio (LiAlH4) viene calcolato sommando i pesi atomici di tutti i suoi elementi costitutivi. Il peso molecolare di LiAlH4 è di circa 37,95 g/mol.
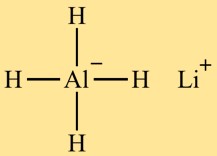
Struttura dell’idruro di litio alluminio (LiAlH4)
Il tetraidroalluminato di litio (LiAlH4) ha una struttura tetraedrica. L’atomo di alluminio è al centro, circondato da quattro atomi di idrogeno. L’atomo di litio è collegato anche all’atomo di alluminio, completandone la struttura.
Solubilità dell’idruro di litio alluminio (LiAlH4)
Il tetraidriddoalluminato di litio (LiAlH4) è insolubile nella maggior parte dei solventi organici come eteri e idrocarburi. Tuttavia, è molto reattivo con l’acqua, subendo una vigorosa reazione esotermica e producendo gas idrogeno. Pertanto, LiAlH4 viene generalmente maneggiato e conservato in condizioni anidre per evitare qualsiasi reazione avversa con l’umidità.
| Aspetto | polvere bianca |
| Peso specifico | 0,917 g/ml |
| Colore | Incolore |
| Odore | Inodore |
| Massa molare | 37,95 g/mole |
| Densità | 0,917 g/ml |
| Punto di fusione | 150-160°C |
| Punto di ebollizione | Decomposto |
| Punto flash | Non applicabile |
| solubilità in acqua | Reagisce vigorosamente con l’acqua |
| Solubilità | Insolubile in solventi organici come eteri e idrocarburi |
| Pressione del vapore | Non applicabile |
| Densità del vapore | Non applicabile |
| pKa | Non applicabile |
| pH | Non applicabile |
Sicurezza e pericoli del litio alluminio idruro (LiAlH4).
Il tetraidroalluminato di litio (LiAlH4) comporta notevoli rischi per la sicurezza e deve essere maneggiato con estrema cautela. È un composto altamente reattivo che reagisce violentemente con l’acqua, rilasciando gas idrogeno infiammabile. LiAlH4 è piroforico, il che significa che può accendersi spontaneamente nell’aria. Dovrebbe essere conservato lontano dall’umidità e conservato in contenitori ermeticamente chiusi. Il contatto diretto con LiAlH4 può causare gravi ustioni e irritazioni alla pelle, agli occhi e al sistema respiratorio. L’inalazione delle sue polveri o dei suoi fumi può causare difficoltà respiratorie. Quando si lavora con LiAlH4 è necessario indossare dispositivi di protezione individuale adeguati, come guanti e occhiali protettivi, e maneggiarlo solo in aree ben ventilate con adeguate misure di sicurezza in atto.
| Simboli di pericolo | F,C |
| Descrizione della sicurezza | Altamente infiammabile. Reagisce violentemente con l’acqua. Maneggiare con estrema cautela. |
| Numeri di identificazione delle Nazioni Unite | ONU 1410 |
| Codice SA | 2850.00.00 |
| Classe di pericolo | 4.3 |
| Gruppo di imballaggio | IO |
| Tossicità | Molto tossico, può causare gravi ustioni e difficoltà respiratorie. |
Nota: i simboli di pericolo utilizzati sono “F” per infiammabile e “C” per corrosivo. La descrizione della sicurezza evidenzia la reattività con l’acqua e sottolinea la necessità di estrema cautela. Gli identificatori ONU e il codice HS sono codici identificativi specifici utilizzati per scopi di trasporto e commercio. La classe di pericolo indica la classificazione della sostanza in base alle sue caratteristiche. Il gruppo di imballaggio rappresenta il livello di pericolo durante il trasporto. Il tetraidriddoalluminato di litio (LiAlH4) è altamente tossico e può causare gravi ustioni e difficoltà respiratorie per contatto o inalazione.
Metodi per la sintesi del litio alluminio idruro (LiAlH4)
Diversi metodi consentono la sintesi del tetraidroalluminato di litio (LiAlH4).
Un metodo comune per sintetizzare il tetraidruro di litio (LiAlH4) consiste nel riscaldare AlCl3 e combinarlo con l’idruro di litio (LiH) in un solvente come l’etere etilico . La reazione avviene in presenza di calore, dando luogo alla formazione di LiAlH4.
Un altro metodo consiste nel mescolare l’alluminio in polvere con l’idruro di litio e quindi riscaldare la miscela. La reazione avviene portando alla formazione di LiAlH4.
Per sintetizzare LiAlH4 utilizzando un approccio diverso, combinare il deuteruro di litio alluminio (LiAlD4) con LiH in un solvente come tetraidrofurano (THF) . Riscaldare la miscela, provocando una reazione tra LiAlD4 e idruro di litio, con conseguente formazione di LiAlH4.
Va notato che questi metodi sintetici richiedono un’attenta manipolazione a causa della reattività dei composti coinvolti. Precauzioni come lavorare in condizioni inerti, utilizzare attrezzature di sicurezza adeguate e condurre reazioni in aree ben ventilate sono essenziali per garantire una sintesi sicura e di successo.
Usi del litio alluminio idruro (LiAlH4)
Il tetraidroalluminato di litio (LiAlH4) ha diverse applicazioni in chimica organica grazie alle sue potenti proprietà riducenti. Ecco alcuni usi comuni:
- Riduzione dei composti carbonilici: LiAlH4 converte in modo significativo vari composti carbonilici, come aldeidi, chetoni, esteri e acidi carbossilici, nei loro corrispondenti alcoli. Questa reazione di riduzione è cruciale nella sintesi di prodotti farmaceutici, prodotti di chimica fine e intermedi organici.
- Riduzione dei composti nitro: LiAlH4 può ridurre i composti nitro ad ammine primarie. Questa trasformazione è preziosa nella sintesi di un’ampia gamma di composti organici, inclusi prodotti farmaceutici, coloranti e prodotti chimici per l’agricoltura.
- Deossigenazione: LiAlH4 può rimuovere selettivamente gli atomi di ossigeno da vari gruppi funzionali, come alcoli, acidi e ossime. Questo processo di deossigenazione è utile nella preparazione di composti sensibili all’ossigeno o quando è necessario rimuovere la funzionalità dell’ossigeno.
- Reazioni di polimerizzazione: LiAlH4 agisce come agente riducente in alcune reazioni di polimerizzazione, facilitando la formazione di polimeri. I ricercatori utilizzano LiAlH4 nella produzione di materiali ad alte prestazioni, tra cui polimeri conduttivi e plastiche speciali.
- Applicazioni sintetiche: LiAlH4 viene utilizzato nella sintesi di vari composti organici, tra cui idrazine, fosfine e composti organometallici. Questi composti sono essenziali nella ricerca farmaceutica, nella catalisi e nella scienza dei materiali.
- Agente riducente da laboratorio: LiAlH4 funge da agente riducente versatile in laboratorio. Consente ai chimici di ridurre selettivamente gruppi funzionali specifici, consentendo così la sintesi di molecole complesse con elevata precisione.
Nel complesso, il tetraidriddoalluminato di litio (LiAlH4) svolge un ruolo cruciale nella sintesi organica, fornendo ai chimici un potente strumento per varie reazioni di riduzione e consentendo la preparazione di un’ampia gamma di composti preziosi.
Domande:
D: L’idruro di litio e alluminio riduce i doppi legami?
R: Sì, il tetraidroalluminato di litio può ridurre i doppi legami e convertirli in legami singoli.
D: Quale gas rilascia l’idruro di litio alluminio quando reagisce con un solvente protico?
R: Quando il tetraidriddoalluminato di litio reagisce con un solvente protico, rilascia gas idrogeno.
D: Dove posso acquistare l’idruro di litio e alluminio?
R: Il tetraidroalluminato di litio può essere acquistato da fornitori di prodotti chimici o fornitori di apparecchiature di laboratorio specializzate.
D: È a base di litio alluminio idruro?
R: No, il tetraidriddoalluminato di litio non è considerato una base ma un potente agente riducente.
D: Cosa riduce LiAlH4?
R: Il tetraidroalluminato di litio può ridurre vari gruppi funzionali, inclusi composti carbonilici, gruppi nitro e alcoli.
D: Il litio alluminio idruro è un nucleofilo?
R: Sì, il tetraidruroalluminato di litio agisce come nucleofilo in molte reazioni organiche a causa della presenza dello ione idruro.
D: L’idruro di litio e alluminio riduce gli alcoli?
R: Sì, il tetraidroalluminato di litio può ridurre gli alcoli per produrre alcoli primari o secondari.
D: L’idruro di litio alluminio riduce gli alcheni?
R: No, il tetraidrididoalluminato di litio generalmente non reagisce con gli alcheni.
D: Con quale dei seguenti solventi l’idruro di litio alluminio non reagisce?
R: Il tetraidriddoalluminato di litio generalmente non reagisce con solventi non polari come l’esano o l’etere etilico.
D: L’idruro di litio e alluminio influisce sugli alcoli?
R: Sì, il tetraidrididoalluminato di litio può ridurre gli alcoli, ma dovrebbe essere usato con cautela poiché può essere molto reattivo e potenzialmente pericoloso.
