NH4OH o idrossido di ammonio è una soluzione limpida e incolore comunemente nota come ammoniaca domestica. È una soluzione fortemente alcalina con un pH di 11-12. Viene utilizzato come detergente, nella produzione di fertilizzanti e in alcune applicazioni alimentari come agente lasciando.
| Nome IUPAC | Idrossido d’ammonio |
| Formula molecolare | NH4OH |
| numero CAS | 1336-21-6 |
| Sinonimi | Soluzione di ammoniaca, ammoniaca acquosa, ammoniaca domestica |
| InChI | InChI=1S/H5NO/c1-5(2,3)4/h(H,1,2,3,4)/p+1 |
Proprietà dell’idrossido di ammonio
Formula di idrossido di ammonio
La formula chimica dell’idrossido di ammonio è NH4OH. La formula rappresenta il numero relativo e i tipi di atomi nel composto. La “N” rappresenta l’azoto, “H” rappresenta l’idrogeno e “O” rappresenta l’ossigeno. I numeri indice nella formula indicano il numero di atomi di ciascun elemento nel composto. Nel caso dell’idrossido di ammonio, c’è un atomo di azoto, quattro atomi di idrogeno e un atomo di ossigeno. La formula dell’idrossido di ammonio rappresenta il composto ionico, che è composto da ioni ammonio caricati positivamente (NH4+) e ioni idrossido caricati negativamente (OH-).
Idrossido di ammonio Ph
Il pH dell’idrossido di ammonio (NH4OH) è basico, con un valore intorno a 11. Ciò significa che l’idrossido di ammonio ha un’alta concentrazione di ioni idrossido (OH-) ed è molto alcalino. Il pH delle soluzioni di idrossido di ammonio può variare a seconda della concentrazione, della temperatura e di altri fattori, ma è generalmente considerata una base forte con un pH superiore a 7,0. L’idrossido di ammonio è comunemente utilizzato in varie applicazioni industriali e domestiche, come la pulizia e la regolazione del pH, a causa della sua elevata alcalinità. Tuttavia, è importante maneggiare l’idrossido di ammonio con cautela, poiché può essere corrosivo e pericoloso se non maneggiato correttamente.
Idrossido di ammonio MSDS
MSDS sta per Material Safety Data Sheet, un documento che fornisce informazioni sulle proprietà, la manipolazione, lo stoccaggio e lo smaltimento di una sostanza chimica. Una scheda di sicurezza per l’idrossido di ammonio (NH4OH) fornirebbe informazioni sulle sue proprietà fisiche e chimiche, sui potenziali effetti sulla salute, sui pericoli di incendio ed esplosione e su eventuali misure protettive da adottare durante la manipolazione o l’utilizzo della sostanza.
La scheda di sicurezza per l’idrossido di ammonio includerebbe anche informazioni sulla sua tossicità, reattività e infiammabilità, nonché eventuali misure di primo soccorso adeguate in caso di esposizione. Inoltre, la scheda di sicurezza fornirebbe informazioni sulla corretta conservazione e smaltimento dell’idrossido di ammonio, comprese eventuali precauzioni necessarie per prevenire fuoriuscite o perdite.
Solubilità dell’idrossido di ammonio
L’idrossido di ammonio (NH4OH) è molto solubile in acqua. Forma una soluzione limpida, incolore, altamente alcalina con un odore caratteristico. La solubilità dell’idrossido di ammonio in acqua dipende dalla temperatura e dalla concentrazione, con temperature e concentrazioni più elevate che determinano una maggiore solubilità.
In generale, l’idrossido di ammonio si dissolve facilmente in acqua, producendo una soluzione da neutra ad alcalina con un pH compreso tra circa 9 e 11. La solubilità dell’idrossido di ammonio in acqua è influenzata anche da altri fattori come pressione, temperatura e presenza di altri fattori. sostanze disciolte.
Massa molare dell’idrossido di ammonio
La massa molare dell’idrossido di ammonio (NH4OH) è 35,05 g/mol. Questo valore è importante per determinare la quantità di idrossido di ammonio in un campione, nonché per le reazioni chimiche che coinvolgono il composto. Per determinare la massa molare di una sostanza si sommano i pesi atomici di tutti gli elementi del composto. Nel caso dell’idrossido di ammonio, la massa molare viene calcolata sommando i pesi atomici di azoto (14,01 g/mol), idrogeno (1,01 g/mol) e ossigeno (16,00 g/mol).
Punto di ebollizione dell’idrossido di ammonio
Il punto di ebollizione dell’idrossido di ammonio è di circa 38°C. Questo valore è importante per determinare le condizioni in cui il composto cambierà da liquido a gas. Trova il punto di ebollizione dell’idrossido di ammonio misurando la tensione di vapore della sostanza. La tensione di vapore è la pressione esercitata dal vapore sul liquido in un contenitore chiuso. Tieni presente che il punto di ebollizione può cambiare anche a seconda della pressione e della temperatura.
Punto di fusione dell’idrossido di ammonio
Il punto di fusione dell’idrossido di ammonio è -77°C. Questo valore è importante per determinare le condizioni in cui il composto cambierà da solido a liquido. Misurare il punto di fusione dell’idrossido di ammonio valutando la forza dei suoi legami intermolecolari. Ricordare che il punto di fusione può variare a seconda della pressione e della temperatura dell’ambiente circostante.
Densità dell’idrossido di ammonio g/ml
La densità dell’idrossido di ammonio è di circa 0,91 g/mL. Questo valore è importante per determinare la quantità di idrossido di ammonio in un dato volume, nonché per calcolare la massa della sostanza in un dato volume. Determina la densità dell’idrossido di ammonio dividendo la sua massa per il volume che occupa. Tieni presente che la densità di una sostanza può cambiare a seconda della temperatura e della pressione.
Peso molecolare dell’idrossido di ammonio
Il peso molecolare dell’idrossido di ammonio è 35,05 g/mol. Questo valore è importante per determinare la quantità di idrossido di ammonio in un campione, nonché per le reazioni chimiche che coinvolgono il composto. Calcolare il peso molecolare dell’idrossido di ammonio aggiungendo i pesi atomici di azoto (14,01 g/mol), idrogeno (1,01 g/mol) e ossigeno (16,00 g/mol).
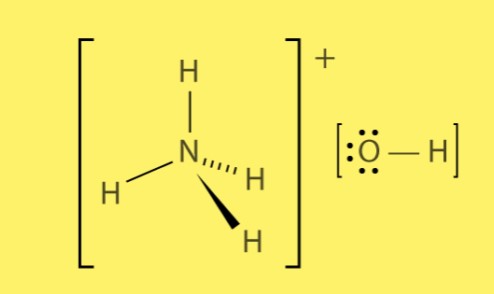
Struttura dell’idrossido di ammonio
L’idrossido di ammonio è formato dalla combinazione di ioni ammonio caricati positivamente (NH4+) e ioni idrossido caricati negativamente (OH-). I legami ionici tra questi ioni creano una forte attrazione elettrostatica, portando alla formazione del composto.
| Aspetto | Liquido limpido e incolore |
| Peso specifico | 0,91 g/ml |
| Colore | Incolore |
| Odore | Odore pungente, simile all’ammoniaca |
| Massa molare | 35,05 g/mole |
| Densità | 0,91 g/ml |
| Punto di fusione | -77°C |
| Punto di ebollizione | 38°C |
| Punto flash | Non applicabile |
| solubilità in acqua | Completamente solubile |
| Solubilità | Solubile in etanolo e metanolo |
| Pressione del vapore | 17,5 mmHg a 20°C |
| Densità del vapore | 0,6 (aria = 1) |
| pKa | 10.64 |
| pH | 11.6 (soluzione 1M) |
Sicurezza e pericoli dell’idrossido di ammonio
L’idrossido di ammonio è una soluzione fortemente alcalina e può essere pericolosa se maneggiata in modo improprio. Se inalato può causare irritazione alla pelle e agli occhi e problemi respiratori. In caso di contatto con la pelle, abbondantemente con acqua e se necessario consultare un medico. Se ingerito può causare gravi danni o la morte. È quindi importante tenerlo fuori dalla portata dei bambini e degli animali domestici. Inoltre è infiammabile e va tenuto lontano da fonti di calore e fiamme. Quando si utilizza l’idrossido di ammonio, è importante indossare dispositivi di protezione come guanti e protezione per gli occhi. In caso di fuoriuscita, neutralizzare con acido e pulire con ventilazione adeguata. L’osservanza delle precauzioni di sicurezza e una corretta conservazione sono essenziali quando si maneggia l’idrossido di ammonio.
| Simboli di pericolo | Corrosivo |
| Descrizione della sicurezza | S26, S37/39 |
| Numeri di identificazione delle Nazioni Unite | UN2672 |
| Codice SA | 2814.10.00 |
| Classe di pericolo | 8 |
| Gruppo di imballaggio | II |
| Tossicità | Nocivo se ingerito, inalato o a contatto con la pelle. Può causare gravi irritazioni e ustioni. |
Metodi per la sintesi dell’idrossido di ammonio
L’idrossido di ammonio può essere sintetizzato mediante due metodi principali: il processo del cloruro di ammonio e il processo dell’ammoniaca.
Il processo del cloruro di ammonio prevede la reazione del gas di ammoniaca e dell’acido cloridrico, producendo cloruro di ammonio e acqua:
NH3 + HCl → NH4Cl + H2O
Il cloruro di ammonio viene quindi sciolto in acqua per produrre una soluzione di idrossido di ammonio. Questa soluzione può essere ulteriormente concentrata mediante distillazione per produrre una soluzione concentrata di idrossido di ammonio.
Il processo dell’ammoniaca prevede la reazione diretta del gas di ammoniaca e dell’acqua, producendo idrossido di ammonio e gas idrogeno:
NH3 + H2O → NH4OH + H2
La produzione di idrossido di ammonio può essere controllata regolando la temperatura e la pressione durante la reazione esotermica, ottenendo una soluzione che può essere purificata e concentrata attraverso tecniche di lavaggio e distillazione. La produzione industriale di idrossido di ammonio utilizza comunemente il processo con ammoniaca per la sua semplicità ed efficienza, ma il processo con cloruro di ammonio funge da opzione di backup durante la carenza di ammoniaca.
Usi dell’idrossido di ammonio
L’idrossido di ammonio ha molti usi in diversi settori. Alcune delle sue applicazioni comuni sono:
- In varie applicazioni domestiche e industriali, l’idrossido di ammonio viene utilizzato come detergente per rimuovere efficacemente grasso, olio e sporco dalle superfici.
- Nell’industria alimentare viene utilizzato come disinfettante per uccidere batteri e agenti patogeni sulle superfici a contatto con gli alimenti. In agricoltura, l’idrossido di ammonio fornisce azoto essenziale come fertilizzante per la crescita delle piante ed è un ingrediente chiave nella produzione di fertilizzante a base di nitrato di ammonio.
- Nell’industria farmaceutica viene utilizzato nella produzione di alcuni farmaci e come regolatore del pH nella fabbricazione di alcuni prodotti medici.
- L’industria della panificazione utilizza l’idrossido di ammonio come agente lievitante per far lievitare l’impasto e funziona anche come agente aromatizzante in alcuni prodotti alimentari e come regolatore del pH nella produzione di alcuni alimenti e bevande.
- Nell’industria tessile, l’idrossido di ammonio neutralizza gli acidi e regola i livelli di pH nella produzione tessile. Nel trattamento dell’acqua, regola i livelli di pH e rimuove le impurità.
Nel complesso, l’idrossido di ammonio è una sostanza chimica versatile e ampiamente utilizzata, con applicazioni in vari settori. Tuttavia, è importante maneggiare l’idrossido di ammonio in modo sicuro, poiché può essere pericoloso se non maneggiato correttamente.
Domande:
L’idrossido di ammonio è solubile?
Sì, l’idrossido di ammonio è molto solubile in acqua. Forma una soluzione limpida, incolore, altamente alcalina con un odore caratteristico. La solubilità dell’idrossido di ammonio in acqua dipende dalla temperatura e dalla concentrazione, con temperature e concentrazioni più elevate che determinano una maggiore solubilità.
Qual è la formula chimica dell’idrossido di ammonio?
La formula chimica dell’idrossido di ammonio è NH4OH.
Qual è la formula dell’idrossido di ammonio?
La formula dell’idrossido di ammonio è NH4OH.
L’idrossido di ammonio è una base forte?
Sì, l’idrossido di ammonio è considerato una base forte. Si dissocia completamente in acqua per formare ioni idrossido (OH-) e ioni ammonio (NH4+), rendendolo molto alcalino con un pH di circa 11. Questa elevata alcalinità lo rende una sostanza chimica utile in varie applicazioni industriali e domestiche, come la pulizia e Regolazione del pH. Tuttavia, è importante maneggiare con cura l’idrossido di ammonio, poiché può essere corrosivo e pericoloso se non maneggiato correttamente.
nome composto nh4oh
Il nome del composto chimico di NH4OH è idrossido di ammonio.
nome nh4oh
Il nome di NH4OH è idrossido di ammonio.
