L’idrosolfito di sodio (Na2S2O4) è una polvere cristallina bianca utilizzata come agente riducente in vari settori come quello tessile e della carta. Rimuove il colore dai tessuti e dalla pasta di carta.
| Nome IUPAC | Ditionito di sodio |
| Formula molecolare | Na2S2O4 |
| numero CAS | 7775-14-6 |
| Sinonimi | Iposolfito di sodio, ditionato di sodio, solfossilato di sodio, idrogeno solfito di sodio |
| InChI | InChI=1S/2Na.H2O4S2/c;;1-5(2,3)4/h;;(H2,1,2,3,4)/q2*+1;/p-2 |
Proprietà dell’idrosolfito di sodio
Formula di idrosolfito di sodio
La formula chimica dell’idrosolfito di sodio è Na2S2O4. Ciò significa che ciascuna molecola di idrosolfito di sodio contiene due atomi di sodio, due atomi di zolfo e quattro atomi di ossigeno. La formula indica che il composto è costituito da ioni sodio caricati positivamente e ioni solfito caricati negativamente.
Massa molare dell’idrosolfito di sodio
La massa molare di Na2S2O4 è 174,11 g/mol. Questo valore si calcola sommando le masse atomiche degli elementi presenti in una molecola di Na2S2O4. La massa molare è un parametro importante in stechiometria e viene utilizzato per calcolare la quantità di sostanza in un dato campione del composto.
Punto di ebollizione dell’idrosolfito di sodio
Na2S2O4 è un composto stabile e non ha punto di ebollizione. Si decompone invece se riscaldato a temperature superiori a 150°C rilasciando anidride solforosa e vapore acqueo. La reazione di decomposizione è esotermica e occorre prestare attenzione quando si riscalda Na2S2O4.
Punto di fusione dell’idrosolfito di sodio
Il punto di fusione di Na2S2O4 è 300°C. A questa temperatura il composto solido si scioglie formando un liquido incolore. Il punto di fusione è un parametro importante nel determinare la stabilità del composto e la sua idoneità per diverse applicazioni.
Densità dell’idrosolfito di sodio g/ml
La densità di Na2S2O4 è 1,48 g/ml. Questo valore indica che Na2S2O4 è un composto relativamente denso rispetto all’acqua. La densità è un parametro importante nel determinare la solubilità del composto e la sua capacità di mescolarsi con altre sostanze.
Peso molecolare dell’idrosolfito di sodio
Il peso molecolare di Na2S2O4 è 174,11 g/mol. Questo valore si calcola sommando le masse atomiche degli elementi presenti in una molecola di Na2S2O4. Il peso molecolare è un parametro importante per determinare la quantità di sostanza in un dato campione del composto.
Struttura dell’idrosolfito di sodio
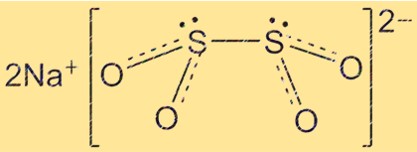
La struttura di Na2S2O4 è tetraedrica, con gli atomi di zolfo situati agli angoli del tetraedro e gli atomi di ossigeno che formano i bordi. Gli ioni sodio si trovano al centro del tetraedro. La struttura di Na2S2O4 è importante per comprenderne le proprietà chimiche e fisiche.
Solubilità dell’idrosolfito di sodio
Na2S2O4 è altamente solubile in acqua, con una solubilità di 58 g/100 mL a 20°C. La solubilità è influenzata dalla temperatura e dal pH, con una maggiore solubilità osservata a temperature più elevate e valori di pH più bassi. L’elevata solubilità di Na2S2O4 lo rende utile in varie applicazioni come l’industria tessile e della carta dove viene utilizzato come agente riducente.
| Aspetto | Polvere cristallina bianca |
| Peso specifico | 1.48 |
| Colore | Incolore |
| Odore | Inodore |
| Massa molare | 174,11 g/mole |
| Densità | 1,48 g/ml |
| Punto di fusione | 300°C |
| Punto di ebollizione | Si decompone a 150°C |
| Punto flash | Non applicabile |
| solubilità in acqua | Molto solubile |
| Solubilità | Solubile in acqua, glicerolo, etanolo |
| Pressione del vapore | Non applicabile |
| Densità del vapore | Non applicabile |
| pKa | 6.6 |
| pH | 7-8 (soluzione all’1%) |
Sicurezza e pericoli dell’idrosolfito di sodio
Na2S2O4 è generalmente sicuro se maneggiato e utilizzato correttamente, ma può comportare alcuni pericoli se maneggiato in modo errato o utilizzato in modo inappropriato. È classificato come sostanza pericolosa e può causare irritazione alla pelle e agli occhi se entra in contatto con queste parti del corpo. Anche l’inalazione di polvere o nebbia di Na2S2O4 può irritare il sistema respiratorio. Na2S2O4 è anche un agente riducente, il che significa che può reagire con altri prodotti chimici per produrre gas infiammabili o esplosivi. Per evitare incidenti e lesioni è necessario seguire misure di sicurezza adeguate, come indossare dispositivi di protezione e maneggiare la sostanza in aree ben ventilate.
| Simboli di pericolo | XI, C |
| Descrizione della sicurezza | Evitare il contatto con la pelle e gli occhi. Non inalare polvere o nebbia. Indossare dispositivi di protezione. Manipolare in aree ben ventilate. |
| Numeri di identificazione delle Nazioni Unite | UN1384 |
| Codice SA | 28311000 |
| Classe di pericolo | 4.2 |
| Gruppo di imballaggio | III |
| Tossicità | LD50: 1.520 mg/kg (orale, ratto); LC50: 1840 ppm/4h (inalazione, ratto) |
Metodi per la sintesi dell’idrosolfito di sodio
Esistono diversi metodi per sintetizzare Na2S2O4, ma i più comuni prevedono la reazione del bisolfito di sodio e del ditionito di sodio.
Un metodo prevede l’aggiunta di bisolfito di sodio a una soluzione di idrossido di sodio e ditionito di sodio, mentre un altro metodo prevede il riscaldamento di una miscela di bisolfito di sodio e ditionito di sodio.
La formazione di Na2S2O4 produce una polvere cristallina bianca che può essere raccolta e purificata utilizzando entrambi i metodi.
Un altro metodo per sintetizzare Na2S2O4 prevede la reazione tra anidride solforosa e boroidruro di sodio . La reazione produce Na2S2O4, borato di sodio e idrogeno gassoso. Questo metodo è generalmente meno comune dei metodi con bisolfito di sodio e ditionito di sodio.
Usi dell’idrosolfito di sodio
Na2S2O4 ha vari usi in diversi settori grazie alle sue proprietà uniche. Ecco alcuni dei suoi usi:
- Industria tessile: utilizzato come agente riducente nell’industria tessile per rimuovere la tintura e lo sbiancamento in eccesso dai tessuti.
- Industria della carta: utilizzato nell’industria della carta per sbiancare la pasta di legno e i prodotti di carta.
- Industria alimentare: utilizzato come additivo alimentare per prevenire lo scolorimento e come conservante nella frutta e nella verdura in scatola.
- Trattamento dell’acqua: utilizzato per rimuovere il cloro in eccesso nel trattamento dell’acqua potabile e delle acque reflue.
- Industria mineraria: utilizzato nell’industria mineraria per separare i minerali di rame e molibdeno.
- Industria dei polimeri: utilizzato nell’industria dei polimeri per ridurre il colore dei polimeri e della plastica.
- Industria fotografica: utilizzato nell’industria fotografica come fissatore fotografico per rimuovere gli alogenuri d’argento non esposti dalle stampe fotografiche.
- Altre applicazioni industriali: utilizzato in vari altri settori, come la lavorazione del cuoio, l’estrazione petrolifera e come agente riducente nelle reazioni di sintesi chimica.
Domande:
D: Quale detergente contiene idrosolfito di sodio?
R: Na2S2O4 è comunemente utilizzato nei detergenti domestici per rimuovere le macchie e come alternativa alla candeggina.
D: Qual è la funzione dell’idrosolfito di sodio nella reazione con l’indaco?
R: Na2S2O4 agisce come agente riducente nella reazione con l’indaco, che converte il colorante blu indaco insolubile in un composto solubile e incolore.
D: Dove acquistare idrosolfito di sodio?
R: Na2S2O4 può essere acquistato da fornitori di prodotti chimici, come Sigma-Aldrich, Fisher Scientific e VWR International.
D: Come neutralizzare l’idrosolfito di sodio?
R: Na2S2O4 può essere neutralizzato con idrossido di sodio o un’altra base forte.
D: Quali alimenti indiani utilizzano idrosolfito di sodio?
R: Na2S2O4 non è comunemente usato nei cibi indiani.
D: Come sbianca l’idrosolfito di sodio?
R: Na2S2O4 agisce come agente riducente e distrugge i legami chimici che danno colore al materiale, eliminando così il colore e portando allo sbiancamento.
D: Qual è la funzione dell’idrosolfito di sodio nella reazione con l’indaco?
R: Na2S2O4 agisce come agente riducente nella reazione con l’indaco, che converte il colorante blu indaco insolubile in un composto solubile e incolore.
D: Cosa produce odore quando si aggiunge idrosolfito di sodio?
R: Quando si aggiunge Na2S2O4, si potrebbe produrre un odore di zolfo dovuto al rilascio di gas di anidride solforosa.
D: L’idrosolfito di sodio diidrato è un agente riducente?
R: Sì, Na2S2O4 diidrato è un potente agente riducente comunemente utilizzato nei processi industriali.
