L’acetil cloruro o C2H3ClO è un liquido incolore e fumante con un odore pungente. Viene utilizzato principalmente come reagente nella sintesi organica e come agente acetilante nella produzione di prodotti farmaceutici e coloranti.
| Nome dell’UPAC | Cloruro di acetile |
| Formula molecolare | C2H3ClO |
| numero CAS | 75-36-5 |
| Sinonimi | Cloruro di etanoile, cloruro di acido acetico, cloruro acetico, cloruro di cloroacetile, AcCl |
| InChI | InChI=1S/C2H3ClO/c1-2(3)4/h1H3 |
Proprietà del cloruro di acetile
Massa molare del cloruro di acetile
L’acetil cloruro, con formula chimica C2H3ClO, ha una massa molare di circa 78,50 g/mol. Questo viene calcolato aggiungendo le masse atomiche di ciascun atomo nella molecola, che sono carbonio (12,01 g/mol), idrogeno (1,01 g/mol), cloro (35,45 g/mol) e ossigeno (16,00 g/mol). La massa molare del cloruro di acetile è importante nei calcoli stechiometrici per determinare la quantità di reagenti e prodotti nelle reazioni chimiche.
Punto di ebollizione del cloruro di acetile
Il punto di ebollizione del cloruro di acetile è 51,5°C (124,7°F) a pressione atmosferica standard. Questo basso punto di ebollizione, unito alla sua natura altamente reattiva, significa che l’acetil cloruro deve essere maneggiato con cautela in laboratorio. È un liquido incolore, fumante con un odore pungente che è altamente solubile in solventi polari come etanolo e acetone.
Punto di fusione del cloruro di acetile
C2H3ClO ha un punto di fusione di -112,1°C (-169,8°F) a pressione atmosferica standard. Ciò lo rende un composto altamente volatile e reattivo che richiede un’attenta manipolazione e conservazione.
Densità del cloruro di acetile g/mL
L’acetil cloruro ha una densità di 1,104 g/mL a 25°C (77°F). Ciò significa che C2H3ClO è più denso dell’acqua e affonderà in essa. La densità di C2H3ClO è importante per determinare la quantità di materiale che può essere immagazzinata in un dato volume, nonché le misure di sicurezza adeguate necessarie per maneggiare e immagazzinare il materiale.
Peso molecolare del cloruro di acetile
Il peso molecolare di C2H3ClO è 78,50 g/mol. Questo valore è importante per determinare la quantità di C2H3ClO necessaria nelle reazioni chimiche e per la conversione tra diverse unità di misura.
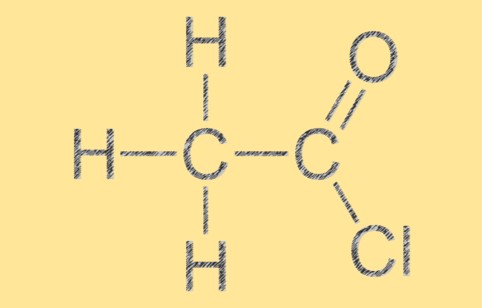
Struttura del cloruro di acetile
L’acetil cloruro ha una geometria molecolare planare trigonale, con l’atomo di carbonio al centro circondato da altri tre atomi in una disposizione triangolare piatta. La molecola ha un doppio legame C=O tra gli atomi di carbonio e ossigeno e un legame singolo tra gli atomi di carbonio e cloro. La struttura molecolare di C2H3ClO gli conferisce la sua caratteristica reattività e proprietà chimiche.
Formula del cloruro di acetile
La formula chimica dell’acetil cloruro è C2H3ClO, che rappresenta il numero e il tipo di atomi nella molecola. La formula è importante per i calcoli stechiometrici nelle reazioni chimiche e per identificare il composto in laboratorio. C2H3ClO viene utilizzato principalmente come reagente nella sintesi organica e come agente acetilante nella produzione di prodotti farmaceutici e coloranti.
| Aspetto | Liquido incolore |
| Peso specifico | 1.104 g/ml a 25°C |
| Colore | Incolore |
| Odore | Acri |
| Massa molare | 78,50 g/mole |
| Densità | 1.104 g/ml a 25°C |
| Punto di fusione | -112,1°C |
| Punto di ebollizione | 51,5°C |
| Punto flash | -26°C |
| solubilità in acqua | Reagisce violentemente con l’acqua |
| Solubilità | Solubile nella maggior parte dei solventi organici |
| Pressione del vapore | 69,7 mmHg a 25°C |
| Densità del vapore | 2,7 (aria=1) |
| pKa | -6.3 |
| pH | Molto acido |
Sicurezza e pericoli del cloruro di acetile
C2H3ClO è una sostanza altamente reattiva e pericolosa che comporta rischi significativi per la salute e la sicurezza umana. È una sostanza corrosiva e tossica che può causare gravi ustioni cutanee, danni agli occhi e irritazione respiratoria se esposta. L’acetil cloruro può anche reagire violentemente con l’acqua, producendo gas di acido cloridrico, che è irritante per le vie respiratorie. È importante maneggiare C2H3ClO con estrema cautela, indossando dispositivi di protezione individuale adeguati e utilizzandolo solo in un’area ben ventilata. Anche lo stoccaggio, l’etichettatura e il trasporto adeguati sono essenziali per prevenire incidenti e garantire una manipolazione sicura di questa sostanza.
| Simboli di pericolo | Corrosivo, tossico |
| Descrizione della sicurezza | Non respirare i vapori. Indossare guanti protettivi e proteggere gli occhi/il viso. In caso di incendio, utilizzare un estintore a CO2, prodotti chimici secchi o a schiuma. |
| Identificatori AN | UN1717 |
| Codice SA | 2915.90.9000 |
| Classe di pericolo | 8 |
| Gruppo di imballaggio | II |
| Tossicità | Molto tossico e corrosivo. Provoca gravi ustioni alla pelle e agli occhi. Può essere fatale se inalato o ingerito. |
Metodi per la sintesi dell’acetil cloruro
C2H3ClO viene prodotto facendo reagire l’acido acetico con cloruro di tionile, tricloruro di fosforo o pentacloruro di fosforo. Questi metodi comportano l’uso di reagenti altamente reattivi e pericolosi e devono essere utilizzati con estrema cautela.
Il metodo più comune per sintetizzare C2H3ClO prevede la reazione dell’acido acetico con cloruro di tionile. Questo metodo prevede tipicamente l’aggiunta di cloruro di tionile all’acido acetico in modo controllato, con un attento controllo della temperatura per prevenire il surriscaldamento e la decomposizione. La reazione produce C2H3ClO e anidride solforosa come sottoprodotto.
Un altro metodo per sintetizzare C2H3ClO prevede la reazione dell’acido acetico con tricloruro di fosforo o pentacloruro di fosforo. In questo metodo, l’acido acetico viene miscelato con tricloruro di fosforo o pentacloruro di fosforo e riscaldato per avviare la reazione. La reazione produce C2H3ClO e acido fosforico come sottoprodotto.
È importante notare che questi metodi comportano l’uso di sostanze chimiche altamente reattive e pericolose e devono essere eseguiti solo da chimici esperti in un’area ben ventilata con adeguati dispositivi di protezione individuale. Inoltre, la sintesi di C2H3ClO deve essere effettuata sotto una cappa aspirante per ridurre al minimo l’esposizione a gas tossici e corrosivi.
Usi del cloruro di acetile
L’acetil cloruro è un composto chimico versatile che trova molti usi nell’industria e nella ricerca. Alcuni degli usi comuni di C2H3ClO sono:
- Produzione di prodotti farmaceutici: vari prodotti farmaceutici, inclusi antidolorifici, antibiotici e anestetici, utilizzano C2H3ClO nella loro sintesi.
- Produzione di coloranti e profumi: la produzione di vari coloranti e profumi, come la cumarina utilizzata nei profumi e nei saponi, prevede l’uso di C2H3ClO.
- Produzione di polimeri: la produzione di diversi polimeri come il policarbonato e il cloruro di polivinile legati su C2H3ClO come reagente.
- Produzione di derivati acetilati: C2H3ClO svolge un ruolo cruciale nella produzione di derivati acetilati di composti come amminoacidi e alcol.
- Reazioni chimiche: C2H3ClO mostra un’elevata reattività, rendendolo un prezioso reagente in varie reazioni chimiche, comprese le reazioni di acetilazione e le reazioni di Friedel-Crafts.
- Ricerca di laboratorio: C2H3ClO trova frequente applicazione nella ricerca di laboratorio come reagente per reazioni chimiche e come solvente per vari composti.
È importante notare che C2H3ClO è una sostanza pericolosa e deve essere maneggiata con estrema cautela. È necessario seguire protocolli e normative di sicurezza adeguati quando si utilizza C2H3ClO per ridurre al minimo i rischi associati alla sua manipolazione e utilizzo.
