Il butadiene (C4H6) è un composto chimico versatile. Viene utilizzato nella produzione di gomma sintetica, plastica e vari altri prodotti grazie alla sua elasticità e resistenza.
| Nome IUPAC | buta-1,3-diene |
| Formula molecolare | C4H6 |
| numero CAS | 106-99-0 |
| Sinonimi | Divinile, bietilene, buta-1,3-diene, vinil etilene, eritrene |
| InChI | InChI=1S/C4H6/c1-3-4-2/h3-4H,1-2H2 |
Proprietà del butadiene
Formula del butadiene
La formula del butadiene è C4H6. È composto da quattro atomi di carbonio e sei atomi di idrogeno. Questa formula molecolare rappresenta la disposizione degli atomi nel butadiene e fornisce informazioni sulla sua composizione chimica.
Massa molare del butadiene
La massa molare del Buta-1,3-diene può essere calcolata sommando le masse atomiche dei suoi elementi costitutivi. Il carbonio ha una massa molare di circa 12,01 g/mol e l’idrogeno ha una massa molare di circa 1,01 g/mol. Pertanto, la massa molare del Buta-1,3-diene è di circa 54,09 g/mol.
Punto di ebollizione del butadiene
Il buta-1,3-diene ha un punto di ebollizione relativamente basso rispetto a molti altri composti. Bolle a circa -4,4 gradi Celsius o 24,1 gradi Fahrenheit. Questo basso punto di ebollizione consente una facile conversione del Buta-1,3-diene liquido allo stato gassoso.
Punto di fusione del butadiene
A differenza di molti composti organici, il Buta-1,3-diene non ha un punto di fusione distinto a causa della sua natura altamente reattiva e della tendenza a polimerizzare. Esiste invece come gas incolore a temperatura ambiente e pressione atmosferica.
Densità del butadiene g/mL
La densità del Buta-1,3-diene è di circa 0,63 g/mL. Questo valore indica che il Buta-1,3-diene è meno denso dell’acqua, che ha una densità di 1 g/mL. La bassa densità del Buta-1,3-diene contribuisce alla sua galleggiabilità e alla sua capacità di formare facilmente vapori.
Peso molecolare del butadiene
Il peso molecolare del Buta-1,3-diene è di circa 54,09 g/mol. Questo valore rappresenta la massa media di una molecola di Buta-1,3-diene, tenendo conto delle masse atomiche degli atomi di carbonio e idrogeno presenti nella sua struttura chimica.
Struttura del butadiene
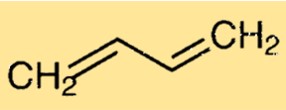
La struttura del Buta-1,3-diene è costituita da una catena di quattro atomi di carbonio legati insieme alternando legami singoli e doppi. Ogni atomo di carbonio è anche legato a due atomi di idrogeno. Questa struttura lineare conferisce al Buta-1,3-diene le sue proprietà e reattività caratteristiche.
Solubilità del butadiene
L’1,3-butadiene è scarsamente solubile in acqua ma si dissolve facilmente in solventi organici come benzene e toluene. La sua bassa solubilità in acqua è dovuta alle differenze di polarità tra il Buta-1,3-diene e le molecole d’acqua.
| Aspetto | Gas incolore |
| Peso specifico | 0,62 – 0,63 |
| Colore | Incolore |
| Odore | Odore leggero e aromatico |
| Massa molare | 54,09 g/mole |
| Densità | 0,62 – 0,63 g/ml |
| Punto di fusione | -138,4°C (-217,1°F) |
| Punto di ebollizione | -4,4°C (24,1°F) |
| Punto flash | -76°C (-105°F) |
| solubilità in acqua | Insolubile |
| Solubilità | Solubile in solventi organici (es. benzene, toluene) |
| Pressione del vapore | 448 mmHg a 20°C |
| Densità del vapore | 1.9 (Aria = 1) |
| pKa | ~43 (stimato) |
| pH | Neutro |
Sicurezza e pericoli del butadiene
L’1,3-butadiene comporta alcuni rischi per la sicurezza e occorre prestare attenzione quando lo si maneggia. È infiammabile e può formare miscele esplosive con l’aria. Pertanto, sono cruciali adeguate misure di ventilazione e prevenzione incendi. L’esposizione prolungata al Buta-1,3-diene può causare irritazione agli occhi, alla pelle e al sistema respiratorio. È anche considerato un potenziale cancerogeno e l’esposizione dovrebbe essere ridotta al minimo. Quando si lavora con Buta-1,3-diene è necessario utilizzare dispositivi di protezione come guanti, occhiali e respiratori. Le fuoriuscite devono essere contenute e ripulite tempestivamente. È importante seguire le linee guida di sicurezza, come quelle fornite dalle agenzie di regolamentazione, per garantire la manipolazione e lo stoccaggio sicuri del buta-1,3-diene.
| Simboli di pericolo | Infiammabile (F), Nocivo (Xn), Cancerogeno (C) |
| Descrizione della sicurezza | Tenere lontano da fonti di calore/scintille/fiamme libere. Utilizzare in aree ben ventilate. Evitare l’esposizione prolungata. Manipolare con guanti e indumenti protettivi. |
| Numeri di identificazione delle Nazioni Unite | ONU 1010 |
| Codice SA | 2903.14.00 |
| Classe di pericolo | 2.1 – Gas infiammabili |
| Gruppo di imballaggio | GE II |
| Tossicità | Considerato un potenziale cancerogeno e può causare irritazione respiratoria e cutanea. |
Metodi di sintesi del butadiene
Esistono diversi metodi per sintetizzare il Buta-1,3-diene, ciascuno con i propri vantaggi e limiti. Un metodo comune è il cracking con vapore di idrocarburi, come nafta o gas naturale liquidi.
In questo processo, il processo riscalda l’alimentazione di idrocarburi a temperature elevate, tipicamente intorno agli 800-900°C, in presenza di vapore. Ciò porta alla rottura dei legami carbonio-carbonio e alla formazione di Buta-1,3-diene.
Un altro metodo prevede la deidrogenazione catalitica del butene o dei butani. Utilizzando catalizzatori specifici, come ossidi metallici o metalli supportati, la reazione rimuove selettivamente gli atomi di idrogeno dal materiale di partenza, determinando la produzione di Buta-1,3-diene.
La dimerizzazione catalitica dell’acetilene produce anche Buta-1,3-diene. Questo processo prevede la reazione di due molecole di acetilene per formare Buta-1,3-diene, solitamente in presenza di un catalizzatore metallico come il rame.
Catalizzatori come l’allumina o le zeoliti facilitano la disidratazione dell’etanolo ad alte temperature. Questo processo forma attivamente Buta-1,3-diene.
Inoltre, alcuni impianti producono buta-1,3-diene come sottoprodotto della produzione di etilene attraverso il processo di cracking della nafta o del gasolio. Questo metodo sfrutta le reazioni di cracking per generare una miscela di olefine, incluso Buta-1,3-diene.
Questi metodi di sintesi svolgono un ruolo cruciale nella produzione di Buta-1,3-diene, fornendo diversi percorsi per soddisfare la domanda di questa importante sostanza chimica in settori quali la produzione di gomma, plastica e fibre sintetiche. .
Usi del butadiene
Il buta-1,3-diene trova applicazione in un’ampia gamma di settori grazie alle sue proprietà versatili. Ecco alcuni usi chiave del Buta-1,3-diene:
- Gomma sintetica: la produzione di gomma sintetica, come la gomma stirene-buta-1,3-diene (SBR) e la gomma polibuta-1,3-diene (PBR), utilizza principalmente gomma 1,3-buta-diene. Queste gomme forniscono eccellente elasticità, resilienza e resistenza all’abrasione, rendendole ideali per pneumatici, componenti automobilistici, nastri trasportatori e calzature.
- Materie plastiche: l’1,3-buta-diene è un monomero essenziale per la produzione di varie plastiche, tra cui le plastiche acrilonitrile-buta-1,3-diene-stirene (ABS) e stirene-buta-1,3-diene (SB) . Queste plastiche presentano una migliore resistenza agli urti, resistenza al calore e stabilità dimensionale, che le rendono preziose per applicazioni in beni di consumo, elettrodomestici e componenti automobilistici.
- Adesivi: le forti capacità di legame dei polimeri a base di 1,3-butadiene li rendono un componente prezioso nelle formulazioni adesive. Forniscono adesione a un’ampia gamma di substrati, rendendoli utili per applicazioni di incollaggio in settori quali l’edilizia, la lavorazione del legno e l’imballaggio.
- Rivestimenti: l’1,3-butadiene contribuisce alla produzione di rivestimenti e vernici con durabilità, flessibilità e proprietà di adesione migliorate. Le resine, come le resine epossidiche e alchidiche, lo utilizzano nella loro sintesi, costituendo componenti essenziali dei rivestimenti protettivi per metalli, calcestruzzo e altre superfici.
- Tessili e fibre: la produzione di fibre sintetiche, come le fibre di acrilonitrile-buta-1,3-diene (AB), utilizza buta-1,3-diene. Queste fibre possiedono un’elevata resistenza, una buona stabilità dimensionale e resistenza agli agenti chimici, che le rendono adatte per tessuti, tappeti e tessuti industriali.
- Additivi per carburanti: il buta-1,3-diene migliora il numero di ottano della benzina come additivo per carburanti utilizzato nella sua produzione. Migliora le proprietà di combustione della benzina, con conseguente miglioramento delle prestazioni del motore e riduzione delle emissioni.
Queste applicazioni evidenziano l’ampia utilità del Buta-1,3-diene in vari settori, contribuendo allo sviluppo di vari prodotti che incontriamo nella nostra vita quotidiana.
Domande:
D: Cos’è il butadiene?
R: Il buta-1,3-diene è un composto chimico con la formula molecolare C4H6, costituito da una catena di quattro atomi di carbonio e due doppi legami.
D: Qual è il nome IUPAC del prodotto principale quando l’1,3-butadiene reagisce con quantità uguali di HCl?
R: Il prodotto principale, secondo la nomenclatura IUPAC, è il 3-clorobut-1-ene.
D: Quanti atomi di H contiene la molecola 1,3-butadiene?
R: Il buta-1,3-diene contiene sei atomi di idrogeno (H) in totale.
D: Qual è la relazione tra le forme s-cis e s-trans dell’1,3-butadiene?
R: Le forme s-cis e s-trans dell’1,3-butadiene sono isomeri geometrici, che differiscono nella disposizione dei sostituenti attorno ai doppi legami.
D: Qual è il numero totale di nodi nel ψ3 MO dell’1,3-butadiene?
R: L’orbitale molecolare ψ3 dell’1,3-butadiene contiene un totale di tre nodi.
D: Quanti legami OM ha il butadiene?
R: Il butadiene ha tre orbitali molecolari di legame (MO) formati da orbitali atomici sovrapposti.
D: Qual è l’assorbimento previsto di butadiene?
R: Si prevede che il butadiene assorba la luce ultravioletta (UV) nell’intervallo compreso tra 190 e 200 nm circa a causa del suo sistema coniugato.
