Il cianuro di idrogeno è un composto altamente tossico utilizzato nelle industrie, noto per i suoi effetti mortali sul sistema respiratorio. È incolore, ha un odore distinto e presenta rischi significativi per la salute umana.
| Nome IUPAC | Acido cianidrico |
| Formula molecolare | HCN |
| numero CAS | 74-90-8 |
| Sinonimi | Acido prussico, Formonitrile, Acido cianidrico, Acido cianidrico |
| InChI | InChI=1S/CHN/c1-2/h1H |
Proprietà dell’acido cianidrico
Formula del cianuro di idrogeno
La formula dell’acido cianidrico è HCN. È costituito da un atomo di idrogeno (H) legato a un atomo di carbonio (C) attraverso un triplo legame e l’atomo di carbonio è ulteriormente legato a un atomo di azoto (N). Questa semplice formula molecolare rappresenta la composizione dell’acido cianidrico.
Massa molare del cianuro di idrogeno
La massa molare dell’acido cianidrico è di circa 27,03 grammi per mole. Si calcola sommando le masse atomiche di idrogeno (H), carbonio (C) e azoto (N) presenti in una molecola di acido cianidrico.
Punto di ebollizione dell’acido cianidrico
Il cianuro di idrogeno ha un punto di ebollizione di circa 25,7 gradi Celsius (78,3 gradi Fahrenheit). A questa temperatura, l’acido cianidrico passa dallo stato liquido a quello gassoso, emettendo fumi tossici.
Punto di fusione dell’acido cianidrico
Il punto di fusione dell’acido cianidrico è di circa -13,4 gradi Celsius (7,9 gradi Fahrenheit). A questa temperatura l’acido cianidrico passa dallo stato solido a quello liquido.
Densità dell’acido cianidrico g/mL
La densità dell’acido cianidrico è di circa 0,687 grammi per millilitro. Questo valore di densità rappresenta la massa di acido cianidrico per unità di volume.
Peso molecolare del cianuro di idrogeno
Il peso molecolare dell’acido cianidrico è di circa 27,03 grammi per mole. Si determina sommando i pesi atomici dei suoi elementi costitutivi.
Struttura dell’acido cianidrico
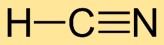
Il cianuro di idrogeno ha una struttura molecolare lineare, con l’atomo di idrogeno (H) legato all’atomo di carbonio (C) e l’atomo di carbonio (C) legato all’atomo di azoto (N). Il triplo legame tra carbonio e azoto conferisce stabilità alla molecola.
Solubilità dell’acido cianidrico
L’acido cianidrico è molto solubile in acqua. Si dissolve facilmente in acqua, formando una soluzione incolore. Questa solubilità consente all’acido cianidrico di mescolarsi e interagire facilmente con altre sostanze in varie applicazioni e ambienti.
| Aspetto | Gas incolore |
| Peso specifico | 0,687 |
| Colore | Incolore |
| Odore | Odore distinto |
| Massa molare | 27,03 g/mole |
| Densità | 0,687 g/ml |
| Punto di fusione | -13,4°C (-7,9°F) |
| Punto di ebollizione | 25,7°C (78,3°F) |
| Punto flash | -17,8°C (0°F) |
| solubilità in acqua | Miscibile con acqua |
| Solubilità | Solubile in solventi organici come etere e alcool etilico |
| Pressione del vapore | 500 mmHg a 20°C |
| Densità del vapore | 0,95 |
| pKa | 9.3 |
| pH | 5.6 (acido cianidrico diluito) |
Sicurezza e pericoli del cianuro di idrogeno
Il cianuro di idrogeno comporta notevoli rischi per la sicurezza e deve essere maneggiato con estrema cautela. È altamente tossico se inalato, ingerito o assorbito attraverso la pelle. L’esposizione all’acido cianidrico può causare gravi difficoltà respiratorie, arresto cardiaco e persino la morte. È importante garantire una ventilazione adeguata e utilizzare dispositivi di protezione individuale quando si lavora con o in prossimità dell’acido cianidrico. Inoltre, il composto è infiammabile e può formare miscele esplosive con l’aria. Lo stoccaggio deve essere effettuato in contenitori ermeticamente chiusi, lontano da fonti di ignizione. Dovrebbero essere messi in atto protocolli di emergenza, come la fornitura di assistenza medica immediata e l’evacuazione delle aree colpite, per mitigare i rischi associati all’esposizione all’acido cianidrico.
| Simboli di pericolo | Teschio e ossa incrociate |
| Descrizione della sicurezza | Molto tossico; maneggiare con estrema cautela |
| Numeri di identificazione delle Nazioni Unite | UN1051 (Acido cianidrico) |
| Codice SA | 2811.11.00 |
| Classe di pericolo | 6.1 (Sostanze tossiche) |
| Gruppo di imballaggio | Io (Grande pericolo) |
| Tossicità | Estremamente tossico; può essere fatale anche in piccole quantità |
Metodi di sintesi dell’acido cianidrico
Vari metodi possono sintetizzare l’acido cianidrico.
Un metodo comune è il processo Andrussow. In questo processo, i catalizzatori di platino o rodio facilitano la reazione dell’ammoniaca (NH₃) e del metano (CH₄) con l’ossigeno (O₂) per sintetizzare l’acido cianidrico. La reazione avviene a temperature elevate, solitamente intorno ai 1000-1200°C. Il metano agisce come agente riducente, convertendo l’ossigeno in acqua (H₂O), mentre l’ammoniaca fornisce la fonte di azoto. La miscela risultante subisce una serie di reazioni che portano alla formazione di acido cianidrico (HCN) e vapore acqueo.
Un altro metodo per sintetizzare l’acido cianidrico è il processo BMA. Ciò comporta la reazione del metano (CH₄) con l’ammoniaca (NH₃) in presenza di un catalizzatore, come rame o nichel, ad alta temperatura. Questo processo genera acido cianidrico e altri sottoprodotti.
Il processo Andrussov-Noddack produce acido cianidrico facendo reagire il cianuro di sodio (NaCN) con un acido forte, come l’acido solforico (H₂SO₄).
Vale la pena ricordare che l’acido cianidrico è un composto altamente tossico e la sua sintesi deve essere effettuata con grande attenzione in strutture ben attrezzate, seguendo adeguati protocolli di sicurezza. L’uso di attrezzature specializzate, un’adeguata ventilazione e il rispetto delle istruzioni di sicurezza sono essenziali per garantire il benessere del personale coinvolto nel processo di sintesi.
Usi del cianuro di idrogeno
Il cianuro di idrogeno trova applicazioni in vari settori grazie alle sue proprietà uniche. Ecco alcuni dei suoi usi:
- Produzione chimica: l’acido cianidrico svolge un ruolo cruciale nella sintesi di diverse sostanze chimiche importanti, tra cui l’adiponitrile (un componente chiave nella produzione del nylon), il metil metacrilato (utilizzato per la plastica acrilica) e il cianuro di sodio (utilizzato nell’estrazione dell’oro).
- Prodotti farmaceutici: la produzione di prodotti farmaceutici, come vitamine, aminoacidi sintetici e alcuni antibiotici, si basa sull’acido cianidrico.
- Fumigazione: le industrie utilizzano l’acido cianidrico come fumigante per controllare i parassiti, soprattutto in spazi chiusi come serre, stive delle navi e impianti di stoccaggio del grano.
- Placcatura dei metalli: le industrie metallurgiche utilizzano l’acido cianidrico per i processi di galvanica per fornire uno strato protettivo sulle superfici metalliche.
- Produzione di polimeri: il cianuro di idrogeno partecipa attivamente alla produzione di fibre sintetiche, gomma e resine.
- Insetticidi: alcuni insetticidi contengono principi attivi derivati dall’acido cianidrico per fornire un efficace controllo dei parassiti in agricoltura e silvicoltura.
- Reagente di laboratorio: Il cianuro di idrogeno funge da reagente in varie reazioni chimiche e procedure di laboratorio.
- Estrazione mineraria: nell’estrazione dell’oro e dell’argento, l’acido cianidrico agisce come un reagente chimico per estrarre i metalli preziosi dai minerali.
- Produzione di gomma sintetica: il cianuro di idrogeno funge da materia prima nella produzione di gomma sintetica, come la gomma stirene-butadiene (SBR).
- Coloranti e pigmenti: la produzione di coloranti e pigmenti prevede l’uso di acido cianidrico, che contribuisce alle loro proprietà coloranti.
Sebbene l’acido cianidrico abbia i suoi usi, è importante maneggiarlo con grande cura a causa della sua elevata tossicità. Protocolli di sicurezza rigorosi e il rispetto di procedure di manipolazione adeguate sono essenziali per ridurre al minimo i rischi associati al suo utilizzo.
Domande:
D: A cosa serve l’acido cianidrico?
R: Il cianuro di idrogeno viene utilizzato nella produzione chimica, nella produzione farmaceutica, nella fumigazione, nella placcatura dei metalli, negli insetticidi e come reagente di laboratorio, tra le altre applicazioni.
D: Qual è la formula chimica dell’acido cianidrico?
R: La formula chimica dell’acido cianidrico è HCN.
D: Quali sono gli “usi consentiti” dell’acido cianidrico?
R: Gli “scopi consentiti” di HCN includono il suo utilizzo approvato e regolamentato in specifici processi industriali, ricerca e altre applicazioni consentite.
D: In cosa si trova l’acido cianidrico?
R: Il cianuro di idrogeno può essere trovato in vari prodotti chimici, ambienti industriali e fonti naturali come alcune piante e semi.
D: Dove è possibile acquistare l’acido cianidrico?
R: L’acquisto di acido cianidrico è altamente limitato e regolamentato a causa della sua tossicità e del potenziale uso improprio.
D: Cos’è l’acido cianidrico?
R: Il cianuro di idrogeno è un composto altamente tossico e volatile con un odore distinto, comunemente utilizzato nei processi industriali.
D: L’acido cianidrico è polare o non polare?
R: Il cianuro di idrogeno è una molecola polare a causa della presenza di legami polari e di una distribuzione asimmetrica della densità elettronica.
D: Quale parola o frase di due parole descrive meglio la forma della molecola di cianuro di idrogeno (HCN)?
R: La forma della molecola HCN è lineare.
D: A cosa serve l’acido cianidrico?
R: Il cianuro di idrogeno viene utilizzato in vari settori per la sintesi chimica, la fumigazione, la placcatura dei metalli, gli insetticidi e la produzione farmaceutica.
D: È stato utilizzato l’acido cianidrico in un attacco terroristico?
R: Sì, l’HCN è stato utilizzato in passato come arma chimica negli attacchi terroristici.
D: Quali sono gli altri nomi chimici associati al cianuro di idrogeno?
R: Altri nomi chimici associati all’HCN includono acido prussico, formonitrile, acido cianidrico e acido cianidrico.
D: Qual è il diagramma a punti di Lewis corretto per l’acido cianidrico?
R: Il diagramma a punti di Lewis corretto per l’HCN include l’atomo di idrogeno (H) legato all’atomo di carbonio (C) tramite un legame singolo e l’atomo di carbonio (C) legato all’atomo di azoto (N) tramite un triplo legame.
D: Qual è la carica degli atomi di acido cianidrico?
R: Nell’HCN, l’atomo di idrogeno (H) ha una carica parziale positiva, l’atomo di carbonio (C) ha una carica parziale negativa e l’atomo di azoto (N) ha una carica parziale negativa.
D: Cosa ti fa una capsula di acido cianidrico?
R: In contesti altamente regolamentati e controllati, una capsula HCN può essere utilizzata come mezzo di autosomministrazione rapido e letale, solitamente per scopi nascosti o di emergenza.
D: Che tipo di legame è il legame carbonio-azoto in una molecola di acido cianidrico (HCN)?
R: Il legame carbonio-azoto in una molecola HCN è un triplo legame.
