Il 2-esanolo è un alcol con sei atomi di carbonio. Ha un gruppo ossidrile (-OH) attaccato al secondo atomo di carbonio, rendendolo utile in varie applicazioni industriali e come ingrediente di profumi.
| Nome IUPAC | 2-esanolo |
| Formula molecolare | C6H14O |
| numero CAS | 626-93-7 |
| Sinonimi | Esan-2-olo, n-esanolo, alcol esilico |
| InChI | InChI=1S/C6H14O/c1-3-5-6(7)4-2/h6-7H,3-5H2,1-2H3 |
Proprietà del 2-esanolo
Formula del 2-esanolo
La formula chimica del 2-esanolo è C6H14O. È costituito da sei atomi di carbonio, quattordici atomi di idrogeno e un atomo di ossigeno. La formula rappresenta l’esatta composizione della molecola, fornendo preziose informazioni sui suoi costituenti elementari.
Massa molare del 2-esanolo
La massa molare dell’esan-2-olo viene calcolata sommando le masse atomiche di tutti i suoi atomi costituenti. Con sei atomi di carbonio, quattordici atomi di idrogeno e un atomo di ossigeno, la massa molare dell’esan-2-olo è di circa 102,18 grammi per mole. Questo valore è cruciale per vari calcoli e conversioni chimiche.
Punto di ebollizione del 2-esanolo
Il punto di ebollizione dell’esan-2-olo è la temperatura alla quale cambia da liquido a gas sotto pressione atmosferica standard. l’esan-2-olo ha un punto di ebollizione compreso tra circa 157 e 158 gradi Celsius (da 315 a 316 gradi Fahrenheit). Questo punto di ebollizione relativamente alto lo rende adatto per applicazioni in cui è richiesta resistenza al calore.
Punto di fusione del 2-esanolo
Il punto di fusione dell’esan-2-olo è la temperatura alla quale passa dallo stato solido a quello liquido. l’esan-2-olo ha un punto di fusione di circa -47 gradi Celsius (-53 gradi Fahrenheit). Questo basso punto di fusione indica che è un liquido alla temperatura ambiente più normale.
Densità del 2-esanolo g/mL
La densità dell’esan-2-olo si riferisce alla massa della sostanza per unità di volume. l’esan-2-olo ha una densità di circa 0,811 grammi per millilitro (g/mL). Questo valore di densità dà un’idea di quanto compatta o concentrata sia la sostanza.
Peso molecolare del 2-esanolo
Il peso molecolare dell’esan-2-olo è la somma dei pesi atomici di tutti gli atomi nella sua formula chimica. Con una formula molecolare C6H14O, l’esan-2-olo ha un peso molecolare di circa 102,18 grammi per mole. Questo valore viene utilizzato in vari calcoli e misurazioni chimiche.
Struttura del 2-esanolo
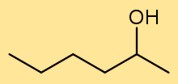
La struttura dell’esan-2-olo è costituita da una catena di sei atomi di carbonio con un gruppo ossidrile (-OH) attaccato al secondo atomo di carbonio. Questa disposizione gli conferisce le sue proprietà e reattività caratteristiche. La struttura può essere visualizzata come una catena diritta con il gruppo ossidrile ramificato nella seconda posizione del carbonio.
Solubilità del 2-esanolo
L’esan-2-olo è moderatamente solubile in acqua. Può mescolarsi con l’acqua in una certa misura a causa della presenza del gruppo ossidrile. Tuttavia, la sua solubilità diminuisce con l’aumentare della lunghezza della catena di carbonio. È più solubile in solventi organici come etanolo, acetone e cloroformio. La solubilità dell’esan-2-olo in diversi solventi influenza le sue applicazioni e il comportamento in vari sistemi.
| Aspetto | Liquido incolore |
| Peso specifico | 0,811 g/ml |
| Colore | Incolore |
| Odore | Odore caratteristico |
| Massa molare | 102,18 g/mole |
| Densità | 0,811 g/ml |
| Punto di fusione | -47°C (-53°F) |
| Punto di ebollizione | 157-158°C (315-316°F) |
| Punto flash | 58°C (136°F) |
| solubilità in acqua | Solubilità moderata |
| Solubilità | Solubile in solventi organici come etanolo, acetone e cloroformio |
| Pressione del vapore | 0,48 mmHg a 25°C |
| Densità del vapore | 3,5 (Aria = 1) |
| pKa | 16.3 |
| pH | Circa neutro (intorno a pH 7) |
Si prega di notare che i valori forniti sono approssimativi e possono variare a seconda delle condizioni e delle fonti specifiche.
Sicurezza e pericoli del 2-esanolo
L’esan-2-olo comporta alcuni rischi per la sicurezza che devono essere considerati. È importante maneggiare questa sostanza chimica con cautela. Il contatto diretto con l’esan-2-olo può causare irritazione alla pelle e agli occhi. L’ingestione o l’inalazione di elevate concentrazioni può causare difficoltà respiratorie. Si consiglia di indossare dispositivi di protezione adeguati, come guanti e occhiali protettivi, quando si lavora con l’esan-2-olo. Una ventilazione adeguata è fondamentale per prevenire l’accumulo di vapori. In caso di esposizione accidentale, è necessario consultare immediatamente un medico. È essenziale conservare e trasportare l’esan-2-olo in contenitori ermeticamente chiusi, lontano da fonti di ignizione per ridurre al minimo il rischio di incendio.
| Simboli di pericolo | Xi (irritante) |
| Descrizione della sicurezza | Evitare il contatto con gli occhi e la pelle. Utilizzare con ventilazione adeguata. Indossare indumenti e guanti protettivi. |
| Numeri di identificazione delle Nazioni Unite | ONU 2282 |
| Codice SA | 2905.12.00 |
| Classe di pericolo | 3 (Liquido infiammabile) |
| Gruppo di imballaggio | III |
| Tossicità | Moderatamente tossico; nocivo se ingerito o |
| inalato |
Metodi per la sintesi del 2-esanolo
Esistono diversi metodi per sintetizzare l’esan-2-olo.
Un approccio comune è il metodo dell’idroborazione-ossidazione. In questo processo, l’1-esene, un alchene, reagisce con il borano (BH3) in presenza di un solvente come il tetraidrofurano (THF). Questa fase di idroborazione porta alla formazione di un intermedio organoborano. L’ossidazione dell’intermedio produce esan-2-olo utilizzando perossido di idrogeno (H2O2) o perborato di sodio (NaBO3).
Un altro metodo prevede l’idrogenazione catalitica del 2-esanone. Per ottenere l’esan-2-olo, la riduzione del 2-esanone avviene utilizzando un catalizzatore come platino (Pt), palladio (Pd) o nichel (Ni) in presenza di una fonte di idrogeno. Questa reazione di idrogenazione converte il gruppo funzionale chetone in un gruppo ossidrile, dando luogo alla formazione di esan-2-olo.
La reazione di Grignard sintetizza l’esan-2-olo facendo reagire un reagente di Grignard, come il bromuro di metilmagnesio (CH3MgBr), con formaldeide (CH2O) o paraformaldeide (CH2O)n in un solvente etereo. La reazione produce un intermedio che subisce idrolisi, con conseguente produzione di esan-2-olo.
Questi metodi sintetici forniscono percorsi per la produzione di esan-2-olo su scala di laboratorio e industriale. La scelta del metodo dipende da fattori quali la disponibilità delle materie prime, la purezza desiderata e l’efficienza del processo.
Usi del 2-esanolo
L’esan-2-olo trova un’ampia gamma di applicazioni grazie alle sue proprietà versatili. Ecco alcuni usi chiave di Hexan-2-ol:
- L’esan-2-olo trova applicazione come solvente in vari settori, tra cui vernici, rivestimenti e prodotti per la pulizia.
- Profumi, saponi e prodotti per la cura personale utilizzano Hexan-2-ol come ingrediente profumato a causa del suo odore gradevole.
- I produttori utilizzano Hexan-2-ol nella produzione di plastificanti, che migliorano la flessibilità e la durata della plastica.
- La sintesi di altre sostanze chimiche, come gli esteri ampiamente utilizzati negli aromi, nei profumi e nei prodotti farmaceutici, si riferisce all’esan-2-olo come precursore.
- L’esan-2-olo svolge un ruolo essenziale nelle applicazioni agricole come intermedio nella produzione di erbicidi e insetticidi.
- A causa della sua natura infiammabile, l’Hexan-2-olo trova applicazione come additivo per carburanti o come componente nei biocarburanti.
- L’industria farmaceutica utilizza l’esan-2-olo come solvente per formulazioni di farmaci e come materia prima nella sintesi di composti farmaceutici.
- L’esan-2-olo viene utilizzato per creare sapori e aromi per prodotti alimentari, migliorando l’esperienza sensoriale complessiva.
- L’esan-2-olo funge da inibitore della corrosione nella lavorazione dei metalli e nei processi industriali, proteggendo dalla degradazione.
- La chimica analitica utilizza l’esan-2-olo come standard di riferimento e i laboratori di ricerca lo utilizzano per una varietà di scopi sperimentali.
Queste diverse applicazioni evidenziano la versatilità dell’esan-2-olo in diversi settori, dimostrando la sua importanza come composto chimico prezioso.
Domande:
D: Qual è il prodotto principale della disidratazione E1 del 2-esanolo?
R: Il prodotto principale della disidratazione E1 dell’esan-2-olo è il 2-esene, un alchene.
D: Qual è il prodotto predominante della reazione del 2-esanolo con H2CrO4?
R: Il prodotto predominante della reazione dell’esan-2-olo con H2CrO4 è il 2-esanone, un chetone.
D: Quali prodotti si otterrebbero dalla disidratazione del 2-esanolo?
R: I prodotti ottenuti dalla disidratazione dell’esan-2-olo sono principalmente 2-esene e acqua.
D: Qual è la sintesi della reazione di Grignard del meccanismo del 2-metil-2-esanolo?
R: Nella sintesi della reazione di Grignard del 2-metil-2-esanolo, un reagente di Grignard reagisce con la formaldeide per formare un intermedio, che viene poi idrolizzato per dare 2-metil-2-esanolo.
D: Qual è il valore Rf del prodotto 2-esanolo?
R: Il valore Rf per l’esan-2-olo può variare a seconda delle condizioni sperimentali specifiche e della fase mobile utilizzata nella separazione cromatografica.
D: Quale composto, quando reagisce con H2SO4 e acqua, produrrà 2-esanolo?
R: Il composto 2-esene, quando reagisce con H2SO4 e acqua, produrrà esan-2-olo tramite idratazione catalizzata da acido.
