Il decano (C10H22) è un composto idrocarburico contenente dieci atomi di carbonio disposti in una catena lineare. È comunemente usato come solvente in varie applicazioni industriali, come i processi di pulizia e produzione.
| Nome IUPAC | Decano |
| Formula molecolare | C10H22 |
| numero CAS | 124-18-5 |
| Sinonimi | n-Decano, Decil idruro, n-Amilmetina, Capdecano |
| InChI | InChI=1S/C10H22/c1-3-5-7-9-10-8-6-4-2/h3-10H2,1-2H3 |
Proprietà del decano
Formula del decano
La formula del decano è C10H22. Rappresenta un composto idrocarburico composto da dieci atomi di carbonio e ventidue atomi di idrogeno. La formula mostra il numero e il tipo esatto di atomi presenti in una molecola di decano.
Massa molare del decano
La massa molare dell’idruro decilico può essere calcolata sommando le masse atomiche dei suoi elementi costitutivi. La massa molare del carbonio (C) è 12,01 g/mol e la massa molare dell’idrogeno (H) è 1,008 g/mol. Pertanto, la massa molare dell’idruro decilico è di circa 142,28 g/mol.
Punto di ebollizione del decano
Il decano ha un punto di ebollizione di circa 174°C (345°F). Ciò significa che alla normale pressione atmosferica, l’idruro decilico inizia a vaporizzare e trasformarsi in uno stato gassoso a quella temperatura. Il punto di ebollizione è una caratteristica importante dell’idruro decilico e viene utilizzato per determinarne le proprietà fisiche e le applicazioni.
Punto di fusione del decano
Il punto di fusione dell’idruro decilico è di circa -29°C (-20°F). Ciò significa la temperatura alla quale l’idruro decilico passa dallo stato solido allo stato liquido. Questo basso punto di fusione rende l’idruro decilico facilmente liquefacibile in condizioni normali.
Densità del decano g/mL
L’idruro di decile ha una densità di circa 0,73 g/mL. La densità è la misura della massa per unità di volume. La densità dell’idruro decilico indica la sua relativa pesantezza o leggerezza rispetto ad un uguale volume d’acqua. La bassa densità dell’idruro decilico suggerisce che sia più leggero dell’acqua.
Peso molecolare del decano
Il peso molecolare dell’idruro decilico è di circa 142,28 g/mol. Si calcola sommando i pesi atomici di tutti gli atomi in una molecola di idruro decilico. Il peso molecolare fornisce preziose informazioni sulla dimensione e sulla massa della molecola di idruro decilico.
Struttura del decano
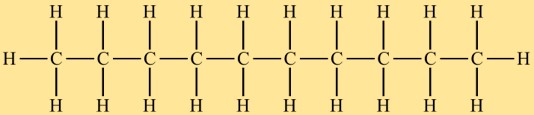
L’idruro di decile ha una struttura a catena lineare, con dieci atomi di carbonio collegati insieme in una disposizione lineare. Ogni atomo di carbonio forma quattro singoli legami covalenti con gli atomi di idrogeno circostanti. La catena di carbonio dell’idruro decilico non è ramificata e questa caratteristica strutturale influenza le sue proprietà chimiche e fisiche.
Solubilità del decano
L’idruro decilico è insolubile in acqua ma solubile in solventi non polari come benzene, etere ed esano. La sua natura non polare ostacola la sua interazione con sostanze polari come l’acqua. La solubilità dell’idruro di decile è una considerazione importante in vari processi e applicazioni industriali, in particolare quando si ha a che fare con solventi non polari.
| Aspetto | Liquido incolore |
| Peso specifico | 0,73 |
| Colore | Incolore |
| Odore | Inodore |
| Massa molare | 142,28 g/mole |
| Densità | 0,73 g/ml |
| Punto di fusione | -29°C (-20°F) |
| Punto di ebollizione | 174°C (345°F) |
| Punto flash | 43°C (109°F) |
| solubilità in acqua | Insolubile |
| Solubilità | Solubile in solventi non polari come benzene, etere ed esano |
| Pressione del vapore | 1,22 mmHg a 20°C |
| Densità del vapore | 4,88 (aria = 1) |
| pKa | Non applicabile |
| pH | Neutro |
Sicurezza e pericoli di Decane
L’idruro di decile presenta alcune considerazioni e pericoli sulla sicurezza. È infiammabile e deve essere maneggiato con cautela poiché potrebbe incendiarsi se esposto a fiamme libere o scintille. Il vapore dell’idruro di decile è più pesante dell’aria, il che significa che può viaggiare lungo il terreno e accumularsi in aree basse, presentando un potenziale pericolo di incendio o esplosione. Il contatto diretto con l’idruro decilico può causare irritazione alla pelle e può anche causare irritazione agli occhi. È importante utilizzare misure protettive adeguate, come guanti e occhiali protettivi, quando si lavora con l’idruro decilico. Una ventilazione adeguata è fondamentale per ridurre al minimo la concentrazione di vapori di idruro decilico negli spazi chiusi.
| Simboli di pericolo | Infiammabile |
| Descrizione della sicurezza | – Tenere lontano da fiamme libere, – Utilizzare in aree ben ventilate – Indossare guanti e occhiali protettivi, – Evitare il contatto diretto con la pelle e gli occhi |
| Identificatori delle Nazioni Unite | ONU 2247 |
| Codice SA | 2901.10.00 |
| Classe di pericolo | Classe 3 (Liquido infiammabile) |
| Gruppo di imballaggio | GE II |
| Tossicità | Bassa tossicità |
Metodi di sintesi del decano
Esistono diversi metodi per sintetizzare l’idruro decilico.
- Un metodo comune per sintetizzare l’idruro di decile consiste nel far reagire il decene con idrogeno gassoso in presenza di un catalizzatore adatto, come palladio o nichel. Questo processo satura i doppi legami carbonio-carbonio del decene, convertendolo in idruro decilico.
- Un altro metodo è l’oligomerizzazione dell’etilene , in cui i catalizzatori, solitamente complessi di metalli di transizione, combinano molecole di etilene per formare idrocarburi a peso molecolare più elevato, compreso l’idruro decilico.
- I processi di raffinazione del petrolio producono anche idruro di decile. In questo processo, la distillazione del petrolio greggio separa e purifica una frazione contenente idruro di decile e idrocarburi simili per ottenere idruro di decile puro.
- Il processo Fischer-Tropsch consente la sintesi dell’idruro decilico facendo reagire monossido di carbonio e idrogeno su un catalizzatore, solitamente un catalizzatore di ferro o cobalto, in condizioni di elevata temperatura e pressione. Questo processo si traduce in una miscela di idrocarburi, incluso l’idruro di decile.
È fondamentale sottolineare che questi metodi di sintesi su scala industriale richiedono attrezzature e competenze specializzate. La scelta del metodo di sintesi dipende da fattori quali la disponibilità delle materie prime, la purezza desiderata e considerazioni economiche.
Usi del decano
L’idruro di decile trova varie applicazioni in diversi settori grazie alle sue proprietà e caratteristiche. Alcuni usi comuni dell’idruro decilico includono:
- Solvente: l’idruro di decile viene utilizzato come solvente nei processi industriali, come applicazioni di pulizia e sgrassaggio. La sua capacità di dissolvere varie sostanze non polari lo rende utile in questi processi.
- Carburante: il carburante diesel contiene idruro di decile come componente e lo utilizza come composto di riferimento per misurare l’indice di cetano, che valuta la qualità di accensione dei carburanti diesel. Contribuisce alle proprietà di combustione del gasolio.
- Intermedio chimico: l’idruro di decile funge da elemento costitutivo per la produzione di altri prodotti chimici. L’idruro di decile funge da materia prima per la sintesi di vari composti, inclusi tensioattivi, lubrificanti e polimeri.
- Estraente: le industrie farmaceutiche e alimentari utilizzano l’idruro di decile come estraente. Aiuta nella separazione e purificazione di alcuni composti e aromi dalle materie prime.
- Applicazioni di ricerca e laboratorio: la ricerca scientifica e i laboratori utilizzano l’idruro decilico. Serve come composto di riferimento nella gascromatografia e come standard per scopi di calibrazione.
- Formulazioni cosmetiche: i prodotti cosmetici e per la cura personale incorporano l’idruro di decile nelle loro formulazioni. Agisce come agente condizionante, emolliente e regolatore di viscosità in vari prodotti per la cura della pelle e dei capelli.
- Lubrificanti industriali: le applicazioni industriali beneficiano della bassa volatilità e del buon potere lubrificante dell’idruro decilico, utilizzandolo come lubrificante. Riduce l’attrito e l’usura tra le parti in movimento.
- Standard di calibrazione: la chimica analitica utilizza l’idruro decilico come standard di calibrazione. Assiste nella calibrazione e validazione di strumenti e tecniche analitiche.
Nel complesso, le proprietà versatili dell’idruro decilico lo rendono prezioso in vari settori, dalla produzione alla ricerca e sviluppo.
Domande:
D: Cos’è un decano?
R: L’idruro di decile è un idrocarburo con la formula molecolare C10H22, composto da dieci atomi di carbonio e ventidue atomi di idrogeno.
D: Quanti equivalenti di idrogeno gassoso sono necessari per ridurre 1-decino in decano?
R: La riduzione dell’1-decino a decil idruro richiede due equivalenti di idrogeno gassoso.
D: Il decano è polare?
R: No, l’idruro decilico è non polare perché è costituito da atomi di carbonio e idrogeno legati da legami covalenti non polari.
D: Lo iodio è solubile in C10H22?
R: Sì, lo iodio è solubile in C10H22 (decile idruro) perché le due sostanze non sono polari e possono mescolarsi.
D: Quale delle seguenti sostanze avrebbe la viscosità più elevata? (a) C4H10 (b) C8H18 (c) C10H22
R: C10H22 (idruro decilico) avrebbe la viscosità più alta tra le sostanze indicate a causa delle sue dimensioni molecolari maggiori e della catena di carbonio più lunga.
D: Calcolare il punto di congelamento di 23,0 g di decano (C10H22) in 53,0 g di CHCl3.
R: Il calcolo del punto di congelamento richiede informazioni aggiuntive come la costante di abbassamento del punto di congelamento per il solvente (CHCl3) e le frazioni molari dei componenti per determinare l’abbassamento del punto di congelamento.
