L’acido ascorbico (C6H8O6) è una vitamina presente in vari frutti e verdure. Aiuta il corpo ad assorbire il ferro, rafforza il sistema immunitario e favorisce la produzione di collagene per una pelle sana.
| Nome IUPAC | (5R)-[(1S)-1,2-diidrossietil]-3,4-diidrossifuran-2(5H)-one |
| Formula molecolare | C6H8O6 |
| numero CAS | 50-81-7 |
| Sinonimi | Vitamina C, acido L-ascorbico, 3-cheto-L-gulofuranolattone, vitamina antiscorbutica, L-ascorbato |
| InChI | InChI=1S/C6H8O6/c7-1-2(8)5-3(9)4(10)6(11)12-5/h2,5,7-10H,1H2 |
Proprietà dell’acido ascorbico
Formula dell’acido ascorbico
La formula dell’acido ascorbico è C6H8O6. È costituito da sei atomi di carbonio, otto atomi di idrogeno e sei atomi di ossigeno. Questa formula molecolare rappresenta la disposizione specifica e la quantità di atomi in una molecola di acido ascorbico.
Massa molare dell’acido ascorbico
La massa molare dell’L-ascorbato è di circa 176,12 grammi per mole. La massa molare si riferisce alla massa di una mole di una sostanza e si calcola sommando le masse atomiche di tutti gli atomi nella formula.
Punto di ebollizione dell’acido ascorbico
Il punto di ebollizione dell’L-ascorbato è di circa 553 gradi Celsius (1.027 gradi Fahrenheit). Questa è la temperatura alla quale la forma liquida dell’L-ascorbato si trasforma nella fase gassosa vincendo le forze intermolecolari che tengono insieme le molecole.
Punto di fusione dell’acido ascorbico
Il punto di fusione dell’L-ascorbato è di circa 190-192 gradi Celsius (da 374 a 378 gradi Fahrenheit). Questa è la temperatura alla quale la forma solida dell’L-ascorbato si trasforma in uno stato liquido a causa della rottura dei legami intermolecolari.
Densità dell’acido ascorbico g/mL
La densità dell’L-ascorbato è di circa 1,65 grammi per millilitro. La densità rappresenta la massa di una sostanza per unità di volume ed è una misura della densità delle molecole in un dato spazio.
Peso molecolare dell’acido ascorbico
Il peso molecolare dell’L-ascorbato è di circa 176,12 grammi per mole. Il peso molecolare, chiamato anche massa molecolare, si riferisce alla somma dei pesi atomici di tutti gli atomi di una molecola.
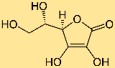
Struttura dell’acido ascorbico
L’L-ascorbato ha una struttura ad anello nota come lattone. È costituito da un anello a cinque membri con doppio legame e un anello a sei membri. La molecola contiene anche gruppi ossidrile (-OH) e un gruppo carbonile (C=O), che contribuiscono alle sue proprietà chimiche.
Solubilità dell’acido ascorbico
L-ascorbato è altamente solubile in acqua. Si dissolve facilmente in acqua grazie alla presenza di gruppi idrofili (-OH) nella sua struttura, permettendogli di formare legami idrogeno con le molecole d’acqua. Questa solubilità consente al corpo di assorbire e utilizzare facilmente l’L-ascorbato quando ingerito.
| Aspetto | Cristalli bianchi |
| Peso specifico | 1,65 g/ml |
| Colore | Bianco |
| Odore | Inodore o debole |
| Massa molare | 176,12 g/mole |
| Densità | 1,65 g/ml |
| Punto di fusione | 190-192°C (374-378°F) |
| Punto di ebollizione | 553°C (1027°F) |
| Punto flash | N / A |
| solubilità in acqua | Molto solubile |
| Solubilità | Solubile in acqua, etanolo |
| Pressione del vapore | 0,000087 mmHg |
| Densità del vapore | N / A |
| pKa | 4,17 (a 25°C) |
| pH | 2,2-2,8 (soluzione al 5%) |
Sicurezza e pericoli dell’acido ascorbico
L-ascorbato è generalmente considerato sicuro per il consumo e l’uso se usato come indicato. Tuttavia, un consumo eccessivo di L-ascorbato sotto forma di integratore può portare a problemi digestivi, come diarrea o crampi allo stomaco. È importante seguire le linee guida sul dosaggio raccomandato. In rari casi possono verificarsi reazioni allergiche che causano sintomi quali eruzione cutanea, prurito o difficoltà di respirazione. Quando si maneggia la polvere concentrata di L-ascorbato, è consigliabile indossare guanti protettivi ed evitare di inalare la polvere per evitare irritazioni. L-ascorbato deve essere conservato in un luogo fresco e asciutto, lontano dalla luce solare diretta e fuori dalla portata dei bambini.
| Simboli di pericolo | Nessuno |
| Descrizione della sicurezza | Nocivo se ingerito. Provoca leggera irritazione alla pelle e agli occhi. Evitare l’inalazione. |
| Numeri di identificazione delle Nazioni Unite | N / A |
| Codice SA | 29362700 |
| Classe di pericolo | Non classificato |
| Gruppo di imballaggio | Non classificato |
| Tossicità | Bassa tossicità. Tuttavia, un consumo eccessivo può portare a problemi digestivi. |
Si prega di notare che l’L-ascorbato è generalmente considerato sicuro per il consumo e non riporta simboli di pericolo specifici, identificatori ONU, classi di pericolo o classificazioni di gruppi di imballaggio.
Metodi per la sintesi dell’acido ascorbico
Innanzitutto, la conversione del sorbitolo sintetizza L-sorbosio.
Il processo Reichstein sintetizza L-ascorbato sottoponendo il D- glucosio a idrogenazione catalitica, con conseguente conversione del D- glucosio in D-sorbitolo. Un processo di fermentazione microbica ossida quindi il D-sorbitolo in L-sorbosio. Le successive reazioni chimiche trasformano l’L-sorbosio in acido 2-cheto-L-gulonico. Infine, un processo di riduzione converte l’acido 2-cheto-L-gulonico in L-ascorbato.
Il processo Reichstein-Grüssner fornisce un metodo più efficiente ed economico per sintetizzare L-ascorbato dal D- glucosio . Questo processo prevede una serie di reazioni di ossidazione, isomerizzazione e riduzione che alla fine producono L-ascorbato.
Un altro metodo in due fasi utilizza il sorbitolo come materia prima. In secondo luogo, una reazione di riduzione converte l’L-sorbosi in L-ascorbato per sintetizzarlo.
È importante notare che, sebbene l’L-ascorbato possa essere sintetizzato, si trova naturalmente anche in vari frutti e verdure, rendendolo facilmente disponibile attraverso fonti alimentari.
Usi dell’acido ascorbico
- L-ascorbato, noto anche come vitamina C, contribuisce in modo significativo al mantenimento della salute e del benessere generale.
- Le persone lo usano principalmente come integratore alimentare per prevenire o curare la carenza di vitamina C, che può causare malattie come lo scorbuto.
- Essendo un potente antiossidante, l’L-ascorbato protegge le cellule dai danni dei radicali liberi, supportando la salute del sistema immunitario.
- Svolge un ruolo cruciale nella sintesi del collagene, promuovendo la salute della pelle, la guarigione delle ferite e il mantenimento della salute del tessuto connettivo.
- L-ascorbato aiuta l’assorbimento del ferro dagli alimenti a base vegetale, migliorando così l’anemia da carenza di ferro.
- I produttori lo aggiungono comunemente agli alimenti come antiossidante per prevenire l’ossidazione e prolungare la durata di conservazione di vari prodotti.
- Cosmetici e prodotti per la cura della pelle contengono L-ascorbato per le sue proprietà schiarenti e antietà.
- Alcune bevande e alimenti contengono L-ascorbato aggiunto per migliorare il loro contenuto di vitamina C e fornire benefici nutrizionali.
- L’industria farmaceutica utilizza L-ascorbato come ingrediente nella formulazione di farmaci e integratori.
Nel complesso, l’L-ascorbato svolge un ruolo vitale in vari settori tra cui salute, nutrizione, cosmetici e industrie alimentari grazie alle sue numerose proprietà e applicazioni benefiche.
Domande:
D: L’acido citrico e l’acido ascorbico sono la stessa cosa?
R: No, l’acido citrico e l’L-ascorbato sono composti diversi con strutture e proprietà chimiche distinte.
D: Quale vitamina è conosciuta come acido ascorbico?
R: La vitamina C è conosciuta come L-ascorbato.
D: A cosa serve l’acido ascorbico?
R: L-ascorbato viene utilizzato per vari scopi, tra cui l’integrazione alimentare, la protezione antiossidante, la sintesi del collagene e il miglioramento dell’assorbimento del ferro.
D: L’acido citrico e l’acido ascorbico sono la stessa cosa?
R: No, l’acido citrico e l’L-ascorbato sono composti diversi con strutture e proprietà chimiche distinte.
D: Qual è la formula empirica dell’acido ascorbico, dato che la pseudoformula è c3.407h4.53o3.406?
R: La formula empirica per l’L-ascorbato è C6H8O6.
D: Quale atomo H della vitamina C (acido ascorbico) è il più acido? Seleziona la risposta migliore.
R: L’atomo di H sul gruppo carbossilico (–COOH) dell’L-ascorbato è il più acido.
D: L’acido ascorbico è dannoso per te?
R: L-ascorbato è generalmente sicuro da consumare nelle dosi consigliate, ma un consumo eccessivo può portare a problemi digestivi. Consultare un operatore sanitario per problemi specifici.
D: Qual è il pH dell’acido ascorbico?
R: L’L-ascorbato ha un intervallo di pH compreso tra circa 2,2 e 2,8 in una soluzione al 5%.
