Il ciclopentadiene (C5H6) è un composto ciclico con cinque atomi di carbonio e un doppio legame. È comunemente usato nella sintesi organica e come elemento costitutivo in varie reazioni chimiche.
| Nome IUPAC | Ciclopentadiene |
| Formula molecolare | C₅H₆ |
| numero CAS | 542-92-7 |
| Sinonimi | Ciclopenta-1,3-diene; 1,3-ciclopentadiene; dimero 1,3-ciclopentadiene; Diciclopentadiene; CPD |
| InChI | InChI=1S/C5H6/c1-2-4-5-3-1/h1-4H,5H2 |
Proprietà del ciclopentadiene
Formula del ciclopentadiene
La formula chimica del ciclopentadiene è C₅H₆. È composto da cinque atomi di carbonio e sei atomi di idrogeno. Questa formula rappresenta la composizione elementare del composto, fornendo informazioni sulla sua struttura molecolare e sulle sue proprietà.
Massa molare del ciclopentadiene
La massa molare del ciclopenta-1,3-diene è di circa 66,10 g/mol. La massa molare è la massa di una mole di una sostanza e si calcola sommando le masse atomiche di tutti gli atomi nella formula. Nel caso del ciclopenta-1,3-diene, la massa molare deriva dalle masse atomiche di carbonio e idrogeno.
Punto di ebollizione del ciclopentadiene
Il ciclopenta-1,3-diene ha un punto di ebollizione di circa 41,5°C. Il punto di ebollizione è la temperatura alla quale una sostanza passa dalla fase liquida alla fase gassosa sotto la pressione atmosferica standard. Il punto di ebollizione relativamente basso del ciclopenta-1,3-diene lo rende volatile e facilmente vaporizzabile.
Punto di fusione del ciclopentadiene
Il ciclopenta-1,3-diene non ha un punto di fusione ben definito a causa della sua tendenza a polimerizzare a temperature più basse. Tuttavia, può esistere allo stato congelato o solido a temperature molto basse. La presenza di impurità o dimerizzazione può influenzare il comportamento di fusione osservato.
Densità del ciclopentadiene g/mL
La densità del ciclopenta-1,3-diene è di circa 0,77 g/mL. La densità è una misura della massa per unità di volume e indica quanto strettamente le molecole sono imballate in una sostanza. La densità relativamente bassa del ciclopenta-1,3-diene suggerisce che sia meno denso dell’acqua e possa galleggiare sulla sua superficie.
Peso molecolare del ciclopentadiene
Il peso molecolare del ciclopenta-1,3-diene è di circa 66,10 g/mol. Si calcola sommando i pesi atomici di tutti gli atomi presenti nella molecola. Il peso molecolare fornisce informazioni importanti sulla massa del composto e viene utilizzato in vari calcoli e conversioni in chimica.
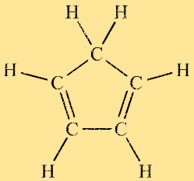
Struttura del ciclopentadiene
Il ciclopenta-1,3-diene ha una struttura ad anello costituita da un anello di carbonio a cinque membri con legami singoli e doppi alternati. La molecola adotta una conformazione planare a causa del suo carattere aromatico e presenta delocalizzazione elettronica nel sistema ad anello. Questa struttura unica contribuisce alla reattività e alle proprietà del ciclopenta-1,3-diene.
Solubilità del ciclopentadiene
Il ciclopenta-1,3-diene è scarsamente solubile in acqua, ma si dissolve facilmente in molti solventi organici, come benzene ed etere. Le sue caratteristiche di solubilità sono influenzate dalla polarità del solvente e dalla capacità delle molecole di soluto di interagire con le molecole di solvente. Il comportamento di solubilità del ciclopenta-1,3-diene è importante in varie applicazioni che coinvolgono la sintesi organica e le reazioni chimiche.
| Aspetto | Incolore |
| Peso specifico | 0,77 |
| Colore | N / A |
| Odore | Acri |
| Massa molare | 66,10 g/mole |
| Densità | 0,77 g/ml |
| Punto di fusione | N / A |
| Punto di ebollizione | 41,5°C |
| Punto flash | -12°C |
| solubilità in acqua | Insolubile |
| Solubilità | Solubile in solventi organici (benzene, etere) |
| Pressione del vapore | 110 mmHg a 25°C |
| Densità del vapore | 2.3 (aria = 1) |
| pKa | N / A |
| pH | Neutro |
Sicurezza e pericoli del ciclopentadiene
Il ciclopenta-1,3-diene presenta diversi rischi per la sicurezza che devono essere considerati. È altamente infiammabile e può formare miscele esplosive con l’aria. Il composto ha un basso punto di infiammabilità pari a -12°C, che aumenta il rischio di incendio. È nocivo anche se ingerito, inalato o assorbito attraverso la pelle e può causare irritazione agli occhi, alla pelle e al sistema respiratorio. Il ciclopentadiene può subire polimerizzazione, con conseguente rilascio di calore e pressione. È importante maneggiare questa sostanza chimica con cautela, utilizzando misure protettive adeguate, come indossare guanti, occhiali e protezione respiratoria. È necessario seguire procedure adeguate di stoccaggio, manipolazione e smaltimento per ridurre al minimo i rischi.
| Simboli di pericolo | Infiammabile |
| Descrizione della sicurezza | Tenere lontano da fonti di calore, scintille e fiamme libere. Utilizzare in un’area ben ventilata. Indossare guanti e occhiali protettivi. Evitare l’inalazione o il contatto con la pelle. |
| Numeri di identificazione delle Nazioni Unite | ONU 2044 |
| Codice SA | 29021900 |
| Classe di pericolo | 3 (Liquido infiammabile) |
| Gruppo di imballaggio | II |
| Tossicità | Nocivo se ingerito, inalato o assorbito attraverso la pelle. Può causare irritazione. È necessario adottare precauzioni adeguate durante la manipolazione. |
Metodi per la sintesi del ciclopentadiene
Vari metodi consentono la sintesi del ciclopenta-1,3-diene.
Un approccio comune per sintetizzare il ciclopenta-1,3-diene prevede la dimerizzazione del butadiene . In questo metodo, complessi di metalli di transizione come nichel o cobalto catalizzano una reazione di cicloaddizione [4+2] tra due molecole di butadiene , con conseguente formazione di ciclopenta-1,3-diene.
Sottoporre il ciclopentanone , un chetone ciclico, a temperature elevate in presenza di un catalizzatore acido consente la sua reazione di decomposizione termica, con conseguente formazione di ciclopenta-1,3-diene. Questa reazione dà il ciclopenta-1,3-diene come uno dei prodotti.
Un altro metodo per sintetizzare il ciclopenta-1,3-diene è la deidrogenazione del ciclopentene, un idrocarburo insaturo. Questo processo prevede l’uso di catalizzatori come platino o palladio per facilitare la rimozione di due atomi di idrogeno dal ciclopentene, con conseguente formazione di ciclopenta-1,3-diene.
Esponendo il diciclopentdiene, un composto dimerico, ad alte temperature, avviene la reazione retro-Diels-Alder, che porta alla sintesi del ciclopenta-1,3-diene. Questo processo termico induce una reazione di cicloaddizione inversa [4+2], che porta alla produzione di ciclopenta-1,3-diene.
Questi metodi di sintesi offrono diverse vie per ottenere il ciclopenta-1,3-diene, consentendo a ricercatori e chimici di scegliere l’approccio più adatto in base alle loro esigenze specifiche e alle risorse disponibili.
Usi del ciclopentadiene
Il ciclopenta-1,3-diene trova applicazione in vari campi grazie alle sue proprietà versatili. Ecco alcuni usi comuni del ciclopenta-1,3-diene:
- Il ciclopenta-1,3-diene svolge un ruolo cruciale in vari campi poiché ha proprietà versatili. È un prezioso elemento costitutivo della sintesi organica, consentendo la produzione di molti composti tra cui prodotti farmaceutici, polimeri e prodotti chimici speciali.
- La reazione Diels-Alder fa ampio uso del ciclopenta-1,3-diene perché agisce come un componente dienico e facilita la costruzione di strutture ad anello complesse in chimica organica. Questa reazione consente la formazione di sistemi ad anelli fusi.
- Nella produzione dei polimeri, il ciclopenta-1,3-diene agisce come monomero e contribuisce alla produzione di gomme sintetiche ed elastomeri. Svolge un ruolo essenziale nello sviluppo di materiali con proprietà meccaniche desiderabili.
- Il ciclopenta-1,3-diene trova applicazione nella formulazione di adesivi e rivestimenti grazie alla sua reattività e capacità di subire reazioni di reticolazione. Migliora l’adesione e la durabilità di questi prodotti, rendendoli adatti a varie applicazioni.
- Gli additivi per carburanti, come il metilciclopentadienil manganese tricarbonile (MMT), utilizzano derivati del ciclopenta-1,3-diene per migliorare l’efficienza della combustione e ridurre la detonazione del motore nella benzina.
- Il ciclopenta-1,3-diene svolge un ruolo importante negli studi sull’aromaticità perché presenta caratteristiche aromatiche grazie alla sua struttura ciclica. I ricercatori lo usano come composto modello per comprendere e studiare i sistemi aromatici.
Domande:
D: Cosa dimerizza il ciclopentadiene?
R: Il ciclopenta-1,3-diene può subire dimerizzazione, dove due molecole di ciclopentadiene si combinano per formare un dimero chiamato diciclopentadiene.
D: Il ciclopentadiene è aromatico?
R: Sì, il ciclopenta-1,3-diene è considerato aromatico a causa della sua struttura planare e della presenza di un sistema coniugato di legami singoli e doppi alternati.
D: Perché l’1,3-ciclopentadiene (pKa = 16) è un acido molto più forte del ciclopentano (pKa = 44)?
R: L’1,3-ciclopentadiene è più acido del ciclopentano perché ha un sistema coniugato di elettroni pi, che stabilizza la carica negativa risultante durante la deprotonazione, facilitando così la perdita di uno ione idrogeno.
D: Quale dei seguenti reagirebbe più rapidamente con l’1,3-ciclopentadiene?
R: I composti con doppi legami elettrofili, come l’anidride maleica o le aldeidi, reagirebbero più rapidamente con l’1,3-ciclopentadiene a causa della natura nucleofila del ciclopentadiene.
D: Perché il ciclopentadiene si rompe?
R: Il ciclopentadiene può subire cracking, un processo in cui subisce una decomposizione termica, che spesso porta alla formazione di frammenti più piccoli o alla polimerizzazione, a causa della sua intrinseca reattività e tendenza a subire riarrangiamenti.
D: pKa del ciclopentadiene?
R: Il pKa del ciclopenta-1,3-diene è circa 16.
D: Monomero di ciclopentadiene?
R: Il ciclopenta-1,3-diene esiste principalmente come monomero, ma può dimerizzare in determinate condizioni per formare diciclopentadiene.
D: Reazione del ciclopentadiene con l’anidride maleica?
R: Il ciclopenta-1,3-diene subisce una reazione Diels-Alder con l’anidride maleica per formare l’addotto ciclopentadiene-anidride maleica, una via sintetica comune per la produzione di vari composti.
