L’alcol allilico (C3H6O) è un liquido incolore con un odore pungente. Viene utilizzato nella produzione di resine, plastificanti e prodotti farmaceutici. Ciò potrebbe causare irritazione alla pelle e agli occhi.
| Nome IUPAC | Prop-2-in-1-olo |
| Formula molecolare | C3H6O |
| numero CAS | 107-18-6 |
| Sinonimi | 2-propen-1-olo; vinilcarbinolo; 2-propenolo; Propilenolo |
| InChI | InChI=1S/C3H6O/c1-2-3-4/h2.4H,1.3H2 |
Proprietà dell’alcool allilico
Formula di alcol allilico
La formula dell’alcol allilico è C3H6O. È costituito da tre atomi di carbonio (C3), sei atomi di idrogeno (H6) e un atomo di ossigeno (O). Questa formula chimica rappresenta la composizione e la disposizione degli atomi in una molecola di alcol allilico.
Massa molare dell’alcool allilico
La massa molare del vinilcarbinolo si calcola sommando le masse atomiche dei suoi elementi costitutivi. Il carbonio ha una massa atomica di circa 12,01 g/mol, l’idrogeno ha una massa atomica di circa 1,01 g/mol e l’ossigeno ha una massa atomica di circa 16,00 g/mol. Sommando questi valori si ottiene la massa molare del vinilcarbinolo pari a circa 58,08 g/mol.
Punto di ebollizione dell’alcol allilico
Il vinilcarbinolo ha un punto di ebollizione di circa 97,2 gradi Celsius (207 gradi Fahrenheit). Questa è la temperatura alla quale la forma liquida del vinilcarbinolo passa allo stato gassoso. Il punto di ebollizione è influenzato dalle forze intermolecolari e dalla struttura molecolare.
Punto di fusione dell’alcool allilico
Il punto di fusione del vinilcarbinolo è di circa -129 gradi Celsius (-200 gradi Fahrenheit). Questa è la temperatura alla quale la forma solida del vinilcarbinolo si trasforma in uno stato liquido. Il punto di fusione è determinato dalla forza delle forze intermolecolari e dalla disposizione delle molecole.
Densità dell’alcol allilico g/mL
La densità del vinilcarbinolo è tipicamente di circa 0,854 g/ml a 20 gradi Celsius (68 gradi Fahrenheit). La densità è la misura della massa per unità di volume, che indica quanto strettamente le molecole sono imballate in una sostanza.
Alcool allilico Peso molecolare
Il peso molecolare del vinilcarbinolo è di circa 58,08 grammi per mole (g/mol). Si calcola sommando i pesi atomici di tutti gli atomi della molecola in base alla sua formula chimica.
Struttura dell’alcool allilico
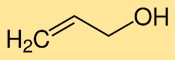
Il vinilcarbinolo ha una struttura molecolare costituita da una catena a tre atomi di carbonio (propene) con un gruppo ossidrile (-OH) attaccato a uno degli atomi di carbonio. Questa disposizione conferisce al vinilcarbinolo le sue proprietà chimiche e reattività uniche.
Solubilità dell’alcool allilico
Il vinilcarbinolo è in una certa misura solubile in acqua. Forma legami idrogeno con le molecole d’acqua a causa della presenza del gruppo ossidrile. Tuttavia, la sua solubilità diminuisce all’aumentare della temperatura. Il vinilcarbinolo è più solubile nei solventi polari e nei solventi organici come l’etanolo e l’acetone.
| Aspetto | Liquido incolore |
| Peso specifico | 0,854 g/ml |
| Colore | N / A |
| Odore | Acri |
| Massa molare | 58,08 g/mole |
| Densità | 0,854 g/ml |
| Punto di fusione | -129°C (-200°F) |
| Punto di ebollizione | 97,2°C (207°F) |
| Punto flash | 27,8°C (82°F) |
| solubilità in acqua | Miscibile |
| Solubilità | Solubile in solventi polari |
| Pressione del vapore | 22 mmHg a 20°C |
| Densità del vapore | 2.0 (aria = 1) |
| pKa | 15.4 |
| pH | 6.5-8.5 |
Sicurezza e pericoli dell’alcol allilico
Il vinilcarbinolo presenta alcuni rischi per la sicurezza e deve essere maneggiato con cautela. Può causare irritazione alla pelle, agli occhi e al sistema respiratorio per contatto diretto o inalazione. L’esposizione prolungata o ripetuta può causare dermatiti. L’ingestione di vinilcarbinolo può causare nausea, vomito e dolore addominale. È infiammabile e può formare miscele esplosive con l’aria. Pertanto, durante lo stoccaggio e la movimentazione sono essenziali un’adeguata ventilazione e misure di sicurezza antincendio. Quando si lavora con il vinilcarbinolo è necessario utilizzare dispositivi di protezione individuale, come guanti e occhiali protettivi, per ridurre al minimo il rischio di esposizione.
| Simboli di pericolo | Corrosivo, Infiammabile |
| Descrizione della sicurezza | – Provoca gravi ustioni cutanee e gravi lesioni oculari – Liquido e vapori facilmente infiammabili |
| Numeri di identificazione delle Nazioni Unite | ONU 1098 |
| Codice SA | 2905.13.00 |
| Classe di pericolo | Classe 6.1 (Materie tossiche) <br> Classe 3 (Liquidi infiammabili) |
| Gruppo di imballaggio | GE II |
| Tossicità | Tossico se ingerito, inalato o assorbito attraverso la pelle. Può causare gravi effetti sulla salute. |
Metodi per la sintesi dell’alcol allilico
La sintesi del vinilcarbinolo prevede diversi metodi. Un approccio comunemente utilizzato è l’idratazione catalitica del propilene , in cui il propilene reagisce con l’acqua in presenza di catalizzatori di acido solforico o acido fosforico. Condizioni di temperatura e pressione controllate facilitano la formazione di vinilcarbinolo.
Un altro metodo prevede l’idrolisi del cloruro di allile o dell’acetato di allile. Trattando il cloruro di allile con acqua e una base come idrossido di sodio o idrossido di potassio si ottengono vinilcarbinolo e il corrispondente sale cloruro. Allo stesso modo, l’idrolisi dell’acetato di allile con acqua e una base forte porta alla produzione di vinilcarbinolo e acido acetico.
La deidrogenazione del glicerolo, un sottoprodotto della produzione di biodiesel, è un’altra via per ottenere il vinilcarbinolo. Il glicerolo subisce la deidrogenazione catalitica a temperature elevate, producendo vinilcarbinolo.
Inoltre, la sintesi di Reppe prevede la reazione della formaldeide con l’acetilene. Per questa reazione sono necessari catalizzatori metallici come palladio o platino. Formaldeide e acetilene reagiscono per generare vinilcarbinolo.
Questi metodi di sintesi forniscono vari percorsi per la produzione di vinilcarbinolo su scala industriale per soddisfare vari requisiti applicativi.
Usi dell’alcol allilico
- I produttori utilizzano il vinilcarbinolo per produrre resine, che hanno molte applicazioni nella realizzazione di rivestimenti, adesivi e sigillanti.
- I composti farmaceutici, inclusi medicinali e farmaci, subiscono sintesi con il vinilcarbinolo che funge da precursore.
- Il vinilcarbinolo funge da componente chiave nella produzione di plastificanti, che migliorano la flessibilità e la durata della plastica.
- I produttori utilizzano il vinilcarbinolo come elemento costitutivo per produrre eteri allilici, che funzionano come solventi e intermedi nella sintesi organica.
- Il vinilcarbinolo aiuta a produrre aromi e fragranze sintetici, che aggiungono caratteristiche uniche ad alimenti, bevande e prodotti per la cura personale.
- Le formulazioni polimeriche beneficiano dell’incorporazione di vinilcarbinolo come agente reticolante, che migliora la resistenza meccanica e la resistenza al calore.
- I produttori producono resine alliliche, che hanno un’eccellente resistenza chimica, da utilizzare nella produzione di adesivi, rivestimenti e sigillanti.
- Il vinilcarbinolo serve come materia prima per la sintesi degli esteri allilici, che trovano applicazione nella preparazione di vari prodotti cosmetici e per la cura personale.
- Le reazioni di chimica organica utilizzano il vinilcarbinolo come reagente per facilitare la sintesi di vari composti.
- Il vinilcarbinolo svolge un ruolo cruciale nella produzione di prodotti chimici speciali e intermedi per varie industrie, compresi i settori farmaceutico, agricolo e chimico.
Domande:
D: Che tipo di reazione può essere utilizzata per preparare l’alcol allilico dal bromuro di allile?
R: Il vinilcarbinolo può essere preparato dal bromuro di allile mediante una reazione di sostituzione nucleofila utilizzando una base forte, come l’idrossido di sodio o l’idrossido di potassio.
D: Cosa c’è di insolito negli atomi di carbonio allilici?
R: Gli atomi di carbonio allilico sono adiacenti a un doppio legame carbonio-carbonio, conferendo loro reattività e stabilità uniche rispetto agli altri atomi di carbonio nella molecola.
D: Cos’è l’alcol allilico?
R: L’alcol allilico è un composto alcolico in cui il gruppo ossidrile (-OH) è attaccato a un atomo di carbonio allilico, che è adiacente a un doppio legame carbonio-carbonio.
D: Quale dei seguenti è un alcol allilico?
R: Il 2-buten-1-olo è un esempio di alcol allilico.
D: Come si forma l’alcol allilico?
R: Gli alcoli allilici possono essere formati attaccando un gruppo ossidrile a un atomo di carbonio allilico attraverso appropriate reazioni chimiche, come reazioni di sostituzione nucleofila o di addizione.
D: Cosa sono gli alcoli allilici secondari?
R: Gli alcoli allilici secondari sono alcoli allilici in cui l’atomo di carbonio allilico è attaccato ad altri due atomi di carbonio e il gruppo ossidrile è attaccato a uno di questi atomi di carbonio.
D: Come produrre l’alcol allilico?
R: Gli alcoli allilici possono essere sintetizzati introducendo un gruppo ossidrile in un atomo di carbonio allilico tramite reazioni chimiche appropriate, come l’utilizzo di nucleofili o l’aggiunta di acqua agli alogenuri allilici o alle olefine.
D: Gli alcoli possono essere allilici?
R: Sì, gli alcoli possono essere allilici se il gruppo ossidrile è attaccato a un atomo di carbonio allilico adiacente a un doppio legame carbonio-carbonio.
D: L’alcol allilico è un alcol primario?
R: No, l’alcol allilico non è un alcol primario. È classificato come alcol secondario poiché il gruppo ossidrile è attaccato ad un atomo di carbonio legato ad altri due atomi di carbonio.
