L’etere vinilico (C4H6O) è un composto chimico utilizzato in varie applicazioni. Ha proprietà uniche, come reattività e bassa tossicità, che lo rendono prezioso in settori come quello farmaceutico e di sintesi organica.
| Nome IUPAC | Etossietilene |
| Formula molecolare | C4H6O |
| numero CAS | 109-93-3 |
| Sinonimi | Etere divinilico; 1,1′-ossibisetene; Ossirano, ossido divinilico, vinether |
| InChI | InChI=1S/C4H6O/c1-2-5-4-3-1/h1-4H2 |
Proprietà dell’etere vinilico
Formula di etere vinilico
La formula dell’etere vinilico è C4H6O. È costituito da quattro atomi di carbonio, sei atomi di idrogeno e un atomo di ossigeno. Questa formula molecolare rappresenta la composizione dell’etere vinilico, fornendo informazioni sui tipi e sul numero di atomi presenti in una singola molecola.
Massa molare dell’etere vinilico
La massa molare dell’etere divinilico viene calcolata sommando le masse atomiche di tutti gli atomi nella sua formula. La massa molare di C4H6O (etere divinilico) è di circa 70,09 grammi per mole. Questo valore è cruciale per vari calcoli, come determinare la quantità di etere divinilico necessaria per le reazioni.
Punto di ebollizione dell’etere vinilico
L’etere divinilico ha un punto di ebollizione di circa 34,6 gradi Celsius (94,3 gradi Fahrenheit). Questa temperatura indica il punto in cui l’etere divinilico subisce un cambiamento di fase da liquido a gas sotto pressione atmosferica standard. Il punto di ebollizione relativamente basso rende l’etere divinilico utile in determinate applicazioni e processi.
Etere vinilico Punto di fusione
Il punto di fusione dell’etere divinilico è di circa -116 gradi Celsius (-177 gradi Fahrenheit). Questa temperatura indica il punto in cui l’etere divinilico passa dallo stato solido a quello liquido. Il basso punto di fusione è importante perché influenza la manipolazione e lo stoccaggio dell’etere divinilico.
Densità del vinil etere g/mL
La densità dell’etere divinilico è di circa 0,734 grammi per millilitro (g/mL). La densità si riferisce alla massa di una sostanza per unità di volume. La densità dell’etere divinilico fornisce informazioni sulla sua compattezza o concentrazione, che possono essere utili per una varietà di applicazioni, inclusi calcoli di formulazione e dosaggio.
Peso molecolare dell’etere vinilico
Il peso molecolare dell’etere divinilico è di circa 70,09 grammi per mole. Rappresenta la massa di una mole di molecole di etere divinilico. Il peso molecolare è fondamentale per vari calcoli, inclusa la determinazione del numero di molecole o moli presenti in una data quantità di etere divinilico.
Struttura dell’etere vinilico
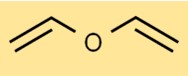
La struttura dell’etere divinilico è costituita da due doppi legami carbonio-carbonio (C=C) e un atomo di ossigeno legato a due carboni (CO). Questa disposizione conferisce all’etere vinilico le sue proprietà e reattività uniche. Comprendere la struttura è importante per studiarne il comportamento nelle reazioni chimiche e nelle interazioni con altre sostanze.
Solubilità dell’etere vinilico
L’etere divinilico è scarsamente solubile in acqua ma può dissolversi in solventi organici come etanolo, acetone e cloroformio. La sua solubilità dipende da fattori quali la temperatura e la natura del solvente. La conoscenza della solubilità dell’etere divinilico è fondamentale quando si considerano le sue applicazioni, formulazioni e compatibilità con altre sostanze.
| Aspetto | Liquido incolore |
| Peso specifico | 0,734 g/ml |
| Colore | N / A |
| Odore | Odore dolce ed etereo |
| Massa molare | 70,09 g/mole |
| Densità | 0,734 g/ml |
| Punto di fusione | -116°C (-177°F) |
| Punto di ebollizione | 34,6°C (94,3°F) |
| Punto flash | -40°C (-40°F) |
| solubilità in acqua | Scarsamente solubile |
| Solubilità | Solubile in solventi organici |
| Pressione del vapore | 155 mmHg a 20°C |
| Densità del vapore | 2,50 (aria = 1) |
| pKa | N / A |
| pH | N / A |
Sicurezza e pericoli dell’etere vinilico
L’etere divinilico presenta alcuni rischi per la sicurezza che devono essere considerati. È infiammabile e può formare miscele esplosive con l’aria. Pertanto, deve essere conservato e maneggiato lontano da fiamme libere o fonti di ignizione. I vapori dell’etere divinilico possono causare irritazione al sistema respiratorio e agli occhi. Il contatto diretto con la pelle può causare dermatiti o ustioni chimiche. Quando si lavora con l’etere divinilico è necessario utilizzare una ventilazione adeguata e dispositivi di protezione individuale. Inoltre, è essenziale seguire procedure di smaltimento adeguate per evitare la contaminazione ambientale. Nel complesso, seguire i protocolli di sicurezza è fondamentale per ridurre al minimo i rischi associati all’etere divinilico.
| Simboli di pericolo | Infiammabile, nocivo |
| Descrizione della sicurezza | Tenere lontano dalle fiamme libere. Utilizzare in un’area ben ventilata. Evitare il contatto diretto con la pelle e gli occhi. Smaltire i rifiuti correttamente. |
| Numeri di identificazione delle Nazioni Unite | ONU 1159 |
| Codice SA | 2909.19.00 |
| Classe di pericolo | Classe 3 (Liquidi infiammabili) |
| Gruppo di imballaggio | GE II |
| Tossicità | Nocivo se ingerito o inalato. Può causare irritazioni o ustioni alla pelle e agli occhi. |
Metodi per sintetizzare l’etere vinilico
Esistono diversi metodi per sintetizzare l’etere divinilico.
Un approccio comune è la reazione tra etanolo e acetilene in presenza di un catalizzatore acido, come acido solforico o acido p-toluensolfonico. Ciò si traduce nella formazione di etere divinilico come prodotto. Un altro metodo prevede l’aggiunta di uno ione alcossido all’acetilene , che genera un intermedio etere divinilico che può quindi essere convertito in etere divinilico mediante protonazione.
L’etere divinilico può essere preparato facendo reagire un alcol con alogenuri vinilici, come cloruro di vinile o bromuro di vinile, attraverso una reazione di eterificazione. Questa reazione richiede la presenza di una base, come carbonato di sodio o di potassio, per facilitare la formazione dell’etere divinilico desiderato.
Per sintetizzare l’etere divinilico, gli alchini possono essere fatti reagire con alogenuri alchilici in presenza di una base forte, come l’ammide di sodio. Questo processo, noto come riarrangiamento di Favorskii, comporta la conversione dell’alogenuro alchilico in un etere divinilico.
La reazione di aldeidi o chetoni con l’etere etildivinilico, utilizzando catalizzatori acidi di Lewis come il cloruro di zinco o il cloruro di alluminio, consente la preparazione di derivati dell’etere divinilico. Questo processo, noto come reazione Prins, consente la formazione di vari derivati dell’etere divinilico.
Usi dell’etere vinilico
L’etere divinilico trova impiego in varie applicazioni grazie alle sue proprietà uniche. Ecco alcuni usi comuni:
- L’etere divinilico svolge un ruolo cruciale come precursore nella sintesi di composti farmaceutici e aiuta nella produzione di agenti anestetici, rilassanti muscolari e altre sostanze medicinali.
- La sintesi organica trae grandi benefici dalla versatilità dell’etere divinilico, poiché funge da elemento costitutivo versatile in varie reazioni, comprese reazioni di accoppiamento incrociato, polimerizzazioni e cicloaddizioni, dando origine a preziosi composti organici.
- L’etere divinilico funge da intermedio nella produzione di un’ampia gamma di prodotti chimici, come solventi, adesivi, rivestimenti e plastificanti, consentendo la creazione di composti su misura per applicazioni specifiche.
- La rapida polimerizzazione dell’etere divinilico sotto la luce ultravioletta lo rende un componente prezioso nei rivestimenti e negli adesivi polimerizzabili con raggi UV, fornendo rivestimenti durevoli e a polimerizzazione rapida per applicazioni nel settore automobilistico, elettronico e della macchina da stampa.
- La copolimerizzazione dell’etere divinilico con altri monomeri genera copolimeri con proprietà uniche per varie applicazioni, come sistemi di somministrazione di farmaci, biomateriali e rivestimenti.
- Funzionando come agente reticolante, l’etere divinilico migliora la produzione di polimeri reticolati, che presentano una migliore resistenza meccanica, resistenza chimica e stabilità termica, rivelandosi quindi utili in vari settori.
- L’etere divinilico fornisce uno strumento essenziale nella ricerca e nello sviluppo di laboratorio, consentendo agli scienziati di esplorare nuove reazioni, sviluppare nuovi materiali e far avanzare la comprensione scientifica, grazie alla sua reattività e versatilità.
Domande:
D: Gli eteri vinilici sono stabili?
R: Gli eteri divinilici sono generalmente composti stabili, ma la loro stabilità può variare a seconda delle caratteristiche strutturali specifiche e delle condizioni di reazione.
D: Come disegnare la struttura dell’etere vinilico?
R: Per disegnare la struttura dell’etere divinilico, raffigura un doppio legame carbonio-carbonio (C=C) con un carbonio legato a un atomo di ossigeno (CO).
D: Cos’è l’etere vinilico/acido maleico contenuto in Polygrip?
R: Il copolimero etere divinilico/acido maleico viene utilizzato in Polygrip come dente adesivo. Aiuta a garantire l’adesione tra la protesi e le gengive.
D: Come produrre l’etere vinilico?
R: L’etere divinilico può essere prodotto con vari metodi, come la reazione tra etanolo e acetilene o l’eterificazione di alcoli con alogenuri vinilici.
D: Come sintetizzare gli eteri vinilici?
R: Gli eteri divinilici possono essere sintetizzati attraverso varie vie, comprese le reazioni che coinvolgono alcoli, alchini e alogenuri alchilici, nonché le reazioni di Prins e i riarrangiamenti di Favorskii.
D: L’etere vinilico è un accettore di Michael?
R: Gli eteri divinilici generalmente non sono considerati accettori di Michael perché non hanno il gruppo carbonilico α,β-insaturo caratteristico degli accettori di Michael.
D: Qual è il ruolo dell’etere etilvinilico nelle reazioni ROMP?
R: L’etere etilvinilico può fungere da comonomero nelle reazioni di polimerizzazione metatesi ad apertura di anello (ROMP), contribuendo alla formazione di catene polimeriche con proprietà specifiche.
D: Alcol etilviniletere?
R: L’alcol etilviniletere non esiste come composto separato. L’etere etildivinilico è un composto distinto e non un alcol.
