L’etere etilvinilico (C4H8O) è un composto organico volatile utilizzato come solvente e nella produzione di polimeri. Ha un odore gradevole ed è infiammabile.
| Nome IUPAC | Etossietilene |
| Formula molecolare | C4H8O |
| numero CAS | 109-92-2 |
| Sinonimi | Etere vinilico etilico, etossietilene, EVE, EEE, VEVE |
| InChI | InChI=1S/C4H8O/c1-2-5-4-3-6-1/h1-4H2 |
Proprietà dell’etere etilvinilico
Formula etil vinil etere
La formula chimica dell’etossietilene è C4H8O. Descrive la composizione di questo composto, indicando che contiene quattro atomi di carbonio, otto atomi di idrogeno e un atomo di ossigeno.
Massa molare dell’etere vinilico etilico
La massa molare dell’etossietilene si calcola sommando le masse atomiche dei suoi elementi costitutivi. In questo caso si tratta di circa 72,11 grammi per mole. La massa molare viene utilizzata per determinare la quantità di sostanza presente in un dato campione.
Punto di ebollizione dell’etere etilvinilico
L’etossietilene ha un punto di ebollizione compreso tra 35 e 36 gradi Celsius (da 95 a 97 gradi Fahrenheit). Questo punto di ebollizione relativamente basso suggerisce che può facilmente vaporizzare e passare allo stato gassoso quando riscaldato.
Etil vinil etere Punto di fusione
Il punto di fusione dell’etossietilene è di circa -102 gradi Celsius (-152 gradi Fahrenheit). Ciò indica che si tratta di un composto volatile che esiste in forma liquida a temperatura ambiente e si trasforma in solido a temperature molto basse.
Densità dell’etere etilvinilico g/mL
La densità dell’etossietilene è di circa 0,73 grammi per millilitro. Questo valore indica la massa del composto per unità di volume. La densità di una sostanza è importante per varie applicazioni, inclusa la determinazione della sua galleggiabilità e solubilità.
Peso Molecolare dell’etere vinilico etilico
Il peso molecolare dell’etossietilene è di circa 72,11 grammi per mole. Rappresenta la somma dei pesi atomici di tutti gli atomi presenti in una molecola. Il peso molecolare è fondamentale in vari calcoli chimici, come la stechiometria e la determinazione delle concentrazioni.
Struttura dell’etere etilvinilico
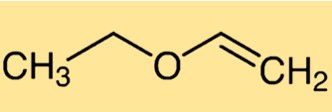
L’etossietilene è costituito da una catena di carbonio con quattro atomi di carbonio (C4), un atomo di ossigeno (O) e un gruppo etilico (-C2H5) attaccato a un gruppo vinilico (-CH=CH2). La struttura ricorda una catena lineare di carbonio con un atomo di ossigeno al centro, collegato a due gruppi di carbonio.
Solubilità dell’etere etilvinilico
L’etossietilene è moderatamente solubile in acqua, con una solubilità di circa 6,2 grammi per 100 millilitri a 25 gradi Celsius (77 gradi Fahrenheit). Tuttavia, mostra una migliore solubilità in solventi organici come etanolo e acetone. La solubilità dell’etossietilene è influenzata dalla sua polarità e dalle sue interazioni molecolari con le molecole del solvente.
| Aspetto | Liquido incolore |
| Peso specifico | 0,73 g/ml |
| Colore | Incolore |
| Odore | Piacevole |
| Massa molare | 72,11 g/mole |
| Densità | 0,73 g/ml |
| Punto di fusione | -102°C |
| Punto di ebollizione | 35-36°C |
| Punto flash | -20°C |
| solubilità in acqua | Moderare |
| Solubilità | Solubile in solventi organici come etanolo, acetone |
| Pressione del vapore | 159 mmHg a 25°C |
| Densità del vapore | 2,5 (aria = 1) |
| pKa | 12.7 |
| pH | Neutro |
Sicurezza e pericoli dell’etere etilvinilico
L’etossietilene presenta alcuni rischi per la sicurezza e deve essere maneggiato con cautela. È altamente infiammabile, con un punto di infiammabilità di -20 gradi Celsius (-4 gradi Fahrenheit), il che significa che può accendersi facilmente. Dovrebbe essere tenuto lontano da fiamme libere, scintille e fonti di calore. Il composto può anche causare irritazione alla pelle, agli occhi e al sistema respiratorio attraverso il contatto o l’inalazione. È necessaria una ventilazione adeguata per ridurre al minimo l’esposizione. L’etossietilene deve essere conservato in contenitori ermeticamente chiusi, lontano da sostanze incompatibili. È importante seguire le corrette procedure di manipolazione, indossare dispositivi di protezione adeguati e consultare le schede tecniche di sicurezza per informazioni complete sulla sicurezza.
| Simboli di pericolo | Infiammabile (F) |
| Descrizione della sicurezza | Tenere lontano da fonti di calore/scintille/fiamme libere. Utilizzare in aree ben ventilate. Evitare il contatto con gli occhi, la pelle e gli indumenti. |
| Numeri di identificazione delle Nazioni Unite | ONU 1151 |
| Codice SA | 29091900 |
| Classe di pericolo | Classe 3 – Liquidi infiammabili |
| Gruppo di imballaggio | GE II |
| Tossicità | Può causare irritazione alla pelle, agli occhi e al sistema respiratorio. Evitare l’esposizione prolungata o ripetuta. |
Metodi per la sintesi dell’etere etilvinilico
Vari metodi possono sintetizzare l’etossietilene. Un approccio comune prevede la reazione tra etanolo e acetilene in presenza di un catalizzatore basico forte, come l’idrossido di potassio (KOH). La reazione procede attraverso un processo di eliminazione, in cui il gruppo ossidrile (-OH) dell’etanolo si combina con un atomo di idrogeno della molecola di acetilene , formando acqua. Segue questa fase la formazione del legame vinil etere tra la molecola di acetilene e il rimanente gruppo -C2H5 dell’etanolo.
Un altro metodo prevede la reazione tra alcol etilico e acetato di vinile in presenza di un catalizzatore acido, come l’acido solforico (H2SO4). Il catalizzatore acido contribuisce al processo di esterificazione, in cui alcol e acido si combinano per formare un composto estere. In questo caso l’estere risultante subisce una successiva decomposizione termica, che porta alla formazione di etossietilene.
La reazione tra alcol etilico e acetilene in presenza di un catalizzatore di palladio può preparare l’etossietilene. Questo metodo, noto come reazione di accoppiamento catalizzata da Pd, consente la conversione diretta di alcol e acetilene nell’etere vinilico desiderato.
Questi metodi di sintesi aprono la strada alla produzione di etossietilene, che trova applicazioni in vari settori come la produzione di polimeri, solventi e intermedi chimici. La corretta manipolazione e il rispetto dei protocolli di sicurezza sono essenziali durante il processo di sintesi a causa dell’infiammabilità e dei potenziali pericoli associati all’etossietilene.
Usi dell’etere etilvinilico
Ecco alcuni degli usi comuni dell’etossietilene grazie alle sue proprietà uniche:
- Solvente: l’etossietilene viene utilizzato come solvente per vari composti organici, in particolare nella produzione di resine, vernici e lacche.
- Polimerizzazione: agisce come monomero nella sintesi di diversi polimeri, come poli(etere vinilico) e poli(etossietilene), che trovano applicazioni in adesivi, rivestimenti e modificatori di superficie.
- Intermedi chimici: Agisce come precursore per la sintesi di altri composti. Subisce varie reazioni chimiche per produrre preziosi intermedi utilizzati nell’industria farmaceutica, agrochimica e dei profumi.
- Additivo per carburante: le industrie lo utilizzano come additivo nella benzina per migliorare l’efficienza della combustione e ridurre le emissioni.
- Reagente di laboratorio: serve come reagente nella sintesi organica, in particolare nella preparazione di composti vinilici, eteri e altre molecole organiche funzionalizzate.
- Sapore e profumo: svolge un ruolo nella produzione di aromi e fragranze artificiali, conferendo odori piacevoli e desiderabili a vari prodotti di consumo.
- Ricerca chimica: trova applicazione come composto di riferimento nelle tecniche di analisi chimica come la gascromatografia e la spettroscopia.
- Solvente di estrazione: serve come solvente per l’estrazione di prodotti naturali, come oli essenziali e aromi.
La natura versatile dell’etossietilene gli consente di contribuire a vari settori, ricoprendo ruoli che vanno dai solventi e monomeri ai reagenti e agli additivi.
Domande:
D: È possibile coniugare l’etere vinil etilico?
R: No, l’etossietilene non presenta coniugazione a causa dell’assenza di legami pi coniugati nella sua struttura.
D: Qual è il ruolo dell’etere etilvinilico nelle reazioni ROMP?
R: L’etossietilene funge da comonomero nelle reazioni di polimerizzazione metatesi ad apertura di anello (ROMP), partecipando alla formazione di polimeri con proprietà e strutture uniche.
D: Alcol etilviniletere?
R: L’etossietilene non ha un gruppo funzionale alcolico; è un composto etereo.
D: Spettro IR dell’etere etilvinilico?
R: Lo spettro infrarosso (IR) dell’etossietilene mostra generalmente picchi caratteristici intorno a 3000-3100 cm^-1 (allungamento CH) e tra 1600 e 1650 cm^-1 (allungamento C=C).
D: Densità dell’etere etilvinilico?
R: La densità dell’etossietilene è di circa 0,73 grammi per millilitro (g/mL).
D: È possibile coniugare l’etere vinil etilico?
R: No, l’etossietilene non presenta coniugazione a causa della sua struttura molecolare priva di legami pi coniugati.
D: Stabilità dell’etere etilvinilico?
R: L’etossietilene è relativamente stabile ma deve essere maneggiato e conservato con cura a causa della sua infiammabilità e dei potenziali pericoli.
D: Produttori di etilviniletere?
R: L’etossietilene è prodotto da vari produttori e fornitori di prodotti chimici in tutto il mondo, comprese aziende di prodotti chimici fini e reagenti.
