Il cloruro di allile è un liquido trasparente e infiammabile con un odore pungente. Viene utilizzato nella produzione di vari composti organici e come solvente. Può essere dannoso per l’uomo se inalato o ingerito.
| Nome dell’IUPAC | 3-cloroprop-1-ene |
| Formula molecolare | C3H5Cl |
| numero CAS | 107-05-1 |
| Sinonimi | Cloruro di 2-propenile, 3-cloropropene, cloropropene, cloruro di allile, 3-cloro-1-propene, 1-cloro-2-propene |
| InChI | InChI=1S/C3H5Cl/c1-2-3-4/h2H,1.3H2 |
Proprietà del cloruro di allile
Formula del cloruro di allile
La formula chimica del cloruro di allile è C3H5Cl. È un liquido limpido, incolore con un odore pungente. La struttura del cloruro di allile è costituita da una molecola di propene con un atomo di cloro attaccato al secondo atomo di carbonio. È un importante intermedio nella produzione di vari composti organici, come epossidi, allilamine e alcoli allilici.
Massa molare del cloruro di allile
La massa molare del 3-cloropropene è 76,53 g/mol. Questo viene calcolato aggiungendo i pesi atomici di carbonio, idrogeno e cloro, che sono rispettivamente 12,01 g/mol, 1,01 g/mol e 35,45 g/mol. La massa molare è una proprietà importante di un composto chimico perché viene utilizzata per calcolare la quantità di sostanza contenuta in una determinata massa.
Punto di ebollizione del cloruro di allile
Il punto di ebollizione del 3-cloropropene è 46,05°C (114,9°F). Questo è relativamente basso rispetto ad altri composti organici, rendendo il 3-cloropropene una sostanza volatile. Il basso punto di ebollizione rende il 3-cloropropene utile anche nei processi industriali perché può essere facilmente evaporato e condensato per purificarlo.
Punto di fusione del cloruro di allile
Il punto di fusione del 3-cloropropene è -136°C (-213°F). Questa è una temperatura molto bassa e significa che il 3-cloropropene esiste in forma liquida a temperatura ambiente. Tuttavia, quando il 3-cloropropene viene raffreddato a temperature molto basse, può solidificarsi in una forma cristallina bianca.
Densità del cloruro di allile g/mL
La densità del 3-cloropropene è 0,950 g/mL. Ciò significa che il 3-cloropropene è più denso dell’acqua, che ha una densità di 1 g/mL. L’elevata densità del 3-cloropropene lo rende utile per separarlo da altre sostanze a densità inferiore, come l’acqua.
Peso molecolare del cloruro di allile
Il peso molecolare del 3-cloropropene è 76,53 g/mol. Questo valore viene calcolato sommando i pesi atomici di tutti gli atomi nella molecola. Il peso molecolare è importante per determinare le proprietà fisiche e chimiche di un composto.
Struttura del cloruro di allile
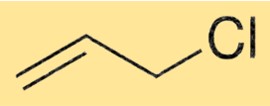
La struttura del 3-cloropropene è costituita da una molecola di propene con un atomo di cloro attaccato al secondo atomo di carbonio. Questo forma un gruppo vinilico, che è un gruppo funzionale nella chimica organica. Il gruppo vinilico è responsabile della reattività del 3-cloropropene in varie reazioni chimiche.
Solubilità del cloruro di allile
Il 3-cloropropene è solubile in molti solventi organici, come etere e benzene, ma è insolubile in acqua. La solubilità del 3-cloropropene in diversi solventi è dovuta alla sua natura polare. La polarità del 3-cloropropene è determinata dalla differenza di elettronegatività tra il legame carbonio-idrogeno e il legame carbonio-cloro.
| Aspetto | Liquido limpido e incolore |
| Densità specifica | 0,950 g/ml |
| Colore | Incolore |
| Odore | Acri |
| Massa molare | 76,53 g/mole |
| Densità | 0,950 g/ml |
| Punto di fusione | -136°C (-213°F) |
| Punto di ebollizione | 46,05°C (114,9°F) |
| Punto flash | -13°C (9°F) |
| solubilità in acqua | < 1g/l |
| Solubilità | Solubile in solventi organici |
| Pressione del vapore | 21,5 kPa a 20°C |
| Densità del vapore | 2,64 (aria = 1) |
| pKa | 9.18 |
| pH | Non applicabile (il pH è definito solo per le soluzioni acquose) |
Sicurezza e pericoli del cloruro di allile
Il 3-cloropropene è una sostanza altamente tossica e corrosiva. Può provocare gravi ustioni cutanee e gravi lesioni oculari in caso di contatto e può essere nocivo se inalato o ingerito. È anche altamente infiammabile e può reagire violentemente con alcuni composti. È necessario adottare adeguate precauzioni di sicurezza quando si lavora con 3-cloropropene, compreso indossare indumenti protettivi, guanti e protezione per gli occhi. Dovrebbe essere conservato in un luogo fresco, asciutto e ben ventilato, lontano da fonti di calore e ignizione. Se esposto o ingerito, consultare immediatamente un medico. È importante seguire protocolli di sicurezza adeguati per evitare incidenti e lesioni durante la manipolazione del 3-cloropropene.
| Simboli di pericolo | T,C |
| Descrizione della sicurezza | Facilmente infiammabile, tossico e corrosivo. Provoca gravi ustioni cutanee e lesioni oculari. Nocivo se inalato o ingerito. |
| Numeri di identificazione delle Nazioni Unite | ONU 1100 |
| Codice SA | 2903.39.90 |
| Classe di pericolo | Classe 3 (Liquidi infiammabili), Classe 6.1 (Materie tossiche), Classe 8 (Materie corrosive) |
| Gruppo di imballaggio | II |
| Tossicità | LD50 = 250 mg/kg (orale, ratto); LC50 = 1220 ppm (inalazione, ratto, 4 ore) |
Metodi per la sintesi del cloruro di allile
Esistono diversi metodi per sintetizzare il 3-cloropropene.
Uno dei metodi più comuni consiste nell’aggiungere gas di acido cloridrico all’alcol allilico in presenza di un catalizzatore. Un altro metodo prevede la reazione del propilene con cloro gassoso in presenza di un catalizzatore per formare 3-cloropropene.
Per preparare il 3-cloropropene, l’alcol allilico può essere fatto reagire con cloruro di tionile o tricloruro di fosforo. Questa reazione comporta la conversione dell’alcol nel corrispondente cloruro attraverso una reazione di sostituzione nucleofila.
Un terzo metodo per preparare il 3-cloropropene prevede la reazione del bromuro di allile con cloruro di sodio in presenza di polvere di rame. I chimici usano spesso questo metodo quando hanno accesso immediato al bromuro di allile ma non dispongono di 3-cloropropene.
Un altro metodo per sintetizzare il 3-cloropropene prevede la reazione dell’alcol allilico con acido cloridrico gassoso in presenza di un agente disidratante come il cloruro di zinco. I chimici usano spesso questo metodo per preparare il 3-cloropropene con resa e purezza elevate.
Usi del cloruro di allile
Il 3-cloropropene ha diversi usi importanti in vari settori grazie alle sue proprietà uniche:
- Produzione di composti allilici: il 3-cloropropene funge da precursore di vari composti allilici come alcol allilico, allilammina ed esteri allilici. La produzione di prodotti farmaceutici, profumi e aromi comporta generalmente l’uso di composti allilici.
- Produzione di polimeri: i produttori utilizzano il 3-cloropropene come monomero per produrre vari polimeri, come il poli3-cloropropene e l’allil diglicole carbonato.
- Solvente: utilizzato come solvente per vari composti organici grazie al suo basso punto di ebollizione e all’elevata polarità.
- Pesticida: utilizzato come fumigante e sterilizzante del terreno in agricoltura per controllare parassiti ed erbe infestanti.
- Produzione di coloranti e pigmenti: utilizzato nella produzione di coloranti e pigmenti per l’industria tessile e delle vernici.
- Industria petrolifera e del gas: utilizzato anche nell’industria petrolifera e del gas come inibitore della corrosione, lubrificante e additivo per fluidi di perforazione.
Domande:
D: Perché il cloruro di allile subisce reazioni SN1 anche se è un alogenuro di 1°?
R: Il 3-cloropropene subisce reazioni SN1 a causa della stabilità del carbocatione intermedio, che è stabilizzato per risonanza dal gruppo allile.
D: Cosa succede al cloruro di allile in una reazione SN2?
R: In una reazione SN2, il nucleofilo attacca il carbonio allilico dalla parte posteriore, portando all’inversione della stereochimica e alla formazione del corrispondente alcol allilico o ammina.
D: Il cloruro di allile è primario, secondario o terziario?
R: Il 3-cloropropene è un alogenuro primario.
D: Quale delle seguenti reazioni avviene più velocemente: AcO- + 3-cloropropene o MeO- + 3-cloropropene? R: MeO- + 3-cloropropene si forma più rapidamente di AcO- + 3-cloropropene a causa dell’ingombro sterico causato dal gruppo acetile più grande di quest’ultimo.
D: Il cloruro di allile è un alogenuro di vinile primario?
R: Sì, il 3-cloropropene è un alogenuro vinilico primario.
D: Come si può produrre l’epicloridrina dal cloruro di allile?
R: L’epicloridrina può essere prodotta dal 3-cloropropene mediante una reazione di epossidazione utilizzando una miscela di ipoclorito di sodio e acido cloridrico.
