L’eptano è un liquido incolore e infiammabile comunemente usato come solvente. Ha una formula molecolare C7H16 e si trova nella benzina. L’eptano ha sette atomi di carbonio e 16 atomi di idrogeno.
| Nome IUPAC | Eptano |
| Formula molecolare | C7H16 |
| numero CAS | 142-82-5 |
| Sinonimi | n-eptano, dipropilmetano, eptile idruro, ecc. |
| InChI | InChI=1S/C7H16/c1-3-5-7-6-4-2/h3-7H2.1-2H3 |
Proprietà dell’eptano
Formula dell’eptano
La formula chimica dell’eptano è C7H16. È costituito da sette atomi di carbonio e 16 atomi di idrogeno, disposti in una catena lineare. La struttura a catena lineare dell’eptano lo rende un membro importante della famiglia degli idrocarburi degli alcani.
Massa molare dell’eptano
La massa molare di C7H16 è 100,20 g/mol. Questo valore si calcola sommando le masse atomiche di tutti gli atomi presenti in una singola molecola C7H16. La massa molare di C7H16 è un parametro importante in molti calcoli chimici, inclusi stechiometria, termodinamica e cinetica.
Punto di ebollizione dell’eptano
C7H16 ha un punto di ebollizione di 98,42°C (209,16°F). Questo punto di ebollizione relativamente basso lo rende un solvente utile per una varietà di applicazioni, come in laboratorio e nella produzione di benzina. Il punto di ebollizione di C7H16 è influenzato da diversi fattori, tra cui l’intensità delle forze intermolecolari e il peso molecolare del composto.
Punto di fusione dell’eptano
Il punto di fusione di C7H16 è -91°C (-132°F). Questo basso punto di fusione indica che C7H16 è un liquido a temperatura ambiente ed è molto volatile. Il basso punto di fusione di C7H16 è dovuto alle deboli forze di Van der Waals tra le sue molecole.
Densità dell’eptano g/mL
La densità di C7H16 è 0,684 g/mL a 20°C (68°F). La densità di C7H16 è una misura della quantità di massa presente in un dato volume. Questo valore è influenzato da fattori quali temperatura, pressione e purezza del campione.
Peso molecolare dell’eptano
Il peso molecolare di C7H16 è 100,20 g/mol. Questo valore si calcola sommando le masse atomiche di tutti gli atomi presenti in una singola molecola C7H16. Il peso molecolare di C7H16 è un parametro cruciale in molte reazioni chimiche perché aiuta a determinare la quantità di reagenti e prodotti presenti in una miscela di reazione.
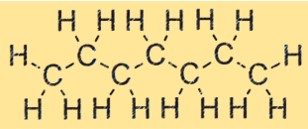
Struttura dell’eptano
C7H16 ha una struttura a catena lineare, con sette atomi di carbonio e 16 atomi di idrogeno disposti in modo lineare. Questa struttura è una caratteristica degli alcani, una famiglia di idrocarburi. La struttura di C7H16 influenza le sue proprietà fisiche e chimiche, inclusi il punto di ebollizione, il punto di fusione e la reattività.
Solubilità dell’eptano
C7H16 è una molecola non polare e scarsamente solubile in solventi polari come l’acqua. Tuttavia, C7H16 è altamente solubile in solventi non polari come esano, benzene e toluene. Questo comportamento di solubilità è dovuto al fatto che il simile si dissolve: le molecole non polari tendono a dissolversi in solventi non polari, mentre le molecole polari tendono a dissolversi in solventi polari.
| Aspetto | Liquido incolore |
| Densità specifica a 25°C | 0,684 g/ml |
| Colore | Incolore |
| Odore | Odore di benzina |
| Massa molare | 100,20 g/mole |
| Densità a 25°C | 0,684 g/ml |
| Punto di fusione | -91°C (-132°F) |
| Punto di ebollizione | 98,42°C (209,16°F) |
| Punto flash | -4°C (25°F) |
| Solubilità in acqua a 25°C | 0,004 g/100 ml |
| Solubilità in altri solventi | Molto solubile in solventi non polari (esano, toluene, benzene) |
| Pressione di vapore a 20°C | 25,31 mmHg |
| Densità di vapore a 20°C | 3,46 (aria = 1) |
| pKa | 50 (stimato) |
| pH | Non applicabile |
Sicurezza e pericoli dell’eptano
C7H16 presenta diversi rischi per la sicurezza, principalmente a causa della sua natura altamente infiammabile. Può facilmente prendere fuoco e rilasciare vapori infiammabili se esposto a calore o fiamme. I vapori di C7H16 possono anche irritare gli occhi, la pelle e il sistema respiratorio, provocando tosse, respiro sibilante e mancanza di respiro. Inoltre, C7H16 può essere dannoso se ingerito, causando nausea, vomito e dolore addominale. Pertanto, è necessario adottare precauzioni adeguate durante la manipolazione di C7H16, ad esempio utilizzare dispositivi di protezione adeguati, garantire una buona ventilazione nell’area di lavoro e tenerlo lontano da fonti di calore e fiamme libere. È inoltre essenziale seguire adeguati protocolli di conservazione, manipolazione e smaltimento di C7H16 per ridurre al minimo eventuali rischi.
| Simboli di pericolo | F, Xi |
| Descrizione della sicurezza | Liquido e vapori altamente infiammabili. Provoca irritazione cutanea. |
| Numeri di identificazione delle Nazioni Unite | ONU 1206 |
| Codice SA | 2902.41.000 |
| Classe di pericolo | 3 (Liquidi infiammabili) |
| Gruppo di imballaggio | II |
| Tossicità | Può essere nocivo se ingerito e può causare irritazione alla pelle e agli occhi |
Metodi di sintesi dell’eptano
Esistono vari metodi per sintetizzare C7H16, ma il metodo principale prevede la distillazione frazionata del petrolio o del petrolio greggio. Questo metodo separa gli idrocarburi in base al loro punto di ebollizione e distillando la parte della miscela che bolle a una temperatura compresa tra 90 e 100°C si ottiene C7H16.
Un altro metodo per sintetizzare C7H16 prevede l’idrogenazione catalitica dell’esene o di altre olefine utilizzando un catalizzatore di palladio a temperature e pressioni elevate.
Utilizzando il processo Fischer-Tropsch, è possibile sintetizzare C7H16 facendo reagire monossido di carbonio e idrogeno gassoso su un catalizzatore di ferro o cobalto a temperature e pressioni elevate. Questo processo produce una miscela di idrocarburi, incluso C7H16, che può essere separata mediante distillazione frazionata.
Per sintetizzare C7H16, è possibile utilizzare un catalizzatore al platino a temperature e pressioni elevate per deidrociclizzare il metilcicloesano. Inoltre, la combinazione di idrocarburi più piccoli ottenuti dal cracking della nafta o di altre frazioni petrolifere può produrre C7H16.
Nel complesso, la sintesi di C7H16 prevede vari metodi, utilizzando principalmente petrolio o petrolio greggio come materie prime, e prevede varie reazioni chimiche come distillazione, idrogenazione e deidrociclizzazione.
Usi dell’eptano
C7H16 ha diverse applicazioni industriali e commerciali, tra cui:
- Solvente: comunemente utilizzato come solvente in vari settori, come quello del petrolio e del gas, della gomma e della produzione di adesivi. Scioglie un’ampia gamma di composti tra cui grassi, oli e resine.
- Carburante: utilizzato come carburante di riferimento per i motori a benzina. Comunemente utilizzato nei laboratori di ricerca per test e sviluppo di motori.
- Estrazione: utilizzato come solvente di estrazione per prodotti naturali, come oli vegetali, estratti vegetali e oli essenziali.
- Pulizia: utilizzato come detergente nell’industria elettronica. Utilizzato per rimuovere contaminanti dai componenti elettronici.
- Reagente di laboratorio: utilizzato come reagente in varie procedure di laboratorio, tra cui l’estrazione del DNA, la cromatografia e la spettroscopia.
- Diluente per vernici: utilizzato come diluente per vernici per diluire le vernici a base di olio e per pulire le attrezzature di verniciatura.
- Adesivo: utilizzato come adesivo in varie applicazioni, come laminazione, incollaggio e sigillatura.
Domande:
D: Qual è il valore di n in ch3(ch2)nch3 se il nome dell’idrocarburo è eptano?
R: Il valore di n in ch3(ch2)nch3 per l’eptano è 5.
D: L’eptano è solubile in acqua?
R: No, C7H16 non è solubile in acqua perché è un idrocarburo non polare e l’acqua è una molecola polare.
D: L’eptano è polare?
R: No, C7H16 è un idrocarburo non polare a causa della sua struttura molecolare simmetrica e dell’eguale condivisione di elettroni tra atomi di carbonio e idrogeno.
D: Cos’è l’eptano?
R: C7H16 è un idrocarburo alcano a catena lineare con la formula chimica C7H16. È un liquido incolore dall’odore caratteristico e viene comunemente utilizzato come carburante di riferimento per i motori a benzina.
D: Come si chiama questo idrocarburo? C7H16
R: Il nome di questo idrocarburo è C7H16.
D: Quanti isomeri di eptano?
R: C7H16 ha nove possibili isomeri, inclusi isomeri a catena lineare e ramificata.
D: L’eptano è volatile?
R: Sì, C7H16 è un liquido volatile con un basso punto di ebollizione di 98,4°C e un’elevata pressione di vapore.
D: Qual è la formula molecolare dell’eptano?
R: La formula molecolare dell’eptano è C7H16.
D: Cos’è più esano o eptano polare?
R: L’esano e il C7H16 sono entrambi idrocarburi non polari, ma C7H16 è leggermente più polare dell’esano a causa delle sue dimensioni molecolari maggiori e delle maggiori forze di dispersione di London.
D: L’eptano è coperto dal PSM?
R: Sì, C7H16 è una sostanza coperta dalle normative sulla gestione della sicurezza dei processi (PSM), che si applicano alle strutture che manipolano, utilizzano o immagazzinano quantità superiori a una soglia di determinate sostanze chimiche pericolose.
