Il tiosolfato di sodio pentaidrato (Na2S2O3 · 5H2O) è un composto cristallino che si dissolve facilmente in acqua. È comunemente usato nell’elaborazione fotografica e come antidoto medico all’avvelenamento da cianuro.
| Nome IUPAC | Sodio tiosolfato pentaidrato |
| Formula molecolare | Na2S2O3 · 5H2O |
| numero CAS | 10102-17-7 |
| Sinonimi | Sodio iposolfito pentaidrato, sodio tiosolfato pentaidrato, sodio tiosolfato idrato, sodio tiosolfato 5-idrato |
| InChi | InChI=1S/2Na.H2O3S2.5H2O/c;;1-5(2,3)4;;;;;/h;;(H2,1,2,3,4);5 1H2/q2 +1; ;;;;;/p-2 |
Proprietà del tiosolfato di sodio pentaidrato
Formula di sodio tiosolfato pentaidrato
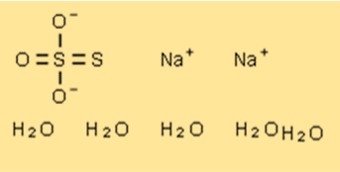
La formula chimica del tiosolfato di sodio pentaidrato è Na2S2O3 · 5H2O. È costituito da due ioni Na+, due ioni (S2O3)2- e cinque molecole d’acqua. Il composto ha un aspetto cristallino bianco ed è altamente solubile in acqua.
Massa molare di sodio tiosolfato pentaidrato
La massa molare di Na2S2O3 · 5H2O è 248,18 g/mol. È la somma delle masse atomiche di sodio, zolfo, ossigeno e idrogeno nel composto. La massa molare è un parametro importante nei calcoli chimici, in particolare per determinare la quantità di sostanza necessaria per una reazione.
Punto di ebollizione del tiosolfato di sodio pentaidrato
Na2S2O3 · 5H2O non ha un punto di ebollizione specifico poiché si decompone se riscaldato. Subisce invece un processo di decomposizione termica che comporta il rilascio di vapore acqueo e anidride solforosa. La temperatura di decomposizione di Na2S2O3 · 5H2O è di circa 48°C.
Sodio tiosolfato pentaidrato Punto di fusione
Il punto di fusione di Na2S2O3 · 5H2O è 48,3°C. A questa temperatura il composto subisce un cambiamento di fase da solido a liquido. Na2S2O3 · 5H2O ha un punto di fusione relativamente basso, attribuito alla presenza di molecole d’acqua nella sua struttura cristallina.
Sodio tiosolfato pentaidrato Densità g/mL
La densità di Na2S2O3 · 5H2O è 1,67 g/mL. Il composto ha una densità relativamente elevata rispetto ad altri sali, dovuta alla presenza di numerosi ioni nella sua struttura cristallina. La densità di una sostanza è definita come la quantità di massa per unità di volume.
Peso molecolare del tiosolfato di sodio pentaidrato
Il peso molecolare di Na2S2O3 · 5H2O è 248,18 g/mol. È la somma dei pesi atomici degli elementi presenti nel composto. Il peso molecolare è un parametro importante nei calcoli chimici, in particolare per determinare la stechiometria di una reazione.
Struttura pentaidrata del tiosolfato di sodio
La struttura cristallina di Na2S2O3 · 5H2O è composta da cationi sodio, anioni tiosolfato e molecole d’acqua. Gli ioni sodio si trovano agli angoli della cella unitaria, mentre gli anioni tiosolfato e le molecole d’acqua sono disposti in una struttura a strati. Gli anioni tiosolfato e le molecole d’acqua formano catene che si estendono lungo l’asse c della cella unitaria.
Solubilità del tiosolfato di sodio pentaidrato
Na2S2O3 · 5H2O è altamente solubile in acqua. La solubilità di una sostanza è definita come la quantità massima di sostanza che può essere disciolta in una data quantità di solvente a una temperatura e pressione specifiche. La solubilità di Na2S2O3 · 5H2O in acqua aumenta con la temperatura e viene utilizzata in varie applicazioni industriali e mediche.
| Aspetto | Solido cristallino bianco |
| Peso specifico | 1,67 g/ml |
| Colore | Bianco |
| Odore | Inodore |
| Massa molare | 248,18 g/mole |
| Densità | 1,67 g/ml |
| Punto di fusione | 48,3°C |
| Punto di ebollizione | Si decompone a 48°C |
| Punto flash | Non applicabile |
| solubilità in acqua | Molto solubile |
| Solubilità | Solubile in acqua e glicerolo |
| Pressione del vapore | Non applicabile |
| Densità del vapore | Non applicabile |
| pKa | 7.2 |
| pH | 6,5-9,5 (soluzione al 5% in acqua) |
Sodio tiosolfato pentaidrato Sicurezza e pericoli
Na2S2O3 · 5H2O è generalmente considerato sicuro da maneggiare e utilizzare. Tuttavia può causare irritazione agli occhi, alla pelle e al sistema respiratorio. L’ingestione di grandi quantità di Na2S2O3 · 5H2O può causare disturbi gastrointestinali. È inoltre importante evitare il contatto con agenti ossidanti e acidi forti, poiché potrebbero reagire violentemente con queste sostanze. Na2S2O3 · 5H2O non è considerato a rischio di incendio o esplosione, ma può emettere fumi tossici se riscaldato fino alla decomposizione. Come per tutti i prodotti chimici, è necessario adottare precauzioni adeguate durante la manipolazione e l’utilizzo di Na2S2O3 · 5H2O per ridurre al minimo eventuali rischi potenziali.
| Simboli di pericolo | Nessuno |
| Descrizione della sicurezza | S24/25 – Evitare il contatto con la pelle e gli occhi |
| Numeri di identificazione delle Nazioni Unite | Non regolato |
| Codice SA | 2832.10.00 |
| Classe di pericolo | Non classificato come pericoloso ai sensi del GHS |
| Gruppo di imballaggio | Non applicabile |
| Tossicità | LD50 (orale, ratto): > 6.000 mg/kg |
Metodi per la sintesi del tiosolfato di sodio pentaidrato
Vari metodi possono sintetizzare Na2S2O3 · 5H2O.
Un metodo comune prevede la reazione del solfito di sodio con lo zolfo in condizioni alcaline. Un altro metodo prevede la reazione dell’idrossido di sodio con l’anidride solforosa, seguita dall’aggiunta di zolfo. Riscaldando la miscela si ottiene Na2S2O3 · 5H2O.
Per sintetizzare Na2S2O3 · 5H2O, i chimici fanno reagire il solfuro di sodio con l’anidride solforosa, dando luogo alla formazione di solfito di sodio. Quindi ossidare il solfito di sodio con perossido di idrogeno o cloro per formare solfato di sodio. La reazione dello zolfo con il solfato di sodio avviene in condizioni alcaline e la miscela risultante viene riscaldata per dare Na2S2O3 · 5H2O.
È importante notare che la sintesi di Na2S2O3 · 5H2O deve essere effettuata con adeguate precauzioni di sicurezza, come l’uso di dispositivi di protezione e un’adeguata ventilazione. Inoltre, la purezza delle materie prime e le condizioni di reazione possono influenzare la resa e la purezza del prodotto finale.
Usi del tiosolfato di sodio pentaidrato
Na2S2O3 · 5H2O ha molti usi in diversi settori grazie alle sue proprietà uniche. Alcuni dei suoi usi comuni includono:
- Fotografia: funziona attivamente come fissatore fotografico per rimuovere l’alogenuro d’argento non esposto dalla pellicola fotografica.
- Medicina: usato come antidoto all’avvelenamento da cianuro perché può reagire con il cianuro per formare il tiocianato meno tossico.
- Trattamento dell’acqua: utilizzato per rimuovere il cloro dall’acqua, che è importante in settori quali piscine, acquari e trattamento delle acque reflue.
- Chimica analitica: Utilizzato come agente riducente nelle titolazioni e come agente complessante nella determinazione dei metalli pesanti.
- Agricoltura: utilizzato come fertilizzante per correggere le carenze di zolfo nelle piante.
- Industria tessile: utilizzato anche come candeggina per tessuti di lana e seta.
- Estrazione dell’oro: utilizzato nell’estrazione dell’oro per estrarre l’oro dai minerali mediante lisciviazione.
- Altri usi: comunemente utilizzato nella produzione di carta, nella produzione di coloranti e come reagente di laboratorio.
Domande:
D: Quanti grammi di tiosolfato di sodio pentaidrato sarebbero necessari per preparare 250,0 ml di 0,1000 M?
R: Per preparare 250,0 ml di soluzione 0,1000 M di Na2S2O3 · 5H2O, sarebbero necessari 9,944 grammi di Na2S2O3 · 5H2O.
D: Come diluire il tiosolfato di sodio pentaidrato?
R: Na2S2O3 · 5H2O può essere diluito sciogliendolo in acqua. La quantità di acqua necessaria dipende dalla concentrazione desiderata della soluzione.
D: Quanti grammi di tiosolfato di sodio pentaidrato solido sono necessari per prepararlo esattamente?
R: La quantità di Na2S2O3 · 5H2O solida necessaria per preparare una soluzione dipende dalla concentrazione e dal volume desiderati della soluzione. È possibile utilizzare la formula C1V1 = C2V2, dove C1 e V1 sono rispettivamente la concentrazione e il volume iniziali, e C2 e V2 sono rispettivamente la concentrazione e il volume finali, per calcolare la quantità di solido richiesta.
D: A cosa serve il tiosolfato di sodio pentaidrato?
R: Na2S2O3 · 5H2O viene utilizzato nella fotografia, nell’industria medica, nel trattamento delle acque, nella chimica analitica, nell’agricoltura, nell’industria tessile, nell’estrazione dell’oro, nella produzione di carta, nella produzione di coloranti e come reagente di laboratorio.
D: Chi vende tiosolfato di sodio pentaidrato?
R: Na2S2O3 · 5H2O è venduto da vari fornitori e distributori di prodotti chimici, sia online che offline. Alcuni esempi includono Sigma-Aldrich, Fisher Scientific e VWR International.
D: Cosa posso usare al posto di Na2S2O3·5H2O per estinguere eventuali reazioni?
R: Esistono vari composti chimici che possono essere utilizzati in alternativa a Na2S2O3 · 5H2O per le reazioni di quenching, a seconda della reazione e dei requisiti specifici. Alcuni esempi includono urea, idrossilammina cloridrato e bisolfito di sodio.
D: Cos’è Na2S2O3·5H2O?
R: Na2S2O3·5H2O è la formula chimica di Na2S2O3·5H2O, un composto cristallino bianco utilizzato in varie applicazioni industriali e di laboratorio.
