Il solfato di zinco è un composto con la formula chimica ZnSO4. È comunemente usato come integratore alimentare per trattare la carenza di zinco e come fertilizzante per le colture.
| Nome IUPAC | Solfato di zinco |
| Formula molecolare | ZnSO4 |
| numero CAS | 7733-02-0 |
| Sinonimi | Vetriolo bianco, vetriolo di zinco, solfato di zinco (II), solfato di zinco (2+), monosolfato di zinco, solfato di zinco eptaidrato, solfato di zinco monoidrato |
| InChI | InChI=1S/2O.H2S.Zn/h2*1H;1H2;/q;;;+2/p-2 |
Formula di solfato di zinco
La formula chimica del solfato di zinco è ZnSO4. È costituito da uno ione zinco (Zn2+) e uno ione solfato (SO42-). La formula mostra che il solfato di zinco contiene un atomo di zinco, un atomo di zolfo e quattro atomi di ossigeno.
Massa molare del solfato di zinco
La massa molare del solfato di zinco (ZnSO4) è 161,44 g/mol. È la somma delle masse atomiche di tutti gli atomi presenti in una mole del composto. Il solfato di zinco è composto da un atomo di zinco (Zn), un atomo di zolfo (S) e quattro atomi di ossigeno (O). La massa molare è un parametro essenziale utilizzato nei calcoli stechiometrici per determinare la quantità di reagenti e prodotti in una reazione chimica.
Punto di ebollizione del solfato di zinco
Il solfato di zinco non ha un punto di ebollizione definito perché si decompone prima di raggiungere il punto di ebollizione. Il composto subisce una decomposizione termica a circa 680°C, formando gas di ossido di zinco (ZnO), anidride solforosa (SO2) e ossigeno (O2). La temperatura di decomposizione è influenzata dalla presenza di impurità, dalla pressione e dalla velocità di riscaldamento. Il solfato di zinco è stabile alle basse temperature ed è solubile in acqua, metanolo ed etanolo.
Punto di fusione del solfato di zinco
Il punto di fusione del solfato di zinco dipende dal livello di idratazione del composto. Il solfato di zinco eptaidrato (ZnSO4.7H2O) ha un punto di fusione di 100°C, mentre il solfato di zinco monoidrato (ZnSO4.H2O) fonde a 70°C. Il solfato di zinco anidro (ZnSO4) si decompone prima di sciogliersi. Il punto di fusione è influenzato da fattori quali pressione, purezza e velocità di riscaldamento.
Densità del solfato di zinco g/ml
La densità del solfato di zinco varia a seconda del suo stato di idratazione. Il solfato di zinco eptaidrato ha una densità di 1,957 g/cm³, il solfato di zinco monoidrato ha una densità di 3,08 g/cm³ e il solfato di zinco anidro ha una densità di 3,54 g/cm³. La densità è una proprietà fisica che determina la quantità di massa per unità di volume di una sostanza. La densità del solfato di zinco è influenzata anche dalla temperatura e dalla pressione.
Peso molecolare del solfato di zinco
Il peso molecolare del solfato di zinco è 161,44 g/mol. Si calcola sommando i pesi atomici di zinco, zolfo e ossigeno, che sono rispettivamente 65,38 g/mol, 32,06 g/mol e 63,998 g/mol. Il peso molecolare viene utilizzato in vari calcoli come la determinazione della concentrazione di soluzioni di solfato di zinco negli esperimenti di chimica e biologia.
Struttura del solfato di zinco
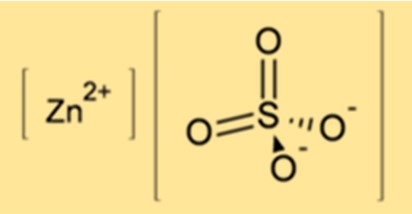
Il solfato di zinco ha una struttura cristallina nella sua forma anidra, con cationi zinco (Zn2+) e anioni solfato (SO42-) disposti alternativamente. Il catione zinco è coordinato da sei atomi di ossigeno provenienti da sei anioni solfato, formando una geometria ottaedrica distorta. In forma idrata, il solfato di zinco eptaidrato forma cristalli monoclini, mentre il solfato di zinco monoidrato forma cristalli ortorombici. Le molecole d’acqua contenute negli idrati sono debolmente legate alla rete del solfato di zinco mediante legami idrogeno.
| Aspetto | Solido cristallino bianco |
| Peso specifico | 3,54 g/cm³ (anidro) |
| Colore | Bianco |
| Odore | Inodore |
| Massa molare | 161,44 g/mole |
| Densità | 1,957 g/cm³ (eptaidrato), 3,08 g/cm³ (monoidrato), 3,54 g/cm³ (anidro) |
| Punto di fusione | 70°C (monoidrato), 100°C (eptaidrato) |
| Punto di ebollizione | Si rompe prima dell’ebollizione |
| Punto flash | Non applicabile |
| solubilità in acqua | Molto solubile |
| Solubilità | Solubile in acqua, metanolo ed etanolo |
| Pressione del vapore | Non applicabile |
| Densità del vapore | Non applicabile |
| pKa | pKa1=1,9, pKa2=3,1, pKa3=9,8 |
| pH | Il pH della soluzione 0,1 M è 4,2 |
Sicurezza e pericoli del solfato di zinco
Il solfato di zinco è generalmente sicuro da maneggiare se utilizzato secondo le istruzioni. Tuttavia, in caso di contatto, può causare irritazione agli occhi, alla pelle e al sistema respiratorio. L’ingestione di grandi quantità può provocare nausea, vomito e diarrea. L’esposizione a lungo termine alla polvere di solfato di zinco può causare irritazione respiratoria o febbre da fumi metallici. È importante indossare adeguati dispositivi di protezione individuale (DPI) come guanti e occhiali protettivi quando si maneggia il solfato di zinco. In caso di esposizione accidentale, lavare abbondantemente le zone interessate con acqua e risciacquare, se necessario consultare un medico. Conservare il solfato di zinco in un contenitore ermeticamente chiuso e lontano da sostanze incompatibili.
| Simboli di pericolo | XI |
| Descrizione della sicurezza | Tenere fuori dalla portata dei bambini. Indossare guanti/indumenti protettivi/proteggere gli occhi/il viso. IN CASO DI CONTATTO CON GLI OCCHI: sciacquare accuratamente con acqua per diversi minuti. Rimuovere le lenti a contatto, se presenti ed è facile da fare. Continua a risciacquare. IN CASO DI INGESTIONE: Sciacquare la bocca. Non provoca il vomito. Chiedi consiglio/assistenza medica se non ti senti bene. Smaltire il contenuto/contenitore in conformità con le normative locali/regionali/nazionali/internazionali. |
| Identificatori AN | Non regolato |
| Codice SA | 2833.29.90 |
| Classe di pericolo | 9 – Merci pericolose varie |
| Gruppo di imballaggio | III |
| Tossicità | Il solfato di zinco è generalmente considerato a bassa tossicità. Tuttavia, l’ingestione di grandi quantità può causare irritazione gastrointestinale e portare a vomito, diarrea e disidratazione. L’inalazione di polvere o nebbia può irritare le vie respiratorie. Il solfato di zinco può causare irritazione agli occhi e alla pelle al contatto. L’esposizione prolungata ad alti livelli di polvere di solfato di zinco può portare alla febbre da fumi metallici. |
Metodi di sintesi del solfato di zinco
Esistono diversi metodi per sintetizzare il solfato di zinco, a seconda della purezza, della dimensione delle particelle e del livello di idratazione desiderati del prodotto finale. Un metodo comune prevede la reazione dello zinco metallico o dell’ossido di zinco con acido solforico:
1. Zinco metallico + acido solforico → solfato di zinco + idrogeno gassoso
2. Ossido di zinco + acido solforico → Solfato di zinco + acqua
Per ottimizzare la resa e la purezza del solfato di zinco, la reazione deve essere condotta in condizioni controllate di temperatura, agitazione e concentrazione di acido. Successivamente, applicare ulteriori fasi di lavorazione come cristallizzazione, essiccazione e setacciatura alla soluzione di solfato di zinco risultante per ottenere la dimensione delle particelle e il livello di idratazione desiderati.
Un altro metodo per produrre solfato di zinco prevede la reazione del minerale di zinco o del concentrato con acido solforico:
3. Minerale/concentrato di zinco + acido solforico → solfato di zinco + solfato di ferro + acqua
Il solfato di zinco può essere separato dal solfato di ferro e da altre impurità utilizzando tecniche quali filtrazione, precipitazione o estrazione con solvente.
Per produrre solfato di zinco, il carbonato di zinco o l’idrossido di zinco possono essere fatti reagire con acido solforico, oppure la cenere di zinco può essere ossidata con acido solforico.
La scelta del metodo dipende da fattori quali la disponibilità delle materie prime, i costi e le specifiche del prodotto.
Usi del solfato di zinco
Il solfato di zinco ha una vasta gamma di applicazioni industriali, agricole e mediche grazie alle sue proprietà uniche. Ecco alcuni usi comuni del solfato di zinco:
- Fertilizzante: utilizzato come fertilizzante micronutriente che fornisce zinco essenziale alle piante per una crescita e uno sviluppo sani.
- Mangimi per animali: aggiunto ai mangimi per animali come integratore nutrizionale per prevenire la carenza di zinco e migliorare la salute generale.
- Trattamento dell’acqua: utilizzato negli impianti di trattamento dell’acqua per rimuovere le impurità e ridurre la torbidità.
- Galvanizzazione: utilizzata nel processo di zincatura, che prevede il rivestimento di ferro e acciaio con uno strato di zinco per prevenire la corrosione.
- Medicina: usato in medicina come integratore alimentare per trattare la carenza di zinco, nonché in unguenti topici per trattare condizioni della pelle come eczema e acne.
- Tintura: utilizzata nella tintura e nella stampa dei tessuti per migliorare la solidità del colore e la brillantezza dei coloranti.
- Galvanotecnica: utilizzato nella galvanica per depositare uno strato di zinco su superfici metalliche per protezione dalla corrosione e scopi decorativi.
- Ritardante di fiamma: utilizzato come ritardante di fiamma in plastica, gomma e altri materiali per ridurre il rischio di incendio.
- Altri usi: Utilizzato nella produzione di pigmenti, carta, saponi e detergenti.
Domande:
D: Cosa osserveresti quando lo zinco viene aggiunto a una soluzione di solfato di ferro?
R: Quando lo zinco viene aggiunto ad una soluzione di solfato di ferro, si verifica una reazione di spostamento. Lo zinco più reattivo sposta il ferro meno reattivo dalla soluzione di solfato, formando solfato di zinco e ferro metallico. La reazione può essere osservata come la formazione di un solido bruno-rossastro e il rilascio di gas idrogeno.
D: Cosa succede quando un pezzo di zinco viene aggiunto a una soluzione di solfato di rame?
R: Quando un pezzo di zinco metallico viene aggiunto a una soluzione di solfato di rame, si verifica una reazione di spostamento. Lo zinco è più reattivo del rame, quindi sposta il rame dalla soluzione di solfato, formando solfato di zinco e un solido bruno-rossastro di rame metallico. La reazione può essere osservata quando la soluzione diventa blu quando gli ioni rame vengono rilasciati nella soluzione e si forma un deposito di rame solido sulla superficie dello zinco metallico.
D: Il solfato di zinco è un sale?
R: Sì, il solfato di zinco è un sale composto da ioni zinco (Zn2+) e ioni solfato (SO42-). È un composto cristallino bianco con la formula ZnSO4 ed è comunemente usato in varie applicazioni come fertilizzanti, mangimi per animali e medicinali.
D: Dove acquistare la polvere di solfato di zinco?
R: La polvere di solfato di zinco può essere acquistata presso fornitori di prodotti chimici, rivenditori online e negozi di forniture agricole. È importante assicurarsi che il prodotto sia di alta qualità e adatto all’uso previsto.
D: Il solfato di zinco è solubile?
R: Sì, il solfato di zinco è solubile in acqua e glicerolo. La solubilità del solfato di zinco varia con la temperatura, con maggiore solubilità a temperature più elevate. La solubilità può anche essere influenzata dalla presenza di altri ioni nella soluzione.
D: A cosa serve il solfato di zinco?
R: Il solfato di zinco ha varie applicazioni, incluso l’uso come fertilizzante, integratore per mangimi per animali, agente per il trattamento dell’acqua, medicine e nella produzione di pigmenti, carta e tessuti. Viene utilizzato anche nella galvanica, nei ritardanti di fiamma e come integratore alimentare per trattare la carenza di zinco e sostenere la salute generale.
