Il blu di bromotimolo (BTB) è un indicatore di pH che cambia colore dal giallo al blu in presenza di una soluzione basica. È comunemente usato negli esperimenti scientifici e come strumento diagnostico medico.
| Nome IUPAC | 3′,3”-dibromotimolsulfonftaleina |
| Formula molecolare | C27H28Br2O5S |
| numero CAS | 76-59-5 |
| Sinonimi | bromotimolo sulfonftaleina; 4,4′-(1,1-diossido-3H-2,1-benzossatiole-3,3-diil)bis(2-bromo-3-metil-6-(1-metiletil)fenolo) |
| InChI | InChI=1S/C27H28Br2O5S/c1-13(2)17-11-20(15(5)23(28)18(17)7-9-19(24(20)29)8-10-21(27) 22(30)12-25(31)32)37(33,34)36-26-14(3)6-4-16(35-26)24-7-9-29-11-10-23( 24)28/h4-7.9-12.31-32H.8H2.1-3H3 |
Massa molare del blu di bromotimolo
BTB ha una massa molare di 624,38 g/mol. La massa molare è la massa di una mole di una sostanza ed è comunemente utilizzata nei calcoli che coinvolgono reazioni chimiche. La massa molare di BTB viene calcolata sommando i pesi atomici di tutti gli atomi nella sua formula chimica, che è C27H28Br2O5S. Conoscere la massa molare di una sostanza è importante per determinare la quantità di sostanza necessaria per una determinata reazione, nonché per determinare la quantità di prodotto prodotto in una reazione.
Punto di ebollizione del blu di bromotimolo
BTB ha un punto di ebollizione di 636,3°C a 760 mmHg. Il punto di ebollizione è la temperatura alla quale una sostanza passa dallo stato liquido allo stato gassoso ad una determinata pressione. L’alto punto di ebollizione del BTB indica che si tratta di un composto stabile che non vaporizza né si decompone facilmente in condizioni normali. Il punto di ebollizione di una sostanza può essere utilizzato per determinarne la purezza, poiché le impurità possono modificare il punto di ebollizione.
Blu di bromotimolo Punto di fusione
BTB ha un punto di fusione di 165-170°C. Il punto di fusione è la temperatura alla quale una sostanza solida passa dallo stato solido allo stato liquido. Il punto di fusione di una sostanza viene utilizzato per identificarla e caratterizzarla, poiché sostanze diverse hanno punti di fusione diversi. Il punto di fusione del BTB è relativamente alto, il che indica che si tratta di un composto stabile che non si decompone facilmente.
Blu di bromotimolo Densità g/ml
BTB ha una densità di 1,36 g/ml. La densità è la massa di una sostanza per unità di volume e misura quanto sono dense le molecole di una sostanza. La densità del BTB indica che si tratta di un composto relativamente denso ed è comunemente utilizzato come standard nelle misurazioni della densità.
Peso molecolare del blu di bromotimolo
Il peso molecolare del BTB è 624,38 g/mol. Il peso molecolare è la somma dei pesi atomici di tutti gli atomi di una molecola ed è un fattore importante nelle reazioni chimiche. Il peso molecolare del BTB viene utilizzato per determinare la quantità di sostanza necessaria per una determinata reazione, nonché per determinare la quantità di prodotto prodotto in una reazione.
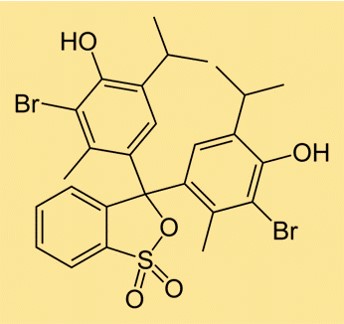
Struttura del blu di bromotimolo
La struttura del BTB è composta da due anelli aromatici, a ciascuno dei quali è attaccato un atomo di bromo. C’è anche un gruppo solfonato attaccato a uno degli anelli, che rende la molecola solubile in acqua. La struttura del BTB è simile ad altri indicatori di pH, utilizzati per determinare l’acidità o la basicità di una soluzione.
Formula blu di bromotimolo
La formula chimica del BTB è C27H28Br2O5S. La formula indica il numero e il tipo di atomi nella molecola e viene utilizzata nelle reazioni chimiche per determinare la quantità di sostanza necessaria per una determinata reazione. La formula del BTB mostra che contiene due atomi di bromo, che gli conferiscono il suo caratteristico colore giallo-verde in soluzioni acide, e un gruppo solfonato, che lo rende solubile in acqua.
| Aspetto | Polvere verde scuro |
| Peso specifico | 1.36 |
| Colore | verde giallastro |
| Odore | Inodore |
| Massa molare | 624,38 g/mole |
| Densità | 1,36 g/ml |
| Punto di fusione | 165-170°C |
| Punto di ebollizione | 636,3°C a 760 mmHg |
| Punto flash | Non applicabile |
| solubilità in acqua | Solubile |
| Solubilità | Solubile in etanolo, leggermente solubile in etere e cloroformio |
| Pressione del vapore | Non applicabile |
| Densità del vapore | Non applicabile |
| pKa | 6.3 |
| pH | Giallo a pH 6,0, verde a pH 7,6, blu a pH 7,9 |
Sicurezza e pericoli del blu di bromotimolo
Il BTB può essere dannoso se ingerito, inalato o assorbito attraverso la pelle. Ciò potrebbe causare irritazione agli occhi, alla pelle e al sistema respiratorio. L’ingestione può causare irritazione gastrointestinale, nausea, vomito e dolore addominale. L’inalazione di polvere o vapori di BTB può causare irritazione respiratoria, tosse e difficoltà respiratorie. La sostanza può anche essere dannosa per la vita acquatica e non deve essere smaltita nelle fonti d’acqua. Quando si maneggia BTB è necessario indossare dispositivi di protezione individuale adeguati, come guanti e protezione per gli occhi, e devono essere utilizzati e smaltiti in conformità con le procedure e le normative di laboratorio appropriate.
| Simboli di pericolo | Nessuno |
| Descrizione della sicurezza | S22: Non respirare le polveri. S24/25: Evitare il contatto con la pelle e gli occhi. S36/37/39: Indossare indumenti protettivi, guanti e proteggersi gli occhi/il viso adeguati. |
| Identificatori AN | Non regolato |
| Codice SA | 2921.59.90 |
| Classe di pericolo | Non classificato |
| Gruppo di imballaggio | Non applicabile |
| Tossicità | LD50 (orale, ratto) = 4.500 mg/kg |
Metodi per la sintesi del blu di bromotimolo
Esistono diversi metodi per sintetizzare BTB.
Un metodo comune è la reazione tra blu timolo e bromo in presenza di un catalizzatore acido forte, come l’acido cloridrico. La reazione procede mediante addizione elettrofila di bromo alla molecola di blu timolo, seguita dalla sostituzione di un atomo di idrogeno con un atomo di bromo. Il composto risultante è BTB.
Un altro metodo prevede la reazione tra il 2,6-dibromoindofenolo e il rosso cresolo in presenza di un catalizzatore acido forte. La reazione avviene per sostituzione elettrofila di un atomo di idrogeno nella molecola del rosso cresolo con un atomo di bromo nella molecola del 2,6-dibromoindofenolo. Il composto risultante è BTB.
Un terzo metodo prevede la reazione tra blu di timolo e bromuro di sodio in presenza di idrossido di sodio. La reazione avviene sostituendo un atomo di idrogeno nella molecola del blu timolo con un atomo di bromo della molecola di bromuro di sodio. Il composto risultante è BTB.
Indipendentemente dal metodo utilizzato, il prodotto risultante deve essere purificato mediante ricristallizzazione o cromatografia su colonna per ottenere BTB puro.
Usi del blu di bromotimolo
BTB ha numerose applicazioni in vari campi. Alcuni degli usi di BTB includono:
- Indicatore: utilizzato come indicatore acido-base, con un intervallo di pH compreso tra 6,0 e 7,6. A pH 6,0 è giallo, a pH 7,6 è verde e a pH 7,9 è blu.
- Esperimenti di laboratorio: utilizzato in vari esperimenti di laboratorio per verificare la presenza di anidride carbonica e altri gas e per determinare il quoziente respiratorio.
- Acquacoltura: utilizzato in acquacoltura per monitorare i livelli di pH dell’acqua negli acquari e negli stagni.
- Campo medico: utilizzato per testare la presenza di bile nei campioni di urina e per rilevare la presenza di infezioni fungine.
- Istruzione: utilizzato nell’istruzione come supporto visivo per dimostrare i principi delle reazioni acido-base e per insegnare agli studenti i livelli di pH.
- Industria agricola: utilizzato per misurare i livelli di pH del suolo, un fattore importante nel determinare la salute e la crescita delle piante.
- Test ambientali: utilizzati nei test ambientali per misurare i livelli di pH delle fonti d’acqua, come laghi e fiumi, per garantirne l’idoneità alla vita acquatica.
Nel complesso, BTB è un composto versatile con molte applicazioni in vari campi.
Domande:
D: Cos’è il blu di bromotimolo?
R: BTB è un indicatore di pH comunemente utilizzato negli esperimenti di laboratorio e in varie altre applicazioni. È un composto chimico che cambia colore a seconda dell’acidità o dell’alcalinità di una soluzione.
D: Qual è l’intervallo di pH del blu di bromotimolo?
R: L’intervallo di pH di BTB è compreso tra 6,0 e 7,6. A pH 6,0 è giallo, a pH 7,6 è verde e a pH 7,9 è blu.
D: Qual è il cambiamento di colore del blu di bromotimolo?
R: Il cambiamento di colore del BTB dipende dal pH della soluzione. A pH 6,0 è giallo, a pH 7,6 è verde e a pH 7,9 è blu.
D: Il blu di bromotimolo è un acido o una base? R: BTB non è né un acido né una base. È un indicatore che cambia colore a seconda dell’acidità o dell’alcalinità di una soluzione.
