L’acido tartarico è un acido organico naturale presente in molti frutti e verdure, comunemente utilizzato nelle industrie alimentari e delle bevande come esaltatore di sapidità, conservante e regolatore di acidità.
| Nome IUPAC | Acido 2,3-diidrossibutandioico |
| Formula molecolare | C4H6O6 |
| numero CAS | 87-69-4 |
| Sinonimi | acido 2,3-diidrossisuccinico; acido 2,3-diidrossibutandioico; acido alfa-idrossi-beta-ossosuccinico; acido 2-idrossi-2,3-diidrossibutandioico; acido 2-idrossibutan-1,2,3-tricarbossilico; acido 2-idrossi-1,2,3-propantricarbossilico; acido racemico; acido tartarico naturale; acido L-(+)-tartarico; acido D-(-)-tartarico; acido mesotatatartarico; tartrato; acido tartronico |
| InChI | InChI=1S/C4H6O6/c5-1(3(7)8)2(6)4(9)10/h1-2.5-6H,(H,7.8)(H,9.10) |
Formula dell’acido tartarico
La formula chimica dell’acido tartarico è C4H6O6. La formula mostra il numero e il tipo di atomi presenti in una singola molecola di acido tartarico. La molecola contiene quattro atomi di carbonio, sei atomi di ossigeno e sei atomi di idrogeno. La formula è importante per determinare la stechiometria delle reazioni che coinvolgono l’acido tartarico e per calcolare la sua massa molare.
Massa molare dell’acido tartarico
L’acido 2,3-diidrossisuccinico ha una massa molare di 150,09 g/mol, che è la somma dei pesi atomici di tutti gli atomi in una singola molecola di acido 2,3-diidrossisuccinico. Questo acido organico ha due gruppi carbossilici e due gruppi idrossilici, rendendolo un acido dicarbossilico. La sua massa molare è importante per determinare la quantità di acido 2,3-diidrossisuccinico necessaria in diverse applicazioni.
Punto di ebollizione dell’acido tartarico
L’acido 2,3-diidrossisuccinico ha un punto di ebollizione relativamente alto di 214°C (417°F) a pressione standard. Questa temperatura è molto più alta del punto di ebollizione dell’acqua, rendendo l’acido 2,3-diidrossisuccinico molto stabile alle alte temperature. Questa proprietà è importante per il suo utilizzo nell’industria alimentare e delle bevande perché può resistere alle alte temperature utilizzate nella lavorazione degli alimenti e può essere utilizzata come conservante naturale.
Punto di fusione dell’acido tartarico
L’acido 2,3-diidrossisuccinico ha un punto di fusione compreso tra 170 e 172 ° C (tra 338 e 342 ° F). Il suo punto di fusione è importante per determinarne le proprietà fisiche, come la solubilità e la viscosità, nonché per la fabbricazione di diversi prodotti che richiedono acido 2,3-diidrossisuccinico.
Densità dell’acido tartarico g/ml
La densità dell’acido 2,3-diidrossisuccinico è 1,79 g/ml, il che significa che un millilitro di acido 2,3-diidrossisuccinico pesa 1,79 grammi. Questa proprietà è importante per determinare la concentrazione dell’acido 2,3-diidrossisuccinico in diverse soluzioni ed è cruciale nella produzione di sali dell’acido 2,3-diidrossisuccinico.
Peso molecolare dell’acido tartarico
Il peso molecolare dell’acido 2,3-diidrossisuccinico è 150,09 g/mol. Questa proprietà è importante per determinare la quantità di acido 2,3-diidrossisuccinico necessaria in diverse applicazioni e la stechiometria delle reazioni che coinvolgono l’acido 2,3-diidrossisuccinico.
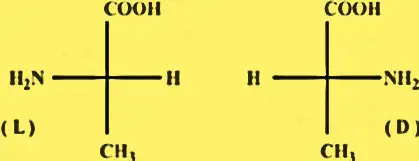
Struttura dell’acido tartarico
L’acido tartarico ha un carbonio chirale, il che significa che esiste in due diversi stereoisomeri, acido L-(+)-2,3-diidrossisuccinico e acido D-(-)-2,3-diidrossisuccinico. . I due isomeri hanno la stessa formula molecolare e gli stessi gruppi funzionali ma differiscono nella loro disposizione spaziale. L’acido 2,3-diidrossisuccinico ha due gruppi di acido carbossilico e due gruppi idrossilici, rendendolo un acido dicarbossilico. La molecola ha un atomo di carbonio centrale legato a due gruppi ossidrile e due gruppi carbossilici.
| Aspetto | Polvere cristallina bianca o cristalli incolori |
| Peso specifico | 1,79 |
| Colore | Incolore |
| Odore | Inodore |
| Massa molare | 150,09 g/mole |
| Densità | 1,79 g/ml a 25°C |
| Punto di fusione | 170-172°C (338-342°F) |
| Punto di ebollizione | 214°C (417°F) |
| Punto flash | Non applicabile |
| solubilità in acqua | 133 g/l (20°C) |
| Solubilità | Solubile in acqua, etanolo ed etere |
| Pressione del vapore | 0,00013 mmHg a 25°C |
| Densità del vapore | Non applicabile |
| pKa | pKa1 = 2,98; pKa2 = 4,34; pKa3 = 5,40 |
| pH | 2,2 (soluzione 0,1 milioni) |
Nota: le proprietà fisico-chimiche dell’acido 2,3-diidrossisuccinico possono variare a seconda della forma specifica del composto, come stereoisomero, forma salina o concentrazione. Questi valori si riferiscono alla forma standard dell’acido 2,3-diidrossisuccinico.
Sicurezza e pericoli dell’acido tartarico
L’acido 2,3-diidrossisuccinico è generalmente riconosciuto come sicuro (GRAS) dalla Food and Drug Administration (FDA) degli Stati Uniti ed è ampiamente utilizzato nell’industria alimentare e delle bevande. Tuttavia, come qualsiasi sostanza chimica, l’acido 2,3-diidrossisuccinico può comportare alcuni pericoli se non maneggiato correttamente. Il contatto diretto con l’acido 2,3-diidrossisuccinico può causare irritazione alla pelle e agli occhi e l’ingestione può causare disturbi gastrointestinali. L’inalazione di polvere di acido 2,3-diidrossisuccinico può causare irritazione respiratoria. Anche l’acido 2,3-diidrossisuccinico è una sostanza combustibile e può presentare pericolo di incendio se esposto a temperature elevate o fiamme. Quando si lavora con questa sostanza chimica è necessario adottare adeguate precauzioni di sicurezza, come indossare dispositivi di protezione e maneggiare l’acido 2,3-diidrossisuccinico in aree ben ventilate.
Metodi di sintesi dell’acido tartarico
L’acido 2,3-diidrossisuccinico può essere sintetizzato con diversi metodi. Un metodo comune è l’idrolisi del tartrato acido di potassio, ottenuto dai residui del succo d’uva e della produzione del vino. Il tartrato acido di potassio viene prima miscelato con acqua e riscaldato per produrre acido 2,3-diidrossisuccinico e idrossido di potassio. La soluzione risultante viene quindi neutralizzata con acido cloridrico per produrre cristalli di acido 2,3-diidrossisuccinico.
Un altro metodo prevede l’ossidazione di alcuni carboidrati, come il glucosio o il saccarosio, utilizzando l’acido nitrico. La miscela risultante viene quindi trattata con carbonato di calcio per far precipitare il tartrato di calcio, che viene poi acidificato con acido solforico per produrre acido 2,3-diidrossisuccinico.
Un terzo metodo prevede la reazione dell’anidride maleica con acido glicolico o glicina per produrre acido 2,3-diidrossisuccinico. Questo metodo viene spesso utilizzato per la produzione di acido 2,3-diidrossisuccinico ad elevata purezza da utilizzare in prodotti farmaceutici o altre applicazioni sensibili.
Usi dell’acido tartarico
L’acido 2,3-diidrossisuccinico ha un’ampia gamma di usi in vari settori.
- L’industria alimentare utilizza l’acido tartarico come acidificante naturale per conferire un sapore aspro ai propri prodotti. L’acido 2,3-diidrossisuccinico viene utilizzato anche nei prodotti alimentari e nelle bevande come agente di controllo del pH, stabilizzante e esaltatore di sapidità, come nelle bevande analcoliche, nelle caramelle e nei prodotti da forno.
- L’industria farmaceutica utilizza l’acido 2,3-diidrossisuccinico come eccipiente nella produzione di compresse e capsule e come agente chelante per migliorare la solubilità e la biodisponibilità di alcuni farmaci.
- I prodotti cosmetici come maschere e peeling contengono acido 2,3-diidrossisuccinico per le sue proprietà esfolianti e schiarenti. L’acido 2,3-diidrossisuccinico viene utilizzato come agente tampone nelle tinture per capelli e nei decoloranti nell’industria cosmetica.
- Le applicazioni industriali dell’acido 2,3-diidrossisuccinico includono il suo utilizzo come agente sequestrante nella placcatura dei metalli, come inibitore delle incrostazioni nel trattamento delle acque e come componente nella produzione di adesivi, tessuti e prodotti in plastica. carta.
Domande:
Quanti stereoisomeri sono possibili per l’acido tartarico?
L’acido tartarico ha due centri chirali, il che significa che può potenzialmente contenere quattro stereoisomeri. Tuttavia, a causa della sua simmetria interna, solo tre di questi stereoisomeri sono effettivamente possibili. I tre stereoisomeri sono: acido meso-tartarico (achirale), acido L-(+)-tartarico (destrogiro) e acido D-(-)-tartarico (levotatorio).
L’acido tartarico è un acido forte?
L’acido tartarico è un acido organico debole, il che significa che non si dissocia completamente in acqua e ha una costante di dissociazione acida (pKa) relativamente bassa. I suoi valori pKa sono circa 2,98 e 4,34, indicando che si tratta di un acido debole. In confronto, un acido forte, come l’acido cloridrico (HCl), ha un valore pKa molto più basso, indicando che è completamente dissociato in acqua ed è un acido molto più basso. più forte dell’acido 2,3-diidrossisuccinico. Tuttavia, anche se l’acido 2,3-diidrossisuccinico può essere considerato un acido debole, grazie alla sua origine naturale, al suo stato sicuro e alle sue varie funzionalità, ha ancora molte applicazioni pratiche in vari settori, tra cui quello alimentare e delle bevande, farmaceutico e cosmetico.
Qual è il pH dell’acido tartarico?
Il pH dell’acido tartarico dipende dalla concentrazione della soluzione e dalla costante di dissociazione (pKa) dell’acido 2,3-diidrossisuccinico. L’acido 2,3-diidrossisuccinico è un acido debole e ha due valori di pKa di circa 2,98 e 4,34. A basse concentrazioni, l’acido 2,3-diidrossisuccinico è solo parzialmente dissociato e il pH della sua soluzione è leggermente acido, tipicamente compreso tra 2,8 e 3,5. Tuttavia, a concentrazioni più elevate, il pH della soluzione di acido 2,3-diidrossisuccinico può diminuire a causa dell’aumento della ionizzazione, risultando in una soluzione più acida. È importante notare che il pH di una soluzione di acido 2,3-diidrossisuccinico dipende anche dalla presenza di altri acidi e basi nella soluzione, nonché dalla temperatura e da altri fattori ambientali.
