Il cicloesanolo o C6H11OH è un liquido oleoso incolore con un leggero odore. È comunemente usato come solvente e nella produzione di nylon e altri prodotti chimici.
| Nome IUPAC | Cicloesanolo |
| Formula molecolare | C6H12O o C6H11OH |
| numero CAS | 108-93-0 |
| Sinonimi | esaidrofenolo; idrofenolo; Alcool cicloesilico; esalino; Cicloesanololo |
| Struttura chimica | InChI=1S/C6H12O/c7-6-4-2-1-3-5-6/h6-7H,1-5H2 |
Struttura del cicloesanolo
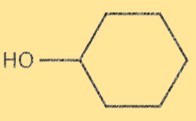
Il cicloesanolo ha un anello di carbonio a sei membri con un gruppo ossidrile (-OH) attaccato a uno degli atomi di carbonio. La formula molecolare del cicloesanolo è C6H12O. L’anello del cicloesano ha una conformazione carne con il gruppo ossidrile situato in posizione assiale. La struttura del cicloesanolo è importante perché ne determina le proprietà fisiche e chimiche.
Formula del cicloesanolo
La formula chimica del cicloesanolo è C6H12O. Questo rappresenta il numero e il tipo di atomi in una molecola di cicloesanolo. La formula è importante perché viene utilizzata per calcolare la quantità di cicloesanolo necessaria in una reazione. Inoltre, viene utilizzato per determinare la stechiometria di una reazione.
Spettro IR del cicloesanolo
Lo spettro IR del cicloesanolo mostra un picco ampio e forte a circa 3400 cm-1 a causa della presenza del gruppo ossidrile (-OH). Questo picco è indicativo della presenza di alcol. Inoltre, lo spettro mostra diversi picchi nell’intervallo 1000–1300 cm-1 dovuti alla presenza dell’anello del cicloesano. Lo spettro IR del cicloesanolo è importante perché può essere utilizzato per identificare e caratterizzare la sostanza.
Massa molare del cicloesanolo
La somma delle masse atomiche di tutti gli atomi di una molecola di cicloesanolo permette di calcolare la sua massa molare, che è 100,16 g/mol. La massa molare gioca un ruolo cruciale nel determinare la quantità di cicloesanolo richiesta in una reazione e nella conversione tra grammi e moli nei calcoli stechiometrici.
Punto di ebollizione del cicloesanolo
Il punto di ebollizione del cicloesanolo è 161,5°C (322,7°F). Questa è la temperatura alla quale la fase liquida del cicloesanolo si trasforma in fase gassosa. Il punto di ebollizione è una proprietà fisica importante perché viene utilizzato per purificare e separare il cicloesanolo dalle altre sostanze in una miscela. Il punto di ebollizione relativamente alto del cicloesanolo lo rende utile come solvente nelle reazioni che richiedono temperature elevate.
C6H11OH Punto di fusione
C6H11OH ha un punto di fusione di 25,93°C (78,67°F). Questa è la temperatura alla quale la fase solida di C6H11OH si trasforma nella fase liquida. Il punto di fusione è una proprietà fisica importante perché viene utilizzato per identificare e caratterizzare C6H11OH. Viene utilizzato anche per determinare la purezza di C6H11OH.
C6H11OH Densità g/mL
C6H11OH ha una densità di 0,962 g/mL a 25°C (77°F). Questa è la massa di C6H11OH per unità di volume della sostanza. La densità è una proprietà fisica importante perché viene utilizzata per determinare la massa di C6H11OH necessaria per una reazione. Inoltre, viene utilizzato per calcolare la concentrazione di C6H11OH in una soluzione.
Peso molecolare C6H11OH
C6H11OH ha un peso molecolare di 100,16 g/mol. È la somma dei pesi atomici di tutti gli atomi in una molecola C6H11OH. Il peso molecolare è una proprietà importante perché viene utilizzato per calcolare la quantità di C6H11OH necessaria in una reazione. Inoltre, viene utilizzato per convertire tra grammi e moli nei calcoli stechiometrici.
| Aspetto | Liquido incolore |
| Peso specifico | 0,962 g/ml |
| Colore | Incolore |
| Odore | Leggero odore |
| Massa molare | 100,16 g/mole |
| Densità | 0,962 g/ml |
| Punto di fusione | 25,93°C (78,67°F) |
| Punto di ebollizione | 161,5°C (322,7°F) |
| Punto flash | 70°C (158°F) |
| solubilità in acqua | Miscibile |
| Solubilità | Solubile in molti solventi organici |
| Pressione del vapore | 0,14 kPa (a 25°C) |
| Densità del vapore | 3,5 (aria = 1) |
| pKa | 16.1 |
| pH | dalle 6 alle 8 |
Nota: i valori presentati in questa tabella sono approssimativi e possono variare a seconda della fonte delle informazioni.
Sicurezza e pericoli del cicloesanolo
C6H11OH deve essere maneggiato con cautela in quanto comporta determinati rischi e pericoli per la sicurezza. L’esposizione a questa sostanza chimica può causare irritazione alla pelle, agli occhi e al sistema respiratorio. Può anche causare mal di testa, vertigini e nausea se inalato. L’ingestione di C6H11OH può causare dolore addominale, vomito e diarrea. Questa sostanza chimica è infiammabile e può accendersi se esposta a calore o fiamme. È importante conservarlo e maneggiarlo in un luogo fresco e asciutto, lontano da fonti di calore e fonti di ignizione. Durante la manipolazione di C6H11OH è necessario utilizzare dispositivi di protezione come guanti, occhiali e respiratori. In caso di esposizione, consultare immediatamente un medico.
| Simboli di pericolo | XI |
| Descrizione della sicurezza | S26 – In caso di contatto con gli occhi, lavare immediatamente e abbondantemente con acqua e consultare un medico.<br> S36/37/39 – Usare indumenti protettivi, guanti e dispositivi di protezione per gli occhi/occhi adatti. viso.<br>S45 – In caso di incidente o di malessere consultare immediatamente un medico (se possibile, mostrargli l’etichetta). |
| Identificatori AN | ONU1986 |
| Codice SA | 2907.13.00 |
| Classe di pericolo | 3 |
| Gruppo di imballaggio | III |
| Tossicità | Tossicità da bassa a moderata |
Metodi di sintesi del cicloesanolo
C6H11OH può essere sintetizzato con diversi metodi.
- Un metodo comune per produrre C6H11OH consiste nell’idrogenare cataliticamente il fenolo in presenza di un catalizzatore metallico come nichel o platino. Questo metodo prevede la riduzione dell’anello aromatico del fenolo per formare C6H11OH.
- Un altro metodo prevede l’ossidazione del cicloesano utilizzando aria o ossigeno in presenza di un catalizzatore come rame o cobalto. Questo processo produce C6H11OH come prodotto intermedio che può essere ulteriormente ossidato per formare cicloesanone.
- C6H11OH può anche essere ottenuto mediante idrolisi del cicloesile acetato utilizzando un catalizzatore acido o basico. Questo metodo prevede la scissione del legame estere nel cicloesile acetato per formare C6H11OH e acido acetico.
- Il riarrangiamento di Beckmann della cicloesanone ossima utilizzando acido solforico come catalizzatore è un altro metodo per sintetizzare C6H11OH. Questo processo prevede la riorganizzazione del gruppo ossima nel cicloesanone ossima per formare un intermedio ammidico, che può essere idrolizzato per produrre C6H11OH.
Nel complesso, la sintesi di C6H11OH richiede che gli individui eseguano vari processi chimici e utilizzino precauzioni e attrezzature di sicurezza adeguate.
Usi del cicloesanolo
C6H11OH ha molte applicazioni in diversi settori.
- Le industrie utilizzano C6H11OH come solvente per produrre lacche, vernici e resine e come solvente per preparare farmaci nell’industria farmaceutica.
- C6H11OH funge da importante intermedio nella produzione di acido adipico, un componente necessario nella produzione del nylon. Agisce anche come materia prima per la sintesi di varie sostanze chimiche, tra cui bisfenolo A, cicloesanone e caprolattame.
- L’industria petrolifera aggiunge C6H11OH come inibitore della corrosione al petrolio greggio per prevenire la corrosione nelle condutture e nei serbatoi di stoccaggio.
- I produttori utilizzano C6H11OH per produrre plastificanti che migliorano la flessibilità e la durata della plastica. È anche un ingrediente comune nei profumi e nei cosmetici.
- C6H11OH è utilizzato come fluido termovettore, lubrificante e pesticida. Inoltre, serve come reagente nella sintesi organica e negli esperimenti di laboratorio.
Nel complesso, C6H11OH ha una vasta gamma di applicazioni in vari settori e le sue proprietà versatili lo rendono una sostanza chimica importante in molti processi industriali.
Domande:
Il cicloesanolo è solubile in acqua?
Il cicloesanolo è moderatamente solubile in acqua, ma la sua solubilità diminuisce all’aumentare della temperatura. È più solubile in solventi organici come etanolo, etere etilico e acetone. La solubilità di C6H11OH in acqua è dovuta alla formazione di legami idrogeno tra il gruppo ossidrile di C6H11OH e le molecole d’acqua. Tuttavia, l’anello idrofobo del cicloesano di C6H11OH riduce la sua polarità complessiva, rendendolo meno solubile in acqua rispetto ad altri alcoli più polari come metanolo ed etanolo. La solubilità di C6H11OH in acqua è una considerazione importante nel suo utilizzo come solvente e nei processi industriali che coinvolgono l’acqua come mezzo.
Quale delle seguenti serie di reazioni converte il cicloesanolo in 1,2-epossicicloesano?
Per convertire il cicloesanolo in 1,2-epossicicloesano, è possibile eseguire la seguente serie di reazioni:
- Il cicloesanolo viene prima trattato con un catalizzatore acido forte come l’acido solforico per formare cicloesene attraverso la disidratazione.
- Il cicloesene risultante reagisce quindi con un peracido come l’acido m-cloroperbenzoico (MCPBA) per formare un epossido, in particolare 1,2-epossicicloesano.
Pertanto, la serie corretta di reazioni per convertire il cicloesanolo in 1,2-epossicicloesano prevede la disidratazione del cicloesanolo per formare cicloesene seguita dall’epossidazione del cicloesene per formare 1,2-epossicicloesano utilizzando un peracido.
Perché il cicloesanolo non ha bisogno di un prefisso numerico?
Il cicloesanolo non necessita di un prefisso numerico nel suo nome perché è un singolo isomero del cicloesanolo. Gli isomeri sono molecole con la stessa formula molecolare ma con diverse disposizioni strutturali degli atomi. Il cicloesanolo ha un singolo gruppo funzionale ossidrile (-OH) attaccato a un anello di cicloesano e la sua formula molecolare è C6H12O. Poiché esiste una sola possibile disposizione degli atomi nel cicloesanolo, non è necessario un prefisso numerico per specificarne la posizione o il numero di gruppi funzionali. Al contrario, altri composti come il cicloesanone e il cicloesandione hanno più isomeri con diverse posizioni e numeri di gruppi carbonilici e quindi richiedono prefissi numerici per specificare la posizione dei gruppi funzionali.
