L’acetato di zinco (Zn(C2H3O2)2) è un composto chimico. I suoi usi sono numerosi nelle industrie e nei laboratori. È solubile in acqua e può formare strutture cristalline bianche.
| Nome IUPAC | Acetato di zinco |
| Formula molecolare | Zn(C2H3O2)2 |
| numero CAS | 557-34-6 |
| Sinonimi | Diacetato di zinco, etanoato di zinco, sale di zinco dell’acido acetico |
| InChI | InChI=1S/2C2H4O2.Zn/c2 1-2(3)4;/h2 1H3,(H,3,4);/q;;+2/p-2 |
Proprietà dell’acetato di zinco
Formula di acetato di zinco
La formula chimica dell’etanoato di zinco è Zn(C2H3O2)2. È costituito da uno ione zinco (Zn) e due ioni acetato (C2H3O2). La formula rappresenta il rapporto tra gli atomi presenti nel composto.
Massa molare dell’acetato di zinco
La massa molare dell’etanoato di zinco può essere calcolata sommando le masse atomiche di ciascun elemento nella formula. Per lo zinco (Zn), la massa atomica è 65,38 g/mol, mentre per l’acetato (C2H3O2) è 59,05 g/mol. Pertanto, la massa molare dell’etanoato di zinco è di circa 183,39 g/mol.
Punto di ebollizione dell’acetato di zinco
L’etanoato di zinco non ha un punto di ebollizione distinto, poiché tende a decomporsi e perdere acido acetico quando riscaldato. Invece, si decompone in ossido di zinco e acido acetico ad alte temperature.
Punto di fusione dell’acetato di zinco
L’etanoato di zinco ha un punto di fusione di circa 237°C (459°F). A questa temperatura il composto solido si trasforma nello stato liquido. Il punto di fusione è una caratteristica importante utilizzata per l’identificazione.
Densità dell’acetato di zinco g/mL
La densità dell’etanoato di zinco è di circa 1,84 g/mL. La densità è la misura della massa per unità di volume di una sostanza. La densità dell’etanoato di zinco è relativamente elevata, indicando la sua compattezza.
Peso molecolare dell’acetato di zinco
Il peso molecolare dell’etanoato di zinco è 183,39 g/mol. È la somma dei pesi atomici di tutti gli atomi presenti nel composto. Il peso molecolare è fondamentale per vari calcoli e reazioni chimiche.
Struttura in acetato di zinco
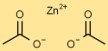
L’etanoato di zinco ha una struttura semplice, con lo ione zinco (Zn) al centro circondato da due ioni acetato (C2H3O2). Gli ioni acetato formano legami covalenti coordinati con lo ione zinco.
Solubilità dell’acetato di zinco
L’etanoato di zinco è solubile in acqua e altri solventi polari. La solubilità in acqua è relativamente alta e forma una soluzione incolore. La solubilità del composto è essenziale per le sue varie applicazioni nelle industrie e nei laboratori.
| Proprietà | Valore |
| Aspetto | Cristalli bianchi |
| Peso specifico | 1,84 g/ml |
| Colore | Incolore |
| Odore | Inodore |
| Massa molare | 183,39 g/mole |
| Densità | 1,84 g/cm³ |
| Punto di fusione | 237°C (459°F) |
| Punto di ebollizione | Decomposto |
| Punto flash | Non applicabile |
| solubilità in acqua | Solubile |
| Solubilità | Solubile in acqua e altri solventi polari |
| Pressione del vapore | Non disponibile |
| Densità del vapore | Non disponibile |
| pKa | Non disponibile |
| pH | Neutro (7) |
Sicurezza e pericoli dell’acetato di zinco
L’etanoato di zinco presenta rischi minimi per la sicurezza se maneggiato correttamente. Ciò potrebbe causare una leggera irritazione alla pelle e agli occhi. Evitare l’inalazione o l’ingestione poiché ciò potrebbe causare disturbi respiratori e gastrointestinali. Conservare in un luogo fresco e asciutto, lontano da sostanze incompatibili. Indossare dispositivi di protezione adeguati durante la manipolazione. In caso di contatto, sciacquare le zone interessate con abbondante acqua. Consultare un medico se l’irritazione persiste. Seguire le buone pratiche di laboratorio e le istruzioni di sicurezza per prevenire incidenti. Sebbene sia generalmente sicuro, una gestione responsabile e misure precauzionali sono essenziali per garantire un ambiente di lavoro sicuro.
| Simboli di pericolo | Nessuno |
| Descrizione della sicurezza | Provoca leggera irritazione cutanea, Provoca irritazione oculare, Evitare l’inalazione/ingestione. |
| Numeri di identificazione delle Nazioni Unite | Non applicabile |
| Codice SA | 29152900 |
| Classe di pericolo | Non classificato |
| Gruppo di imballaggio | Non applicabile |
| Tossicità | Bassa tossicità |
Metodi di sintesi dell’acetato di zinco
Esistono diversi metodi per sintetizzare l’etanoato di zinco. Un approccio comune prevede la reazione tra ossido di zinco (ZnO) e acido acetico (CH3COOH) . Le due sostanze vengono miscelate e la reazione avviene ad alta temperatura. Durante il processo, l’ossido di zinco reagisce con l’acido acetico, formando etanoato di zinco e acqua.
Un altro metodo prevede la reazione dello zinco metallico con acido acetico . Lo zinco metallico viene aggiunto all’acido acetico e avviene la reazione, producendo etanoato di zinco e gas idrogeno.
In alternativa, l’etanoato di zinco può essere preparato facendo reagire il carbonato di zinco (ZnCO3) con acido acetico. Il carbonato di zinco reagisce con l’acido acetico per produrre etanoato di zinco, anidride carbonica e acqua.
Inoltre, l’etanoato di zinco può essere ottenuto trattando l’idrossido di zinco (Zn(OH)2) con acido acetico. La reazione tra queste sostanze dà etanoato di zinco e acqua.
Indipendentemente dal metodo utilizzato, l’etanoato di zinco risultante può essere ulteriormente purificato mediante processi di cristallizzazione o filtrazione. È necessario prestare attenzione durante la sintesi per garantire la sicurezza e ottenere un prodotto di alta qualità.
Usi dell’acetato di zinco
L’etanoato di zinco trova un’ampia gamma di applicazioni in vari settori grazie alle sue proprietà versatili. Alcuni dei suoi usi comuni includono:
- Industria farmaceutica: l’etanoato di zinco contribuisce attivamente alla funzione immunitaria e alla guarigione delle ferite, poiché le aziende farmaceutiche lo incorporano in vari farmaci e integratori alimentari per fornire una fonte di zinco.
- Industria tessile: nell’industria tessile, viene utilizzato come mordente nei processi di tintura per fissare e migliorare la solidità del colore dei coloranti tessili sui tessuti.
- Sintesi chimica: l’etanoato di zinco agisce come catalizzatore nelle reazioni organiche, facilitando i processi di esterificazione e acetilazione.
- Conservazione del legno: le formulazioni per il trattamento del legno utilizzano etanoato di zinco per proteggere dagli attacchi di funghi e termiti, prolungando la vita dei prodotti in legno.
- Galvanizzazione: nella zincatura, l’etanoato di zinco funge da precursore nella produzione di rivestimenti di zinco, fornendo resistenza alla corrosione all’acciaio e ad altri metalli.
- Applicazioni di laboratorio: ricercatori e scienziati utilizzano l’etanoato di zinco come reagente in vari esperimenti di laboratorio e procedure analitiche.
- Prodotti per la cura della pelle: unguenti e creme contengono etanoato di zinco per le sue proprietà astringenti e lenitive, benefiche per condizioni della pelle come l’acne.
- Antighiaccio: alcune aree utilizzano l’etanoato di zinco come antighiaccio ecologico su strade e marciapiedi in inverno per prevenire la formazione di ghiaccio.
- Desolforazione del gas: l’etanoato di zinco trova applicazione nei processi di depurazione del gas per rimuovere i composti di zolfo dalle emissioni industriali.
- Industria alimentare: nell’industria alimentare, l’etanoato di zinco agisce come additivo alimentare, fungendo da regolatore di acidità e stabilizzante in alcuni alimenti trasformati.
Nel complesso, le varie applicazioni dell’etanoato di zinco dimostrano la sua importanza in diversi settori, rendendolo un composto prezioso in vari processi di produzione e ricerca.
Domande:
D: Quale sostanza è importante nella produzione della plastica?
R: L’acido acetico è essenziale nella produzione della plastica poiché viene comunemente utilizzato come materia prima nella produzione di vari polimeri sintetici.
D: Cos’è l’acetato di zinco?
R: L’etanoato di zinco è un composto chimico formato dalla reazione dell’ossido di zinco o dello zinco metallico con acido acetico, che dà come risultato un solido cristallino bianco.
D: Qual è la formula dell’acetato di zinco?
R: La formula per l’etanoato di zinco è Zn(C2H3O2)2.
D: L’acetato di zinco è solubile?
R: Sì, l’etanoato di zinco è solubile in acqua e in altri solventi polari.
D: L’acetato di zinco e il gluconato di zinco sono anticoagulanti?
R: No, l’etanoato di zinco e il gluconato di zinco non sono anticoagulanti. Queste sono forme di zinco utilizzate come integratori alimentari.
D: L’acido zinco acetico è un solido?
R: L’acido zinco acetico non è un composto specifico. Potrebbe riferirsi al prodotto di reazione dello zinco con acido acetico, che sarebbe un composto di zinco solido.
D: Quale elemento e composto ha la stessa reazione chimica dello zinco e dell’acido acetico?
R: L’elemento è lo zinco (Zn) e il composto è l’ossido di zinco (ZnO), che reagisce allo stesso modo dello zinco e dell’acido acetico.
D: Qual è l’equazione bilanciata per zinco e acido acetico?
R: L’equazione bilanciata è: Zn + 2CH3COOH → Zn(CH3COO)2 + H2.
D: Cosa fa l’acetato di zinco per la pelle?
R: L’etanoato di zinco viene utilizzato nei prodotti per la cura della pelle per le sue proprietà astringenti, che aiutano a lenire e alleviare condizioni della pelle come l’acne.
