L’acido borico è una polvere bianca con proprietà antisettiche. Può essere utilizzato come insetticida, fungicida o come ingrediente in colliri e soluzioni antisettiche.
| Nome IUPAC | Acido borico |
| Formula molecolare | H₃BO₃ |
| numero CAS | 10043-35-3 |
| Sinonimi | Acido boracico, acido ortoborico, triidrossidoboro |
| InChI | InChI=1S/BH3O3/c2-1(3)4/h2-4H |
Tieni presente che l’InChI fornito è una versione semplificata e potresti voler consultare database chimici affidabili per informazioni più dettagliate e accurate.
Proprietà dell’acido borico
Formula di acido borico
La formula dell’acido ortoborico è H₃BO₃. È costituito da tre atomi di idrogeno, un atomo di boro e tre atomi di ossigeno. La formula rappresenta la composizione dell’acido ortoborico a livello molecolare.
Massa molare dell’acido borico
La massa molare dell’acido ortoborico è di circa 61,83 grammi per mole. Si determina sommando le masse atomiche dei suoi elementi costitutivi secondo la formula molecolare H₃BO₃.
Punto di ebollizione dell’acido borico
L’acido ortoborico ha un punto di ebollizione di circa 300 gradi Celsius (572 gradi Fahrenheit). Questa temperatura indica il punto in cui l’acido ortoborico passa dalla fase liquida a quella gassosa quando riscaldato.
Punto di fusione dell’acido borico
Il punto di fusione dell’acido ortoborico è di circa 170 gradi Celsius (338 gradi Fahrenheit). Questa temperatura indica il punto in cui l’acido ortoborico passa dalla fase solida a quella liquida quando riscaldato.
Densità dell’acido borico g/mL
La densità dell’acido ortoborico è di circa 1,44 grammi per millilitro. La densità è una misura della quantità di massa contenuta in un dato volume. Nel caso dell’acido ortoborico questo valore rappresenta la compattezza della sostanza.
Peso molecolare dell’acido borico
Il peso molecolare dell’acido ortoborico è di circa 61,83 grammi per mole. Si calcola sommando i pesi atomici dei singoli atomi in una singola molecola di acido ortoborico.
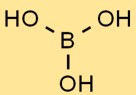
Struttura dell’acido borico
L’acido ortoborico ha una struttura unica costituita da atomi di boro legati a tre gruppi idrossilici (OH). Forma una disposizione planare trigonale con l’atomo di boro al centro e i gruppi idrossilici che si estendono verso l’esterno.
Solubilità dell’acido borico
L’acido ortoborico è moderatamente solubile in acqua. Si dissolve facilmente in acqua, soprattutto quando l’acqua viene riscaldata. La solubilità dell’acido ortoborico in acqua è influenzata da fattori quali temperatura e pH.
| Aspetto | Polvere cristallina bianca |
| Peso specifico | 1.435 g/cm³ |
| Colore | Incolore |
| Odore | Inodore |
| Massa molare | 61,83 g/mole |
| Densità | 1,44 g/ml |
| Punto di fusione | 170°C (338°F) |
| Punto di ebollizione | 300°C (572°F) |
| Punto flash | Non applicabile |
| solubilità in acqua | 25 g/l a 20°C |
| Solubilità | Solubile in solventi come alcool, glicerolo |
| Pressione del vapore | 0,001 mmHg a 25°C |
| Densità del vapore | Non applicabile |
| pKa | 9.14 |
| pH | Circa 5,1 (soluzione 0,1 milioni) |
Si prega di notare che questi valori sono approssimativi e possono variare a seconda delle condizioni specifiche e della purezza del campione di acido ortoborico.
Sicurezza e pericoli dell’acido borico
L’acido ortoborico può comportare alcuni rischi per la sicurezza se maneggiato o utilizzato in modo errato. È importante prendere le precauzioni necessarie. Evitare il contatto diretto con la pelle, gli occhi e gli indumenti poiché ciò potrebbe causare irritazione. L’ingestione di grandi quantità può essere tossica e causare problemi di salute. Quando si lavora con acido ortoborico, garantire una buona ventilazione per evitare l’inalazione di polvere o vapori. In caso di ingestione o esposizione accidentale consultare immediatamente un medico. Conservare l’acido ortoborico in un luogo sicuro fuori dalla portata di bambini e animali domestici. Seguire le corrette procedure di smaltimento per ridurre al minimo l’impatto ambientale. Il rispetto delle precauzioni di sicurezza favorisce una manipolazione sicura e riduce al minimo i potenziali rischi associati all’acido ortoborico.
| Simboli di pericolo | Xn (dannoso) |
| Descrizione della sicurezza | Evitare il contatto con la pelle e gli occhi. Utilizzare con ventilazione adeguata. Rivolgersi al medico se ingerito o esposto. Tenere lontano dalla portata dei bambini e degli animali domestici. Seguire le corrette procedure di smaltimento. |
| Numeri di identificazione delle Nazioni Unite | UN3077 |
| Codice SA | 2810.00.90 |
| Classe di pericolo | 9 (Sostanze e oggetti pericolosi vari) |
| Gruppo di imballaggio | III (Pericolo minore) |
| Tossicità | Moderatamente tossico se ingerito in grandi quantità. Può causare irritazione al contatto. |
Metodi di sintesi dell’acido borico
Esistono diversi metodi per sintetizzare l’acido ortoborico.
Metodo di acidificazione del borace: il borace, noto anche come borato di sodio, viene acidificato per produrre acido ortoborico. Per produrre acido ortoborico puro, mescola una soluzione di borace con un acido forte, come acido cloridrico (HCl) o acido solforico (H₂SO₄) . L’acido reagisce con il borace, rilasciando acido ortoborico come precipitato. Filtrare, lavare ed asciugare il precipitato per ottenere acido ortoborico puro.
Nel metodo dell’idrolisi dell’ossido di boro, idrolizzare l’ossido di boro (B₂O₃) facendolo reagire con acqua (H₂O) in condizioni controllate, solitamente a temperature elevate. La reazione tra B₂O₃ e H₂O produce acido ortoborico come prodotto principale. Concentrare, cristallizzare ed essiccare la soluzione di acido ortoborico risultante per ottenere acido ortoborico solido.
L’industria utilizza ampiamente i due metodi sopra menzionati per produrre acido ortoborico. La scelta del metodo dipende da fattori quali la disponibilità delle materie prime, la purezza desiderata e la scala di produzione. È importante notare che questi metodi di sintesi implicano l’uso di misure di sicurezza adeguate e il rispetto delle normative applicabili per garantire la manipolazione e la produzione sicure dell’acido ortoborico.
Usi dell’acido borico
L’acido ortoborico trova ampie applicazioni in vari settori grazie alle sue proprietà versatili. Ecco alcuni usi comuni dell’acido ortoborico:
- Insetticida e controllo dei parassiti: l’acido ortoborico controlla efficacemente i parassiti come formiche, scarafaggi e termiti interrompendo il loro sistema digestivo, eliminandoli infine.
- Preservante del legno: L’acido ortoborico preserva il legno proteggendolo dagli attacchi di funghi e insetti. Le persone generalmente lavorano il legno per l’edilizia, i mobili e altre strutture in legno.
- Ritardante di fiamma: l’acido ortoborico migliora le proprietà ritardanti di fiamma di materiali come tessuti, tappezzerie e isolanti, riducendone così l’infiammabilità e prevenendo la propagazione del fuoco.
- Colliri e soluzioni per lenti a contatto: i produttori utilizzano acido ortoborico nella produzione di colliri e soluzioni per lenti a contatto per pulire e lubrificare gli occhi, alleviando secchezza e irritazione.
- Tampone pH: a causa della sua natura debolmente acida, l’acido ortoborico agisce come tampone pH in vari prodotti. Aiuta a mantenere i livelli di pH desiderati nei cosmetici, nei prodotti per la cura personale e nelle formulazioni farmaceutiche.
- Usi antisettici e medicinali: l’acido ortoborico ha proprietà antisettiche, che lo rendono utile nel trattamento di ferite minori, infezioni della pelle e alcune patologie oculari. Vari preparati farmaceutici utilizzano anche l’acido ortoborico nella loro produzione.
- Industria del vetro e della ceramica: l’acido ortoborico è un ingrediente essenziale nella produzione di vetro, ceramica e fibra di vetro resistenti al calore. Ciò aiuta a migliorare la robustezza, la durata e la resistenza al calore di questi materiali.
Gli utilizzatori dell’acido ortoborico comprendono un’ampia gamma di applicazioni, come evidenziato dagli esempi sopra menzionati. Le sue diverse proprietà lo rendono un composto prezioso in vari settori, dai prodotti domestici ai processi industriali.
Domande:
D: Cosa succede quando si aggiunge acido borico all’acqua?
R: Quando l’acido ortoborico viene aggiunto all’acqua, si dissolve e forma una soluzione di acido ortoborico.
D: L’acido borico è un acido protico? Spiegare.
R: Sì, l’acido ortoborico è un acido protico perché può donare un protone (H+) durante una reazione chimica.
D: Come preparare l’acido borico?
R: L’acido ortoborico può essere preparato mediante acidificazione del borace (borato di sodio) o mediante idrolisi dell’ossido di boro (B₂O₃).
D: Come sciogliere l’acido borico in acqua?
R: Per sciogliere l’acido ortoborico in acqua, aggiungilo semplicemente all’acqua e mescola finché l’acido ortoborico non si dissolve completamente.
D: Il borace è uguale all’acido borico?
R: No, il borace (borato di sodio) non è la stessa cosa dell’acido ortoborico (H₃BO₃), sebbene entrambi contengano boro.
D: Cos’è l’acido borico?
R: L’acido ortoborico è un composto cristallino bianco con proprietà antisettiche, insetticide e conservanti, comunemente utilizzato in varie applicazioni.
D: Dove acquistare l’acido borico?
R: L’acido ortoborico può essere acquistato da diverse fonti, inclusi rivenditori online, farmacie e negozi che vendono prodotti chimici o prodotti per la casa.
D: L’acido borico è sicuro per l’uomo?
R: L’acido ortoborico può essere tossico se ingerito in grandi quantità, ma se usato come indicato e in quantità adeguate, è generalmente considerato sicuro per l’uomo.
D: Quali sostanze sono basi? Seleziona tutto ciò che si applica: NaOH, KOH, H₃BO₃, NaCl, Ca(OH)₂, Fe₂O₃.
R: Le basi tra le sostanze indicate sono NaOH, KOH, Ca(OH)₂.
D: Quale formula rappresenta l’acido borico? H₃B, H₃BO₃, HBr, H₃PO₄.
R: La formula dell’acido ortoborico è H₃BO₃.
D: Qual è il numero di ossidazione del boro (B) in H₃BO₃?
R: Il numero di ossidazione del boro (B) in H₃BO₃ è +3.
D: H₃BO₃ è un acido forte?
R: No, H₃BO₃ (acido ortoborico) è un acido debole.
D: H₃BO₃ è un elettrolita forte o debole?
R: H₃BO₃ (acido ortoborico) è un elettrolita debole.
