La nitroglicerina è un composto esplosivo usato in medicina per trattare l’angina. Rilassa i vasi sanguigni, migliorando la circolazione sanguigna e riducendo il dolore al petto. Maneggiare con estrema cautela a causa della sua volatilità.
| Nome IUPAC | 1,2,3-trinitroossipropan-2-il nitrato |
| Formula molecolare | C3H5N3O9 |
| numero CAS | 55-63-0 |
| Sinonimi | Trinitrato di glicerile, Trinitroglicerina, NG, Nitrospan, Nitrostat |
| InChI | InChI=1S/C3H5N3O9/c7-4(8)13-1-3(15-6(11)12)2-14-5(9)10/h3H,1-2H2 |
Proprietà della nitroglicerina
Formula di nitroglicerina
La formula della trinitroglicerina è C3H5N3O9. È costituito da tre atomi di carbonio (C), cinque atomi di idrogeno (H), tre atomi di azoto (N) e nove atomi di ossigeno (O). La struttura molecolare della trinitroglicerina è caratterizzata dalla presenza di diversi gruppi nitrato legati ad una molecola di glicerolo.
Massa molare della nitroglicerina
La massa molare della trinitroglicerina è di circa 227,09 grammi per mole. Si calcola sommando le masse atomiche di ciascun elemento nella formula chimica (C3H5N3O9). La massa molare gioca un ruolo cruciale nel determinare la quantità di trinitroglicerina richiesta per varie applicazioni.
Punto di ebollizione della nitroglicerina
La trinitroglicerina è un composto altamente volatile con un basso punto di ebollizione. Bolle a circa 55 gradi Celsius (131 gradi Fahrenheit). Il basso punto di ebollizione consente alla trinitroglicerina di passare facilmente dallo stato liquido a quello gassoso, contribuendo alle sue proprietà esplosive.
Punto di fusione della nitroglicerina
Il punto di fusione della trinitroglicerina è di circa 13 gradi Celsius (55 gradi Fahrenheit). Questo punto di fusione relativamente basso consente alla trinitroglicerina di esistere in forma liquida a temperatura ambiente. Tuttavia, a causa della sua sensibilità al calore e agli urti, richiede un’attenta manipolazione per evitare detonazioni accidentali.
Densità della nitroglicerina g/mL
La densità della trinitroglicerina è di circa 1,6 grammi per millilitro (g/mL). Ciò significa che un millilitro di trinitroglicerina pesa 1,6 grammi. La densità relativamente elevata della trinitroglicerina contribuisce alla sua stabilità e consente un facile stoccaggio e trasporto.
Peso molecolare della nitroglicerina
Il peso molecolare della trinitroglicerina è di circa 227,09 grammi per mole. È la somma dei pesi atomici di tutti gli atomi in una molecola di trinitroglicerina. Il peso molecolare fornisce informazioni importanti per i calcoli chimici e per determinare la quantità di trinitroglicerina necessaria in varie applicazioni.
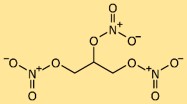
Struttura della nitroglicerina
La struttura della trinitroglicerina è costituita da una molecola di glicerolo (propan-1,2,3-triolo) legata a tre gruppi nitrato (-NO3). I gruppi nitrato sono attaccati a diversi atomi di carbonio nella struttura principale del glicerolo. Questa disposizione molecolare unica contribuisce alla natura esplosiva della trinitroglicerina.
Solubilità della nitroglicerina
La trinitroglicerina è solubile in alcuni solventi organici come etanolo, acetone ed etere. Tuttavia, è solo leggermente solubile in acqua. Questa limitata solubilità in acqua rende difficile la somministrazione orale di trinitroglicerina, che viene spesso somministrata per altre vie come compresse sublinguali o cerotti transdermici per scopi medici.
| Aspetto | Liquido giallo |
| Peso specifico | 1,6 g/ml |
| Colore | Giallo pallido |
| Odore | Leggero odore |
| Massa molare | 227,09 g/mole |
| Densità | 1,6 g/ml |
| Punto di fusione | 13°C (55°F) |
| Punto di ebollizione | 55°C (131°F) |
| Punto flash | 30°C (86°F) |
| solubilità in acqua | Leggermente solubile |
| Solubilità | Solubile in solventi organici come etanolo, acetone, etere |
| Pressione del vapore | 0,1 mmHg |
| Densità del vapore | 8.2 (aria = 1) |
| pKa | 7,7 (pKa1), 8,8 (pKa2), 9,3 (pKa3) |
| pH | Neutro |
Sicurezza e pericoli della nitroglicerina
La trinitroglicerina presenta notevoli rischi per la sicurezza a causa della sua natura esplosiva. È molto sensibile al calore, agli urti e all’attrito, il che lo rende estremamente pericoloso se maneggiato in modo improprio. Può esplodere con grande forza, causando lesioni gravi o mortali. È necessario seguire rigorosi protocolli di sicurezza quando si maneggia la nitroglicerina, compreso l’uso di dispositivi di protezione adeguati e la conservazione in un luogo sicuro, fresco e asciutto. È fondamentale evitare scintille, fiamme libere o fonti di ignizione nelle vicinanze. Particolare attenzione deve essere posta al trasporto e allo stoccaggio per evitare incidenti e ridurre al minimo il rischio di esplosione.
| Simboli di pericolo | Esplosivo, tossico acuto |
| Descrizione della sicurezza | Molto esplosivo. Maneggiare con estrema cautela. Evitare calore, scintille e fiamme libere. |
| Numeri di identificazione delle Nazioni Unite | ONU 0143 (Liquido) |
| Codice SA | 2909.10.00 |
| Classe di pericolo | 1.1D (Esplosivi) |
| Gruppo di imballaggio | PG II (pericolo medio) |
| Tossicità | Tossico per ingestione o inalazione. |
Metodi di sintesi della nitroglicerina
Vari metodi possono sintetizzare la nitroglicerina.
Un approccio comune prevede la reazione tra acido nitrico concentrato (HNO3) e glicerolo (C3H8O3) . La reazione avviene in condizioni attentamente controllate, solitamente con l’aggiunta di acido solforico (H2SO4) come catalizzatore. Mantenere una bassa temperatura e aggiungere lentamente glicerolo a una miscela di acido nitrico concentrato e acido solforico per sintetizzare la nitroglicerina.
Un altro metodo prevede l’uso di acido misto, che è una combinazione di acido nitrico e acido solforico. Aggiungere glicerolo all’acido misto controllando la temperatura durante la sintesi della nitroglicerina.
In entrambi i metodi, l’acido nitrico agisce come agente ossidante, reagendo con il glicerolo per formare nitroglicerina. L’acido solforico aiuta la reazione fornendo un ambiente adatto e agendo come catalizzatore.
È importante notare che la sintesi della nitroglicerina richiede grande cura e competenza a causa della sua natura altamente esplosiva. Seguire sempre rigorose misure di sicurezza per ridurre al minimo il rischio di incidenti durante tutto il processo.
Dopo la sintesi, la soluzione di nitroglicerina risultante viene spesso purificata mediante lavaggio e filtrazione per rimuovere le impurità.
Nel complesso, la sintesi della nitroglicerina comporta una serie di reazioni chimiche che richiedono un controllo preciso e il rispetto dei protocolli di sicurezza per garantire un processo sicuro e di successo.
Usi della nitroglicerina
La trinitroglicerina ha diversi usi importanti in vari campi grazie alle sue proprietà uniche. Ecco alcune applicazioni chiave della nitroglicerina:
- Trattamento dell’angina: i medici usano comunemente la nitroglicerina in medicina per alleviare e prevenire l’angina, una condizione che causa dolore al petto a causa della riduzione del flusso sanguigno al cuore. Rilassa i vasi sanguigni, migliorando la circolazione sanguigna e riducendo il dolore al petto.
- Esplosivi: la trinitroglicerina è l’ingrediente principale di molti esplosivi. L’elevata potenza esplosiva e la sensibilità lo rendono adatto per applicazioni quali attività minerarie, edili e militari.
- Produzione industriale: la trinitroglicerina funge da precursore per la sintesi di altri composti esplosivi, come la dinamite e il TNT (trinitrotoluene). Queste sostanze sono ampiamente utilizzate nei settori dell’edilizia, delle cave e della demolizione.
- Pirotecnica: i fuochi d’artificio e gli spettacoli pirotecnici utilizzano la nitroglicerina per creare effetti visivi vibranti e abbaglianti.
- Chimica analitica: i chimici analitici utilizzano la nitroglicerina come composto standard per determinare le prestazioni e l’efficacia di vari strumenti e metodi analitici.
- Stabilizzatori e propulsori: trova applicazione nei propellenti per razzi e missili, fornendo la spinta necessaria per l’esplorazione spaziale e i sistemi di difesa.
- Proiettili di artiglieria: i produttori incorporano la nitroglicerina nei proiettili di artiglieria per migliorarne la potenza esplosiva e l’efficacia sul campo di battaglia.
- Ricerca scientifica: i laboratori utilizzano la nitroglicerina per scopi di ricerca, compresi studi sul comportamento esplosivo, sulla fisica delle onde d’urto e sulle reazioni chimiche.
I vari usi della nitroglicerina ne evidenziano l’importanza in campo medico, industriale e scientifico, ma con molta cautela a causa della sua natura esplosiva.
Domande:
D: A cosa serve la nitroglicerina?
R: La trinitroglicerina rilassa i vasi sanguigni, migliora la circolazione sanguigna e aiuta a ridurre il dolore al petto (angina).
D: Cos’è la nitroglicerina?
R: La trinitroglicerina è un composto esplosivo utilizzato in medicina per trattare l’angina e negli esplosivi per varie applicazioni industriali e militari.
D: A cosa serve la nitroglicerina?
R: La trinitroglicerina è usata per trattare l’angina, come componente esplosivo e in settori come quello minerario, edile e pirotecnico.
D: Come funziona la nitroglicerina?
R: La trinitroglicerina agisce rilasciando ossido nitrico, che rilassa i muscoli lisci, compresi quelli dei vasi sanguigni, portando a un miglioramento del flusso sanguigno.
D: Come funziona la nitroglicerina nel corpo?
R: Nel corpo, la trinitroglicerina viene convertita in ossido nitrico, che dilata i vasi sanguigni e riduce il carico di lavoro del cuore.
D: Quale singolo legame presente nella nitroglicerina è probabilmente il più corto?
R: Il legame singolo tra carbonio e azoto (CN) nella trinitroglicerina è probabilmente il più breve.
D: La nitroglicerina è un betabloccante?
R: No, la trinitroglicerina non è un beta bloccante. Appartiene a una classe di farmaci chiamati nitrati.
D: Quale singolo legame presente nella nitroglicerina è il meno polare?
R: Il singolo legame tra carbonio e carbonio (CC) nella trinitroglicerina è il meno polare.
D: Come veniva prodotta la nitroglicerina nel Far West?
R: Nel Vecchio West, la trinitroglicerina veniva tipicamente prodotta mescolando glicerolo con acidi nitrico e solforico concentrati in condizioni controllate.
D: Come esplode la nitroglicerina?
R: La trinitroglicerina esplode se sottoposta a calore, shock o attrito, provocando un rapido rilascio di gas e un considerevole aumento di volume e pressione.
D: Che odore ha la nitroglicerina?
R: La trinitroglicerina ha un leggero odore, spesso descritto come leggermente dolce o etereo.
